Clear Sky Science · pt
A cereblon induz a degradação do neossubstrato G3BP2 usando mimetismo da superfície molecular
Transformando a Limpeza Celular em um Sistema de Alvo Inteligente
Medicamentos modernos tentam cada vez mais tratar doenças não apenas bloqueando proteínas problemáticas, mas eliminando-as por completo. Este artigo explora uma forma engenhosa de reprogramar uma das próprias «máquinas de limpeza» da célula para que, quando combinada a uma pequena molécula, reconheça e destrua uma proteína associada ao câncer e a outros distúrbios. O trabalho revela um truque inesperado: a máquina de limpeza remodela parte de sua superfície para imitar um dos parceiros naturais da proteína, permitindo que ela se prenda e envie a proteína para o descarte celular.
O Coletor de Lixo da Célula com Flexibilidade Oculta
Nossas células marcam constantemente proteínas desgastadas ou indesejadas para destruição, usando um sistema centrado em ligases E3 — grandes complexos proteicos que decidem o que deve ser eliminado. Um desses complexos depende de um componente chamado cereblon, que atua como um sensor que reconhece características específicas («degrons») em outras proteínas. Certos medicamentos aprovados já exploram o cereblon atuando como «colas moleculares»: eles se ligam ao cereblon e criam uma nova superfície de ancoragem que atrai proteínas relacionadas a doenças, que então são marcadas e degradadas. Até agora, a maioria dos alvos conhecidos apresentava um padrão estrutural particular, o que parecia limitar o conjunto de proteínas passíveis de remoção por esse mecanismo.
Descobrindo um Novo Alvo Fora das Regras Antigas
No novo estudo, os autores triaram uma coleção de colas moleculares focadas em cereblon em células humanas e identificaram um composto chamado MRT-5702. Essa pequena molécula provocou a perda rápida de uma proteína chamada G3BP2, que ajuda a gerir RNA e faz parte de grânulos de estresse — agregados associados a câncer, problemas cardíacos e doenças neurodegenerativas. Importante, G3BP2 não apresenta o padrão de degron que o cereblon costuma reconhecer. Experimentos celulares complementares, incluindo leituras sensíveis baseadas em luz da proximidade entre proteínas, confirmaram que o MRT-5702 aproxima cereblon e G3BP2 formando um complexo tripartido que leva à degradação de G3BP2, enquanto poupa sua proteína irmã intimamente relacionada, G3BP1, a menos que seu domínio chave seja trocado.
Imitação como Estratégia de Ligação
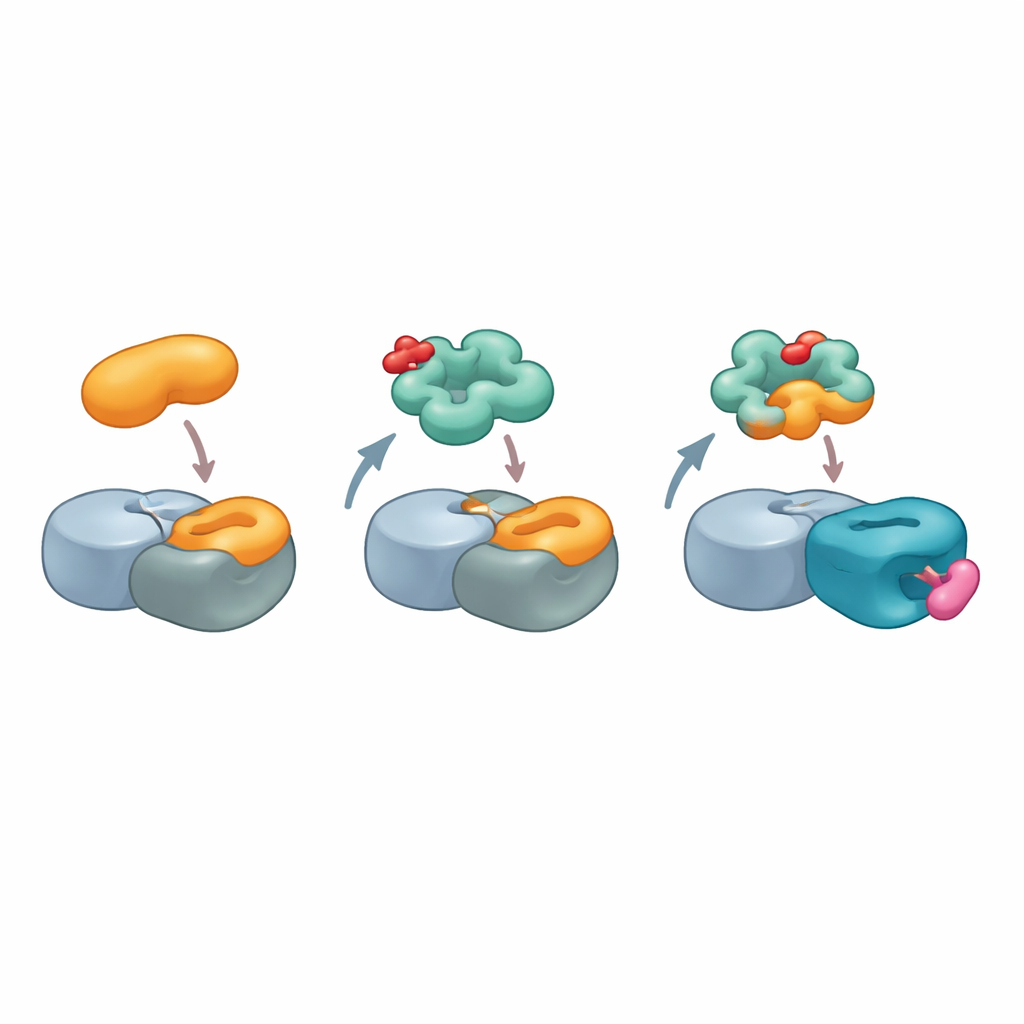
Aprofundando a investigação, os pesquisadores perguntaram como G3BP2 poderia se ligar ao cereblon sem o motivo de reconhecimento padrão. Em vez de procurar semelhanças entre G3BP2 e alvos conhecidos do cereblon, inverteram a pergunta: o cereblon poderia assemelhar-se a um dos parceiros usuais de ligação de G3BP2? Proteínas G3BP costumam interagir com outras moléculas através de um ponto crítico num domínio conhecido como NTF2-like, que normalmente reconhece motivos de sequência curtos. Usando modelos estruturais do parceiro natural de G3BP2, USP10, a equipe escaneou computacionalmente a superfície do cereblon e encontrou uma região em um domínio pouco compreendido, o domínio LON, que imita de forma próxima a forma e a química do motivo de ligação de USP10. Mutar apenas alguns aminoácidos chave nesse trecho, ou no ponto crítico de G3BP2, enfraqueceu o complexo tripartido, sugerindo que o cereblon está efetivamente se fazendo passar por USP10 para se ancorar em G3BP2.
Capturando a Nova Interface em Detalhe Atômico
Para visualizar essa interação incomum, a equipe usou criomicroscopia eletrônica de alta resolução para resolver a estrutura de um complexo contendo cereblon, outro componente central da ligase, MRT-5702 e o domínio NTF2-like de G3BP2. As imagens revelaram que uma alça flexível no domínio LON do cereblon se dobra e remodela para formar quase metade da superfície de contato com G3BP2. A forma ativa espelho do MRT-5702 situa-se no bolso usual de ligação a drogas do cereblon, mas, juntamente com a alça, ajuda a criar uma ampla plataforma que acomod a uma metade do dímero de G3BP2. Notavelmente, esse arranjo quase não usa o sítio canônico do cereblon que lida com alvos anteriores de cola, mostrando que o cereblon pode engajar regiões muito diferentes de sua superfície dependendo da cola e da proteína envolvida. Ao mesmo tempo, a metade não ocupada do dímero de G3BP2 permanece disponível para se ligar a outros parceiros, oferecendo uma via plausível para degradação “colateral” de proteínas que por acaso estejam associadas.
Impressões de Cola para o Design de Fármacos Futuro
Em conjunto, os achados retratam o cereblon como um casamenteiro muito mais versátil do que se pensava. Em vez de exigir que alvos tenham um único tipo de degron, o cereblon pode, quando armado com a cola molecular certa, moldar uma superfície composta que imita contatos naturais proteína–proteína em outras partes da célula. Os autores propõem que tais superfícies combinadas de proteína e cola, que chamam de «glueprints» (impressões de cola), poderiam ser mapeadas e desenhadas para imitar pontos críticos de interação existentes em muitas proteínas ligadas a doenças. Para o leitor leigo, a mensagem chave é que os desenvolvedores de fármacos podem não precisar descobrir bolsões de ligação totalmente novos em proteínas problemáticas; em vez disso, podem ensinar a própria maquinaria de reciclagem da célula a reconhecer essas proteínas copiando de forma inteligente as formas de seus parceiros usuais, ampliando muito o cardápio de alvos que podem ser removidos de forma segura e seletiva.
Citação: Annunziato, S., Quan, C., Donckele, E.J. et al. Cereblon induces G3BP2 neosubstrate degradation using molecular surface mimicry. Nat Struct Mol Biol 33, 479–487 (2026). https://doi.org/10.1038/s41594-025-01738-8
Palavras-chave: degradadores tipo cola molecular, cereblon, degradação proteica direcionada, G3BP2, interações proteína–proteína