Clear Sky Science · pt
Indicadores multicolor de nova geração para imagem in vivo de norepinefrina
Vendo um Mensageiro Oculto do Cérebro
A norepinefrina é uma substância química no cérebro que, de forma silenciosa, molda como despertamos, prestamos atenção, formamos memórias e reagimos ao estresse. Até recentemente, os cientistas só podiam vislumbrar sua atividade com ferramentas lentas ou imprecisas. Este artigo apresenta um novo par de marcadores fluorescentes que permite aos pesquisadores observar o fluxo de norepinefrina no cérebro vivo, em tempo real e com grande resolução. Esses avanços podem aprofundar nossa compreensão do sono, ansiedade, aprendizagem e doenças neurodegenerativas.
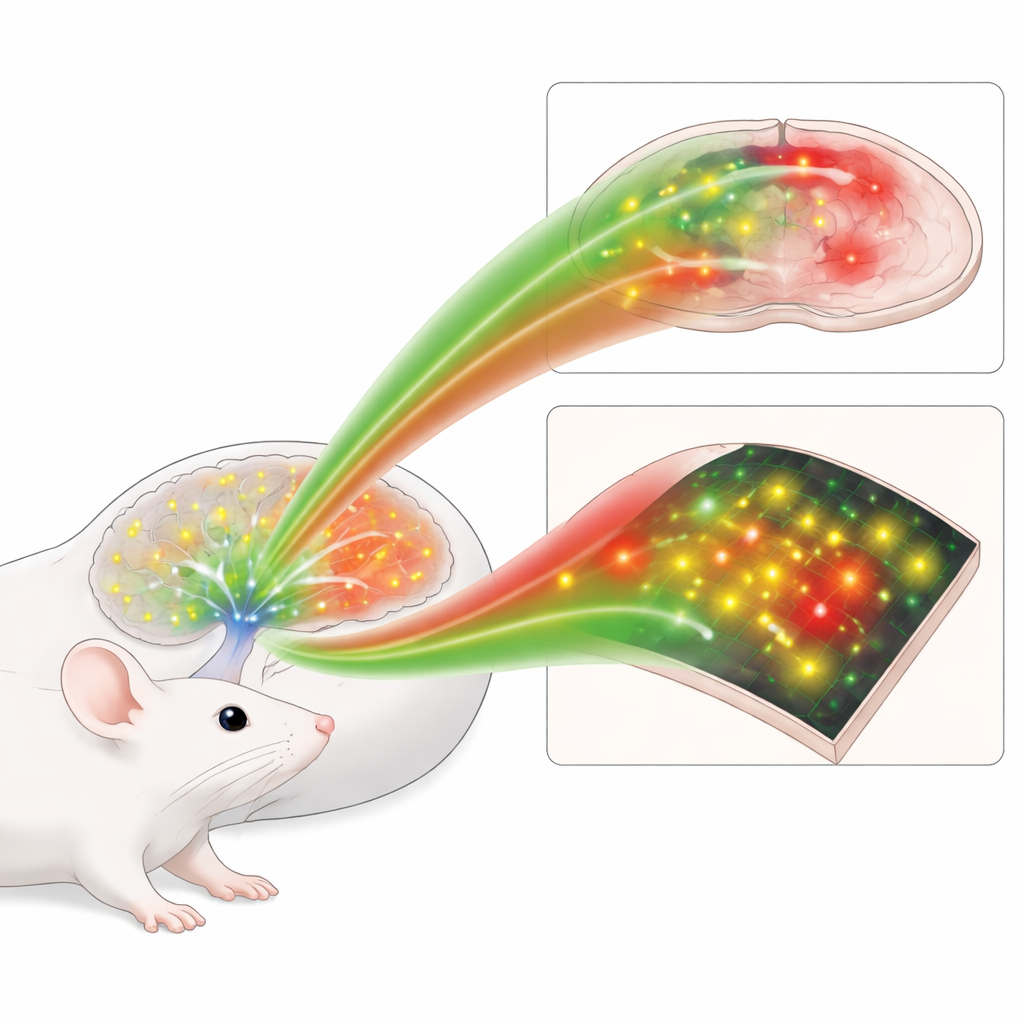
Por que Rastrear Esse Sinal é Tão Difícil
A norepinefrina é liberada por um pequeno grupo de células do tronco encefálico que enviam fibras por todo o cérebro, alterando o comportamento dos circuitos em vez de simplesmente ligá-los ou desligá-los. Métodos clássicos de medição, como minúsculos sensores químicos ou células implantadas que respondem à norepinefrina, ou borram eventos ao longo de muitos segundos ou não a distinguem claramente de moléculas relacionadas. Uma estratégia mais recente usa receptores modificados na superfície celular que brilham quando se ligam à norepinefrina, permitindo leitura óptica. Mas as versões de primeira geração eram relativamente fracas, especialmente na faixa vermelha do espectro, e não eram flexíveis o bastante para experimentos que precisavam combinar várias cores ao mesmo tempo.
Construindo Sentinelas Verdes e Vermelhas Mais Brilhantes
Os autores desenvolveram indicadores verdes e vermelhos aprimorados, chamados nLightG2 e nLightR2, combinando partes de sensores anteriores de dopamina e norepinefrina e testando sistematicamente dezenas de mutações. Essas mudanças tornaram os sensores muito mais brilhantes na presença de norepinefrina, sem alterar muito o brilho básico. Em culturas celulares, as novas ferramentas mostraram respostas várias vezes maiores à norepinefrina do que versões anteriores, reagiram em dezenas de milissegundos e se recuperaram em menos de um segundo. Também responderam minimamente a outros neurotransmissores, como dopamina, e não ativaram as vias de sinalização internas das próprias células — uma verificação de segurança importante para garantir que sejam observadores e não participantes.
Comprovando Sua Potência em Tecido Cerebral
Em seguida, a equipe introduziu os sensores em fatias de cérebro de camundongo e usou microscopia de dois fótons, que alcança profundidade no tecido, para comparar os desenhos antigos e novos. Quando a norepinefrina foi aplicada ao tecido ou quando fibras locais foram estimuladas eletricamente para liberá-la naturalmente, nLightG2 e nLightR2 produziram flashes muito maiores e mais fáceis de detectar do que sensores anteriores. As ferramentas verde e vermelha tiveram desempenho igualmente rápido, o que significa que a escolha de cor não exige mais um compromisso de velocidade. Essa sensibilidade superior permitiu aos pesquisadores mapear onde a norepinefrina se espalhava no espaço, em vez de apenas saber que ela havia sido liberada em alguma parte do campo visual.
Observando Estados Cerebrais, Medo e Navegação em Ação
A verdadeira promessa dessas ferramentas está em animais vivos. Usando fibras ópticas finíssimas, os autores combinaram o indicador vermelho de norepinefrina com um sensor verde de cálcio que relata a atividade dos neurônios. No centro do sono do cérebro, observaram que explosões de atividade em células produtoras de norepinefrina durante o sono profundo foram seguidas de perto por aumentos locais nos níveis de norepinefrina, evento a evento. Na amígdala, uma região cerebral importante para emoções, o sensor verde de norepinefrina revelou que um tom inofensivo passou a desencadear um aumento sustentado de norepinefrina depois de ser pareado com um choque leve, espelhando o fortalecimento de memórias de medo. No hipocampo, que ajuda a mapear o espaço, o sensor vermelho foi imageado junto com um sensor verde de cálcio em astrócitos enquanto camundongos corriam por um corredor virtual em busca de água. Ali, a atividade de astrócitos perto de um local de recompensa estava fortemente ligada a surtos locais de norepinefrina, sugerindo um diálogo entre esse mensageiro químico e as células de suporte durante experiências recompensadoras.
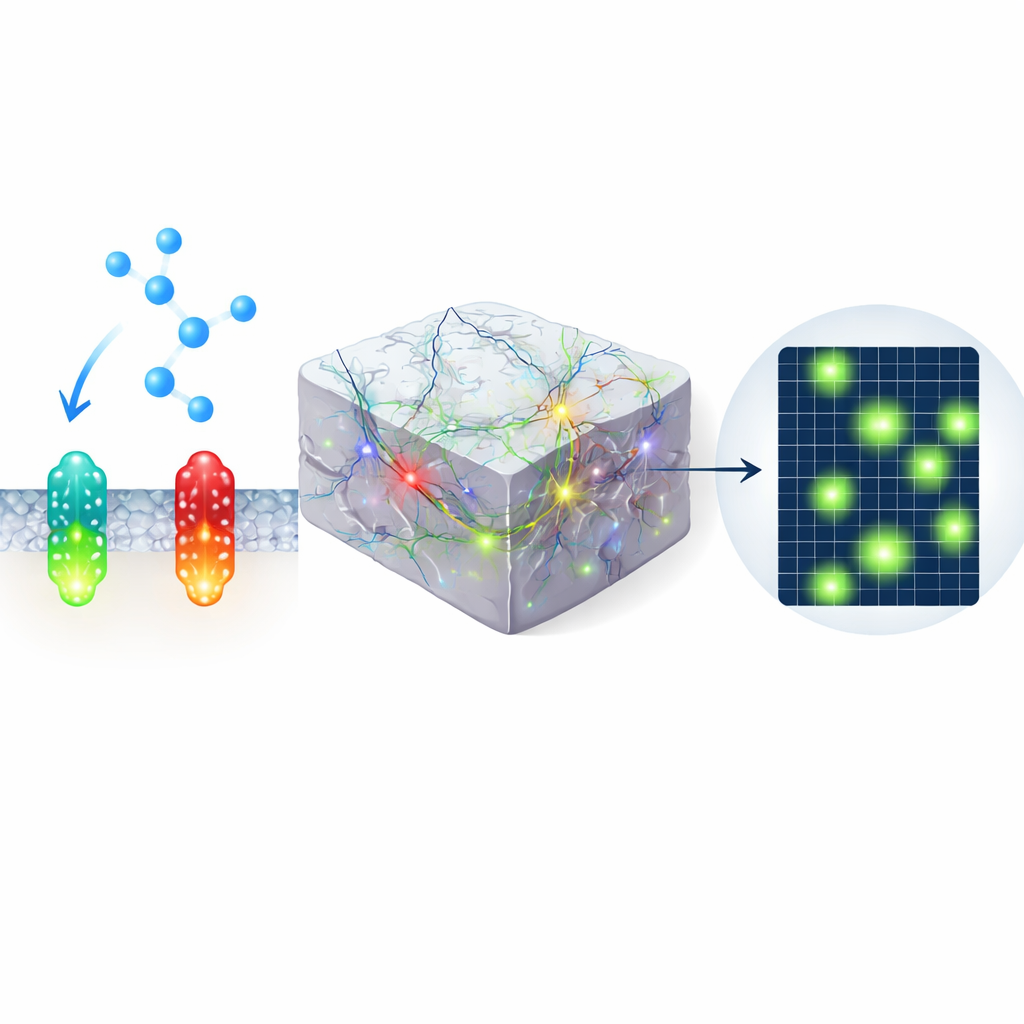
Revelando Pequenos Bolsões de Atividade no Córtex Visual
Em outro conjunto de experimentos, os autores expressaram o sensor verde no córtex visual de camundongos acordados e o imagearam com dois fótons enquanto os animais viam estímulos de aproximação e alternavam entre repouso e corrida. Em vez de um borrão uniforme de sinal, encontraram manchas breves e altamente localizadas de fluorescência aumentada — microdomínios — espalhadas pelo campo visual. Alguns microdomínios respondiam preferencialmente à ameaça visual, outros ao movimento, e muitos surgiam espontaneamente. Esses padrões eram em grande parte invisíveis ao usar um sensor verde mais antigo ou um controle mutado sem ligação, ressaltando a sensibilidade aprimorada do nLightG2 e sugerindo que a norepinefrina modela a atividade cerebral de forma muito mais detalhada do que se imaginava.
O Que Isso Significa para a Pesquisa Cerebral
Em conjunto, esses resultados mostram que nLightG2 e nLightR2 constituem um conjunto poderoso de ferramentas para observar a norepinefrina no cérebro vivo, em escalas que vão de microdomínios individuais a estados comportamentais inteiros. Como existem em cores distintas e podem ser combinados com outros repórteres fluorescentes, os cientistas agora podem rastrear a norepinefrina ao lado de sinais elétricos ou de cálcio em tipos celulares específicos, durante sono, aprendizagem ou estresse. Essa capacidade de ver quando e onde esse importante neuromodulador atua pode, eventualmente, esclarecer como ele sustenta atenção e memória saudáveis e como sua disfunção contribui para condições como ansiedade, depressão e doenças neurodegenerativas.
Citação: Rohner, V.L., Curreli, S., Lamothe-Molina, P.J. et al. Next-generation multicolor indicators for in vivo imaging of norepinephrine. Nat Methods 23, 636–652 (2026). https://doi.org/10.1038/s41592-026-03006-z
Palavras-chave: norepinefrina, neuromodulação, sensores geneticamente codificados, imagem por dois fótons, sono e aprendizagem