Clear Sky Science · pt
Fuga antigênica multimodal a engajadores de células T direcionados a GPRC5D no mieloma múltiplo
Quando o câncer supera a imunoterapia de precisão
Novos medicamentos imunológicos potentes estão transformando o tratamento do mieloma múltiplo, um câncer do sangue que continua incurável para a maioria dos pacientes. Essas terapias funcionam redirecionando as próprias células T do corpo para buscar e destruir células tumorais marcadas por “bandeiras” específicas na superfície. Uma bandeira promissora é a molécula chamada GPRC5D. Ainda assim, como ocorre com muitas terapias direcionadas, os tumores podem evoluir e escapar ao tratamento. Este estudo desvenda, em detalhes incomuns, como as células de mieloma alteram ou ocultam a bandeira GPRC5D para escapar de fármacos que recrutam células T altamente eficazes.
Como os medicamentos inteligentes se prendem às células cancerosas
Anticorpos que engajam células T atuam como casamenteiros moleculares: uma extremidade agarra uma célula T e a outra se liga a uma molécula-alvo na célula cancerosa, aproximando as duas para que a célula T possa matar sua presa. No mieloma múltiplo, GPRC5D é um alvo atraente porque é abundante nas células plasmáticas malignas e raro na maioria dos tecidos normais. Pacientes tratados com um fármaco direcionado a GPRC5D chamado talquetamabe costumam apresentar remissões profundas. Contudo, quase todos acabam recidivando, levantando uma questão crítica: as células cancerosas estão alterando justamente o alvo do qual esses fármacos dependem?
Rastreando a evolução tumoral em tempo real
Os pesquisadores acompanharam 21 pessoas com mieloma de difícil tratamento que receberam talquetamabe. Coletaram amostras de medula óssea antes do tratamento em alguns pacientes e novamente quando o câncer reapareceu, depois usaram várias camadas de análise de DNA, RNA e cromatina para examinar as células tumorais. Essa visão ultra-detalhada revelou que, em cerca de dois terços dos pacientes com recidiva, o câncer havia alterado a GPRC5D de formas que reduziriam ou bloqueariam o efeito do medicamento. De forma marcante, diversos subclones resistentes — ramos geneticamente distintos do tumor — frequentemente coexistiam na mesma pessoa, mostrando que a evolução rumo à fuga pode seguir múltiplos caminhos ao mesmo tempo.
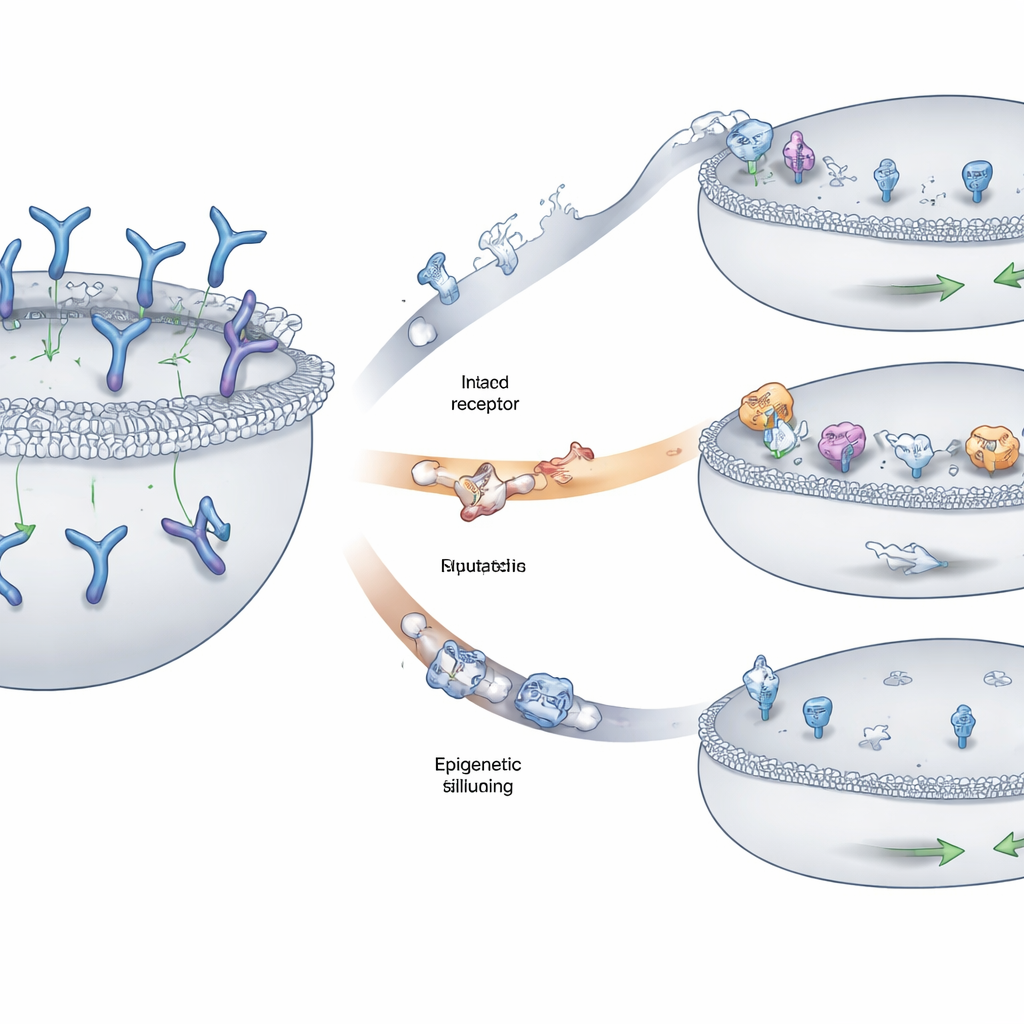
Três maneiras principais pelas quais os tumores escondem o alvo
A equipe identificou três padrões recorrentes pelos quais as células de mieloma evitavam o reconhecimento. Em alguns pacientes, pedaços do cromossomo que carregam o gene GPRC5D foram deletados em ambas as cópias, apagando a bandeira completamente da superfície celular. Em outros, mudanças menores — trocas de uma única letra do DNA ou pequenas inserções e deleções — distorceram regiões-chave da proteína GPRC5D. Muitas dessas alterações comprometeram partes da proteína necessárias para que ela transitasse adequadamente do interior da célula até a membrana externa, fazendo com que a GPRC5D ficasse retida em um compartimento interno em vez de ser exibida onde o medicamento poderia detectá‑la. Uma terceira via envolveu silenciamento epigenético: o DNA ao redor de GPRC5D tornou-se fortemente compactado e quimicamente marcado de modo que o gene era pouco ou quase não transcrito, embora a sequência subjacente permanecesse em grande parte intacta. Células tumorais que usaram essa estratégia produziram pouca ou nenhuma GPRC5D.
Quando a bandeira está presente, mas a trava não se encaixa mais
Nem todas as rotas de fuga removiam a GPRC5D da superfície celular. Em alguns casos, a proteína parecia normal em testes de laboratório padrão, mas já não se encaixava no medicamento como chave na fechadura. A equipe recriou mutações específicas derivadas de pacientes em linhagens celulares de laboratório e testou quão bem diferentes anticorpos direcionados a GPRC5D podiam ligar-se e matar essas células. Uma mutação alterou sutilmente o ponto exato onde o talquetamabe prende o receptor, reduzindo drasticamente a capacidade do fármaco de se ligar e de desencadear a morte celular, mesmo que o receptor ainda fosse visível com colorações rotineiras. Curiosamente, outro fármaco direcionado a GPRC5D que se liga ao receptor em dois locais permaneceu eficaz contra vários desses mutantes, destacando como o desenho do medicamento — por exemplo, o uso de ligação multivalente ou a múltiplos epítopos — pode influenciar se clonas resistentes sobrevivem.
Além do alvo: outros limites ao ataque imune
Embora a maioria das recidivas mostrasse alguma forma de perda ou alteração da GPRC5D, uma minoria de pacientes recidivou sem mudanças óbvias no próprio alvo. Nesses casos, o problema pareceu residir nas células T: elas estavam com menor vigor e menos capazes de matar células cancerosas em testes laboratoriais, sugerindo que a exposição contínua a longo prazo à terapia engajadora pode exaurir o sistema imune. O estudo também revelou que um subtipo genético particular de mieloma (envolvendo uma troca cromossômica chamada t(11;14)) mantém naturalmente o gene GPRC5D em um estado de cromatina mais “fechado”, com expressão basal mais baixa. Isso levanta a possibilidade de que alguns pacientes possam ser predispostos a respostas pobres porque seus tumores já começam com níveis atenuados da bandeira alvo.
O que isso significa para pacientes e tratamentos futuros
Para pacientes e clínicos, este trabalho explica por que mesmo terapias altamente potentes direcionadas a GPRC5D ainda não são curas: as células de mieloma podem deletar, reorganizar, desviar ou desligar a própria bandeira da qual esses fármacos dependem, e frequentemente o fazem de várias maneiras ao mesmo tempo. As descobertas sugerem que monitorar o DNA tumoral, em vez de apenas medir níveis de proteína, será importante para detectar mutações de escape emergentes que testes padrão podem perder. Elas também apontam para estratégias de próxima geração — como fármacos que se liguem à GPRC5D com maior afinidade em múltiplos pontos, combinações que atinjam mais de um alvo ao mesmo tempo, ou agentes que reativem genes silenciados — para se manter à frente da evolução tumoral. Em essência, este estudo mapeia as rotas de fuga usadas pelo mieloma para que futuras terapias possam ser desenhadas para bloqueá‑las, mantendo os tratamentos baseados em células T eficazes por mais tempo.
Citação: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Palavras-chave: mieloma múltiplo, engajadores de células T, GPRC5D, fuga antigênica, imunoterapia contra o câncer