Clear Sky Science · pt
Linavonkibart e pembrolizumabe em tumores sólidos avançados resistentes à bloqueio de ponto de controle imune: um estudo de fase 1
Por que os cânceres teimosos importam para todos nós
Os medicamentos de imunoterapia que “tiram o freio” do sistema imunológico mudaram o tratamento de muitos cânceres, mas a maioria dos pacientes ou nunca se beneficia ou eventualmente volta a apresentar crescimento tumoral. Este estudo testa um novo anticorpo terapêutico, linavonkibart, projetado para desabilitar um escudo poderoso que os tumores usam para se esconder do ataque imunológico, e o combina com uma imunoterapia existente, o pembrolizumabe. Os resultados oferecem um vislumbre inicial de que, mesmo em pacientes cujos cânceres já haviam parado de responder aos fármacos de checkpoint, pode ser possível restaurar o controle imunológico mantendo os efeitos colaterais sob controle.
Um escudo oculto em torno dos tumores
Muitos medicamentos modernos de imunoterapia funcionam bloqueando as chamadas moléculas de checkpoint, como PD‑1, que normalmente contêm as células T. Quando esses freios são liberados, as células imunes podem atacar o câncer de forma mais vigorosa. Mas os tumores frequentemente se adaptam construindo um entorno hostil que impede a entrada das células T assassinas ou as enfraquece quando chegam. Um arquiteto-chave dessa bolha protetora é uma proteína de sinalização chamada TGFβ1, produzida tanto pelas células cancerosas quanto pelas células de suporte próximas. Esforços anteriores para bloquear toda a família TGFβ mostraram promessa, mas esbarraram em problemas graves cardíacos e de sangramento, porque outros membros da família são importantes para tecidos saudáveis. Linavonkibart foi projetado para contornar esse problema ao neutralizar seletivamente apenas a forma latente e inativa de TGFβ1 antes de ser ativada, deixando intocados os moléculas intimamente relacionadas que o corpo precisa.
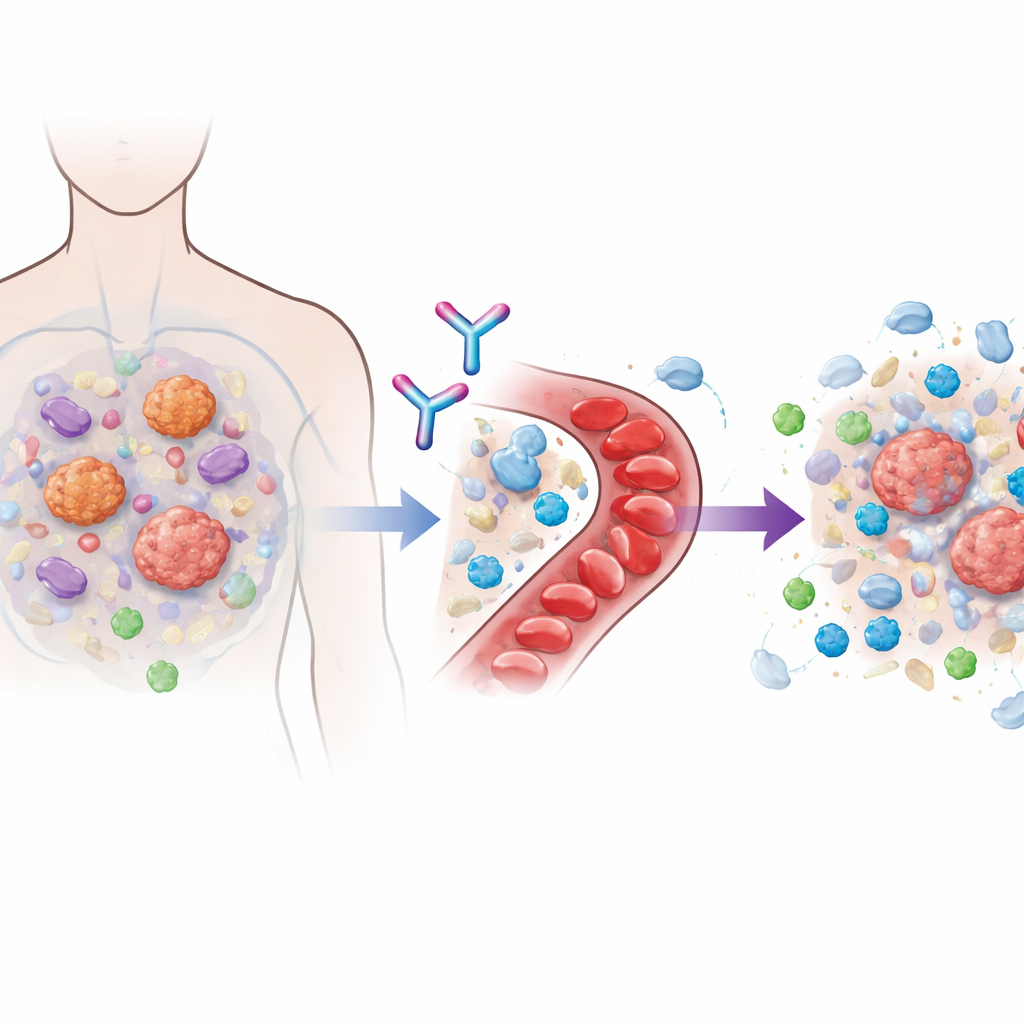
Desenhando um teste humano inicial com cautela
O ensaio DRAGON foi um estudo multicêntrico de fase 1 conduzido em 22 hospitais nos Estados Unidos e na Coreia do Sul. Inscreveu 112 adultos com tumores sólidos avançados, todos com opções terapêuticas limitadas. Na primeira parte do estudo, linavonkibart foi administrado sozinho em doses crescentes a pequenos grupos de pacientes, ou combinado com o medicamento baseado em PD‑1 que já haviam usado. Essa abordagem gradual foi usada para mapear a segurança, como o fármaco se distribui e persiste no sangue, e para escolher uma dose para testes mais amplos. Na segunda parte, 78 pacientes cujos cânceres já haviam resistido a pelo menos um curso de imunoterapia com PD‑1 receberam uma dose fixa de linavonkibart juntamente com pembrolizumabe. Esses pacientes tinham cânceres de difícil tratamento, incluindo carcinoma de células claras do rim, melanoma, câncer de cabeça e pescoço, câncer urotelial (bexiga) e câncer de pulmão, e a maioria havia passado por vários tratamentos prévios.
Segurança em primeiro lugar: o que aconteceu com os pacientes
O objetivo principal deste estudo de fase inicial foi a segurança, e linavonkibart teve um desempenho encorajador nesse aspecto. Em todos os níveis de dose, não foi atingida uma dose máxima tolerada, e não foram observados efeitos adversos limitantes de dose ou fatais atribuíveis ao fármaco. Quando linavonkibart foi combinado com pembrolizumabe na dose de fase 2, cerca de três quartos dos pacientes apresentaram algum efeito adverso relacionado ao tratamento, semelhante ao que frequentemente se observa com a imunoterapia isoladamente. Erupções cutâneas e coceira foram os problemas adicionais mais frequentes, e um pequeno número de pacientes desenvolveu inflamação mais séria da pele ou dos pulmões. Importante, a perigosa reação imune exagerada chamada síndrome de liberação de citocinas, que pode ocorrer com alguns anticorpos terapêuticos, não foi observada, e o padrão geral de segurança assemelhou‑se em grande parte ao do pembrolizumabe sozinho.
Indícios de que o sistema imunológico pode ser reativado
Embora este não tenha sido um grande ensaio definitivo de eficácia, vários sinais sugeriram que bloquear TGFβ1 poderia ajudar a reacender respostas ao bloqueio de PD‑1. Na fase de expansão, a combinação linavonkibart–pembrolizumabe reduziu tumores mensuráveis em uma fração notável de pacientes que anteriormente haviam parado de se beneficiar dos fármacos anti‑PD‑1. As taxas de resposta confirmadas foram de 20% no carcinoma de células claras do rim, 18,2% no melanoma e pouco mais de 9% nos cânceres de cabeça e pescoço e urotelial, com um paciente com câncer renal alcançando desaparecimento completo da doença visível. Muitas dessas respostas duraram vários meses, e os pacientes que responderam permaneceram geralmente na combinação por muito mais tempo do que haviam permanecido na terapia prévia com PD‑1. Biópsias feitas antes e depois do tratamento ofereceram uma explicação biológica: os tumores mostraram maior infiltração de células T CD8 “assassinas”, níveis mais altos de células T ativadas, menos células T reguladoras e células mieloides supressoras, e uma mudança geral em direção a um microambiente mais inflamado e pronto para o ataque.
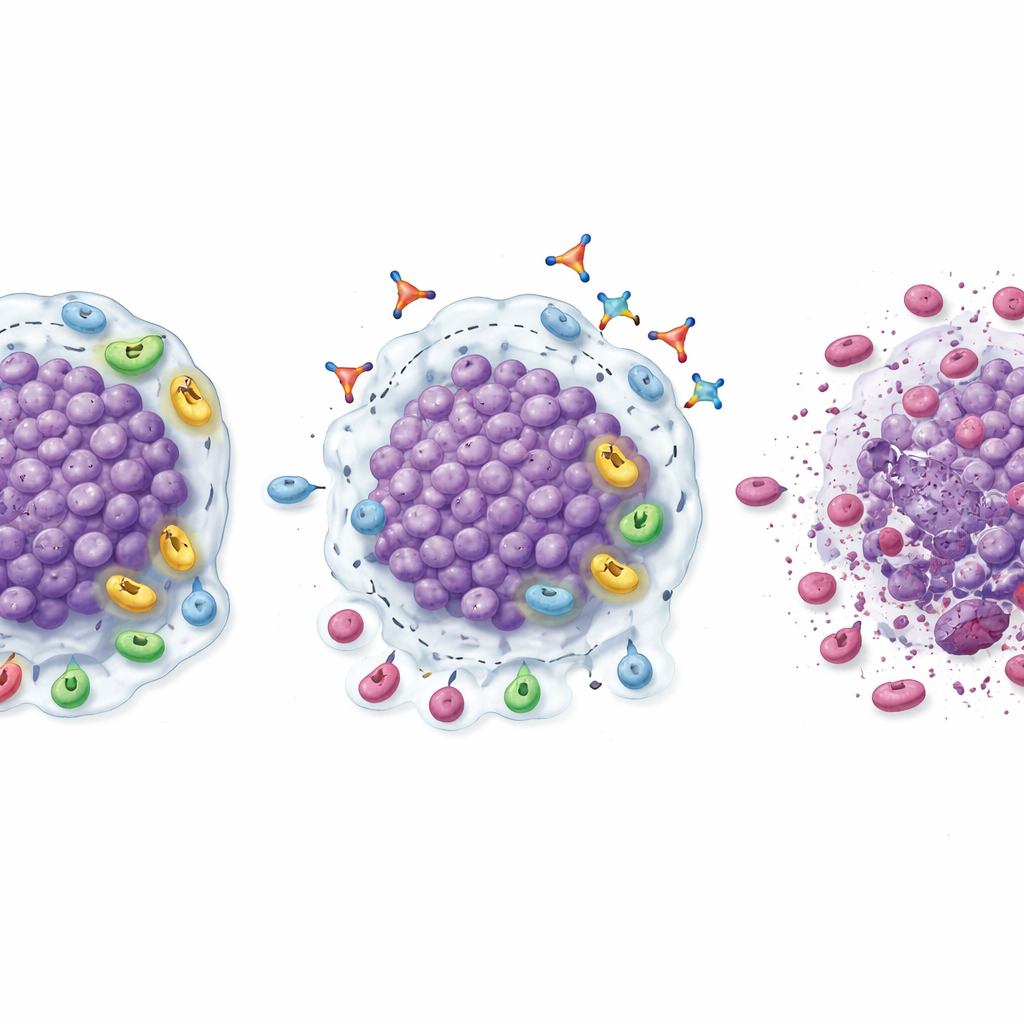
Encontrando quem pode se beneficiar mais
Os pesquisadores também exploraram quais pacientes poderiam ter maior probabilidade de responder. No carcinoma de células claras do rim, tumores que já continham muitas células T CD8 na linha de base — mas que também eram ricos em células T reguladoras e expressavam altos níveis de TGFβ1 — foram mais propensos a diminuir com a terapia combinada. Nesses pacientes, as taxas de resposta e a sobrevida livre de progressão foram substancialmente maiores do que no grupo renal mais amplo. Esse padrão sugere um “ponto ideal”: tumores que têm muitos soldados imunes presentes, mas estão contidos pela supressão mediada por TGFβ1, podem ser candidatos ideais para linavonkibart mais bloqueio de PD‑1. Se validado em estudos maiores, testes simples de tecido para esses marcadores poderiam ajudar os médicos a selecionar os pacientes com maior probabilidade de se beneficiar.
O que este trabalho significa para o futuro
Para pessoas com cânceres avançados que já resistiram à imunoterapia, a perspectiva de reenergizar o próprio sistema imunológico sem acrescentar toxicidade grave é atraente. Este primeiro ensaio em humanos fornece evidência inicial de que desabilitar seletivamente o escudo TGFβ1 com linavonkibart pode ser feito com segurança e pode restaurar controle tumoral significativo quando associado a um inibidor de PD‑1, particularmente em certos cânceres renais. Embora o estudo tenha sido pequeno e não randomizado, seu histórico de segurança, as leituras biológicas e as respostas duráveis juntos constroem um forte argumento para ensaios maiores de fase 2. Se estudos futuros confirmarem esses achados, essa abordagem poderia ampliar o grupo de pacientes que podem se beneficiar da imunoterapia, transformando alguns cânceres atualmente teimosos em tumores novamente vulneráveis às defesas do próprio corpo.
Citação: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
Palavras-chave: imunoterapia contra o câncer, inibição de TGFβ1, resistência a pontos de controle imune, carcinoma de células claras do rim, microambiente tumoral