Clear Sky Science · pt
Paisagem interpretável da inflamação em células imunes circulantes
Por que a inflamação no sangue importa para você
A inflamação está no cerne de muitas doenças, desde artrite e asma até COVID-19 e câncer. Ainda assim, médicos têm dificuldade em interpretar os sinais inflamatórios do corpo de forma que expliquem claramente o que está dando errado e qual tratamento funcionará melhor. Este estudo constrói um enorme “mapa” das células imunes circulantes no sangue e mostra como essas células podem atuar como biomarcadores vivos e facilmente amostrados para classificar uma ampla gama de doenças inflamatórias.
Construindo um mapa gigante de células imunes
Para traçar essa paisagem, os pesquisadores analisaram mais de 6,5 milhões de células imunes coletadas do sangue de 1.047 pessoas. Esses voluntários abrangeram 19 condições, incluindo doenças autoimunes como lúpus e artrite reumatoide, doenças pulmonares crônicas como asma e DPOC, infecções como COVID-19 e HIV, e diversos cânceres, além de doadores saudáveis. Usando sequenciamento de RNA de célula única, eles mediram quais genes estavam ativados em cada célula individual e então aplicaram métodos estatísticos avançados para corrigir diferenças técnicas entre estudos e agrupar as células em 64 estados distintos. Este “Atlas da Inflamação” captura tanto atores conhecidos — como células T, células B e monócitos — quanto subtipos mais especializados que mudam conforme a doença.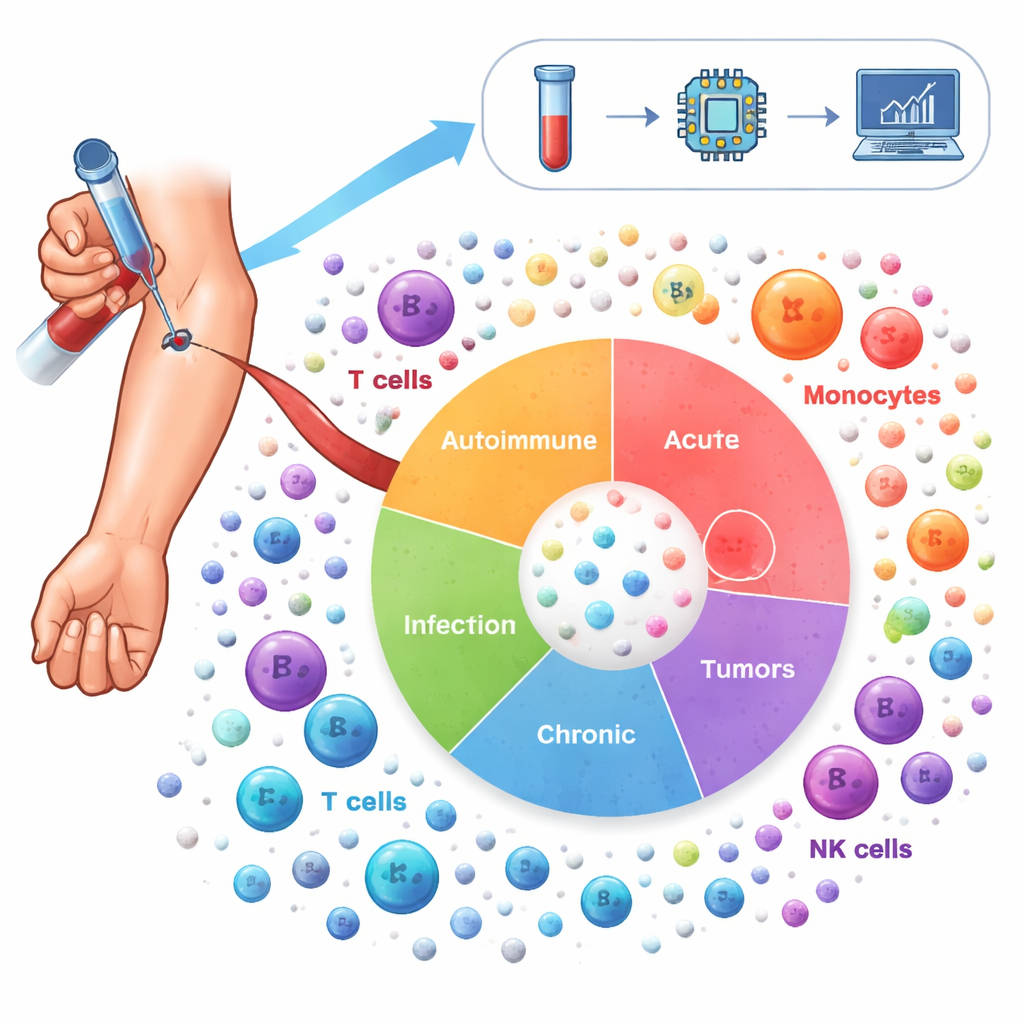
Lendo as assinaturas inflamatórias do corpo
A equipe em seguida focou em genes que controlam como as células imunes se ativam, se movimentam pelo corpo, apresentam antígenos e respondem a moléculas sinalizadoras como interferons e fator de necrose tumoral. Agruparam esses genes em 21 “assinaturas” biológicas e as refinaram para cada tipo celular principal. Ao comparar pacientes com doadores saudáveis, puderam ver quais assinaturas estavam aumentadas ou diminuídas em diferentes doenças. Por exemplo, muitas doenças inflamatórias mediadas pelo sistema imune mostraram maior atividade de moléculas de adesão e da maquinaria de apresentação de antígenos, enquanto respostas a interferons estavam deprimidas na maioria dos tipos celulares, mas aumentadas em certos linfócitos T CD8. Infecções virais como gripe e COVID-19 reforçaram programas induzidos por interferon, ao passo que infecções crônicas como HIV e hepatite B os enfraqueceram.
Aproximando-se de genes-chave e interruptores de controle
Como assinaturas amplas ainda ocultam detalhes importantes, os pesquisadores aprofundaram-se em genes individuais e seus reguladores. Em células T CD8 não naïves, encontraram dois genes, FGFBP2 e GZMB, especialmente ativos em subtipos específicos de memória efetora, particularmente na colite ulcerativa. Esses genes foram associados a danos em superfícies epiteliais, e seu forte sinal no sangue sugere que essas células agressivas já estão preparadas antes de entrarem nos tecidos. Uma análise separada de redes regulatórias de genes destacou dois fatores de transcrição, STAT1 e SP1, como controladores centrais dos programas induzidos por interferon. Seus padrões de atividade diferiram entre doenças e tipos celulares — por exemplo, comportamento oposto em monócitos versus células T CD8 no lúpus, e variações entre fases de surto e não‑surto — indicando como as mesmas vias podem ser protetoras em um contexto e prejudiciais em outro.
Treinando máquinas para identificar doenças a partir de células sanguíneas
Para transformar este atlas em uma ferramenta prática, a equipe aplicou aprendizado de máquina interpretável. Treinaram modelos de árvores de decisão com impulso por gradiente separadamente para cada tipo celular principal, pedindo aos algoritmos que rotulassem células individuais com a doença correta com base em sua expressão gênica. Esses modelos alcançaram alta acurácia quando testados em amostras reservadas, especialmente após a correção por diferenças técnicas. Usando SHAP, um método que explica quais genes conduzem cada decisão, os pesquisadores puderam identificar biomarcadores candidatos. Um exemplo é CYBA em monócitos, cujos níveis ajudaram a distinguir doenças de pele como psoríase de inflamação intestinal na doença de Crohn e na colite ulcerativa. Outro é IFITM1 em certos linfócitos T e células linfoides inatas, separando asma de DPOC e sugerindo padrões diferentes de defesa antiviral crônica.
Rumo a uma bússola diagnóstica baseada no sangue
Finalmente, os autores investigaram se pacientes inteiros — e não apenas células individuais — poderiam ser classificados a partir de seus perfis imunes circulantes. Projetaram os dados de cada célula em um espaço de “incorporação” comprimido, calcularam a média dessas incorporações por tipo celular para cada paciente e treinaram classificadores para prever a doença. Quando novos pacientes se assemelhavam aos do conjunto de treinamento, o desempenho foi excelente. Mas quando amostras vieram de estudos completamente independentes usando métodos laboratoriais diferentes, a acurácia caiu fortemente, revelando quão sensíveis essas ferramentas são à variabilidade técnica. Um conjunto de dados mais controlado e “centralizado”, gerado em um único centro com uma química de sequenciamento única, restaurou grande parte do desempenho, apontando para a necessidade de protocolos padronizados ou conjuntos de treinamento muito grandes e diversos.
O que isso significa para diagnóstico e tratamento futuros
Para o público leigo, a mensagem principal é que suas células imunes circulantes carregam uma rica impressão digital de como seu corpo está inflamado. Ao ler essas impressões célula a célula, este trabalho mostra que é possível distinguir entre muitas doenças, descobrir genes que podem impulsionar sintomas específicos e começar a construir testes sanguíneos universais que classifiquem doenças inflamatórias. O estudo ainda não é um teste clínico pronto — diferenças técnicas entre estudos continuam a limitar a confiabilidade —, mas estabelece a base para futuras ferramentas de “biópsia líquida” que poderiam ajudar médicos a identificar o diagnóstico e o tratamento corretos mais cedo, usando uma simples coleta de sangue.
Citação: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Palavras-chave: inflamação, células imunes, sequenciamento de RNA de célula única, biomarcadores, aprendizado de máquina