Clear Sky Science · pt
Ajustar a dosagem de BACH2 equilibra estamina e função efetora para melhorar a terapia de células T antitumorais
Fazendo com que as células que combatem o câncer durem mais
Muitos dos tratamentos contra o câncer mais promissores atualmente dependem de versões potencializadas das próprias células imunológicas do corpo. Ainda assim, essas células T modificadas frequentemente se esgotam rápido demais dentro dos tumores, limitando sua eficácia. Este estudo explora uma forma de fazer com que as células T antitumorais durem mais sem reduzir seu poder de matar, ajustando cuidadosamente a atividade de uma única molécula reguladora dentro das células.
Por que as células imunes precisam tanto de juventude quanto de força
Nosso sistema imune depende de uma divisão de tarefas. Algumas células T atuam como “sementes” resistentes e semelhantes a células-tronco que vivem muito tempo e podem continuar gerando novos combatentes. Outras se tornam células “soldado” de vida curta, que realizam a maior parte da destruição imediata do tumor, mas se esgotam rapidamente. Uma terapia efetiva contra o câncer precisa de ambos: um reservatório duradouro de sementes e um suprimento constante de soldados. Em infecções crônicas e tumores, porém, muitas células T derivam para um estado exausto e terminal que não consegue mais se multiplicar nem responder bem ao tratamento. Resultados clínicos com terapias de células T existentes mostram que pacientes se saem melhor quando as células infundidas contêm mais do subconjunto semelhante a células-tronco e persistem por mais tempo no organismo.
Um botão molecular para descanso e atividade das células T
Os pesquisadores focaram em uma proteína chamada BACH2, que ajuda a manter as células T em um estado de repouso semelhante à memória. Em respostas imunes naturais, os níveis de BACH2 são altos em células T naïve e semelhantes a células-tronco, e caem conforme as células se tornam assassinas totalmente armadas. Trabalhos anteriores mostraram que BACH2 protege contra a hiperativação e chega a agir como supressor tumoral em células T engenheiradas, tornando-o uma ferramenta atraente, porém delicada: descanso demais pode deixar as células apáticas demais para combater o câncer. Quando a equipe forçou as células T a produzir grandes quantidades de BACH2, foi exatamente isso que aconteceu. As células permaneceram em uma condição quiescente, semelhante a células-tronco, expressaram menos marcadores de ativação, produziram pouco das moléculas tóxicas necessárias para matar células tumorais e controlaram mal os tumores em camundongos.
Encontrando a dose “certa”
Para ver se BACH2 poderia ajudar em vez de atrapalhar a terapia quando ajustado ao nível adequado, os autores construíram vetores genéticos que produzem apenas uma pequena fração da superexpressão habitual — aproximadamente a mesma quantidade de BACH2 encontrada em células T de memória saudáveis. Eles confirmaram essas dosagens marcando a proteína e usando espectrometria de massa para contar suas cópias. Com esse sistema de baixa dose em mãos, eles estimularam repetidamente células T de camundongo em cultura para mimetizar o estresse crônico de um tumor. Tanto a alta quanto a baixa expressão de BACH2 reduziram o surgimento de células terminalmente exaustas e preservaram marcadores associados ao comportamento semelhante a células-tronco. A diferença crucial foi que BACH2 em baixa dose permitiu que as células mantivessem forte produção de citocinas e enzimas-chave, enquanto BACH2 em alta dose suprimiu fortemente essas funções efetoras e até reduziu o tamanho celular, um sinal de ativação deficiente.
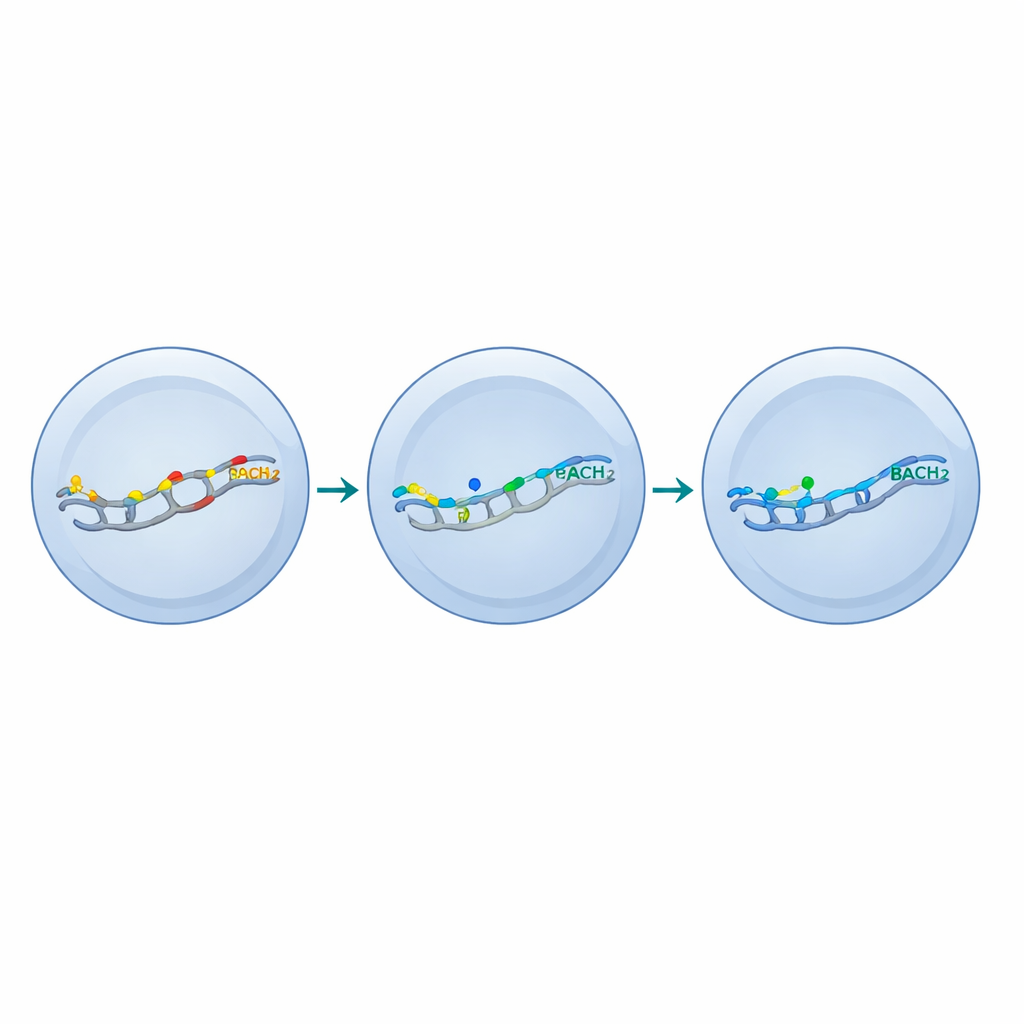
Em nível molecular, a equipe descobriu que BACH2 atua competindo com uma família de proteínas ativadoras conhecidas coletivamente como AP-1 em motivos específicos de DNA. Genes que dependem fortemente de AP-1 carregavam muitos desses motivos e foram especialmente sensíveis a BACH2. BACH2 em alta quantidade quase deslocou totalmente o AP-1 desses sítios, desligando muitos genes efetores. BACH2 em baixa dose reduziu apenas parcialmente a ligação do AP-1, atenuando seletivamente genes que impulsionam a exaustão terminal enquanto poupava grande parte do programa efetor benéfico. Em tumores, células T engenheiradas com BACH2 em baixa dose acumularam-se melhor, mantiveram tanto subconjuntos semelhantes a células-tronco quanto mais diferenciados, e geraram mais células produtoras de citocinas por grama de tumor, levando a um controle marcadamente melhor de melanomas e cânceres colorretais em modelos de camundongo. 
Criando células T híbridas que perduram e atacam
Ao examinar células T que expressavam ou não um marcador de superfície ligado ao comportamento semelhante a células-tronco, os pesquisadores mostraram que BACH2 em baixa dose remodelou as células mais diferenciadas e exaustas para um estado híbrido. Essas células adquiriram características selecionadas de células T semelhantes a células-tronco — como genes associados à longevidade e ao direcionamento tecidual — enquanto mantinham traços centrais de efetoras ativas, incluindo produção vigorosa de citocinas e proliferação. Em outras palavras, em vez de forçar todas as células a um estado silencioso de semente, BACH2 ajustado por dose elevou um patamar de autorrenovação e contenção, especialmente em células que, de outra forma, se consumiriam.
Uma estratégia mais ampla para terapias celulares mais seguras e mais potentes
Para testar se esse conceito se estende além de BACH2, os autores aplicaram o mesmo truque de dosagem a outra proteína que promove quiescência, FOXO1. Mais uma vez, níveis altos aumentaram marcadores semelhantes a células-tronco, mas prejudicaram as funções efetoras, enquanto doses baixas e cuidadosamente ajustadas preservaram tanto a durabilidade quanto a capacidade de matar e melhoraram o controle tumoral em camundongos. Em conjunto, essas descobertas mostram que a quantidade de uma proteína reguladora expressa pode mudar completamente o comportamento de células T engenheiradas. Em vez de depender de circuitos permanentemente hiperativados e potencialmente cancerígenos, os clínicos poderão projetar terapias mais seguras ao ajustar finamente fatores naturais de “repouso e reparo”, de modo que as células T permaneçam mais tempo na luta sem perder sua eficácia.
Citação: Conti, A.G., Evans, A.C., von Linde, T. et al. Fine-tuning BACH2 dosage balances stemness and effector function to enhance antitumor T cell therapy. Nat Immunol 27, 436–451 (2026). https://doi.org/10.1038/s41590-025-02389-z
Palavras-chave: Terapia com células T, imunoterapia contra o câncer, BACH2, quiescência celular, dosagem gênica