Clear Sky Science · pt
Padronização espacial do sinal de TGFβ em fibroblastos fundamenta a resistência ao tratamento na artrite reumatoide
Por que a dor articular persistente importa
Muitas pessoas com artrite reumatoide usam medicamentos modernos que acalmam o sistema imune, mas ainda assim suas articulações permanecem doloridas e rígidas. Este estudo investiga por que alguns pacientes não melhoram mesmo quando a inflamação na articulação parece diminuir. Ao observar de perto onde e como certas células de suporte na articulação ativam programas de cicatrização, os pesquisadores revelam uma forma oculta de dano que pode explicar a dor contínua e apontar para novas estratégias terapêuticas.
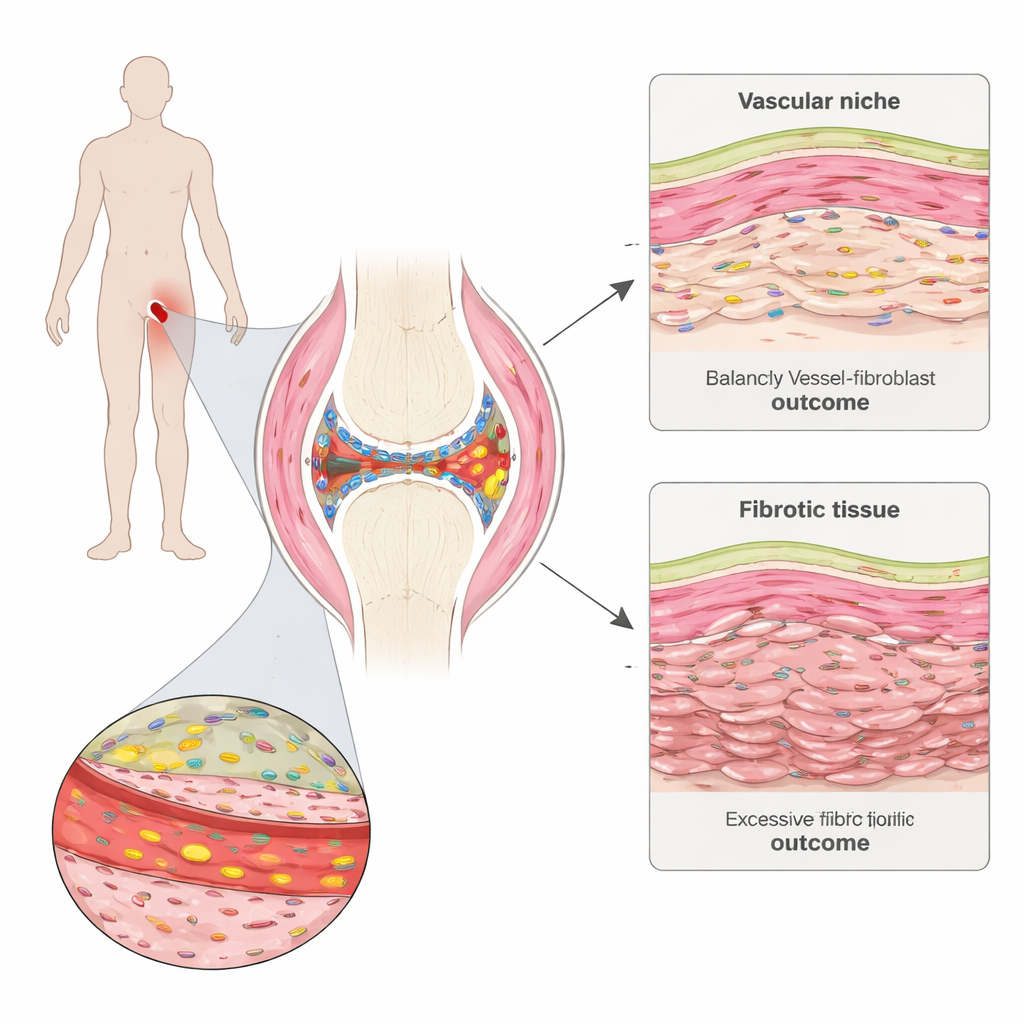
Um olhar mais atento dentro da articulação dolorida
A artrite reumatoide ataca a sinóvia, um tecido delgado que reveste e lubrifica as articulações. A equipe coletou pequenas biópsias sinoviais de pessoas com doença precoce antes do início da terapia e novamente seis meses depois. Usando mapeamento genômico espacial avançado, eles conseguiram ver quais genes estavam ativos em milhares de células individuais preservando a localização dessas células no tecido. Identificaram “vizinhanças” distintas na sinóvia, incluindo aglomerados de células imunes, áreas ricas em gordura, a fina camada interna e regiões repletas de vasos sanguíneos e células estruturais chamadas fibroblastos.
Células formadoras de cicatriz e resistência ao tratamento
Ao comparar pacientes que depois alcançaram remissão com aqueles que não alcançaram, os pesquisadores encontraram um padrão marcante: antes do tratamento, os pacientes sem remissão já apresentavam sinais mais fortes de cicatrização tecidual, ou fibrose. Um programa específico de fibroblastos, marcado por alta produção de uma proteína da matriz extracelular chamada COMP, estava expandido nesses pacientes. Esses fibroblastos ricos em COMP compartilhavam características com células formadoras de cicatriz observadas em fibrose pulmonar e cutânea e estavam mais fortemente associados a resposta ruim ao tratamento. Ao longo do tempo, regiões dominadas por essas células tendiam a ficar densamente preenchidas por tecido conjuntivo, porém relativamente pobres em células, sugerindo que depositavam matriz rígida que pode persistir mesmo após a inflamação diminuir.
Vasos sanguíneos como condutores ocultos
Os fibroblastos fibrogênicos não estavam espalhados ao acaso. Eles se agrupavam ao redor de vasos sanguíneos, formando zonas perivasculares em camadas. A camada mais interna, abraçando a parede do vaso, expressava genes diferentes da camada externa. A equipe mostrou que as células que revestem os vasos sanguíneos enviam sinais Notch para fibroblastos próximos, que por sua vez modulam como esses fibroblastos respondem a uma família de sinais pró‑cicatriz conhecidos como TGF‑beta. Perto do vaso, a sinalização Notch estimula os fibroblastos a produzir TGF‑beta, mas simultaneamente reduz o número de receptores de TGF‑beta em sua superfície, mantendo sua sensibilidade sob controle. Mais afastado, onde a influência Notch desaparece, os fibroblastos apresentam mais receptores e tornam‑se altamente responsivos, convertendo‑se em células ricas em COMP que promovem a fibrose.
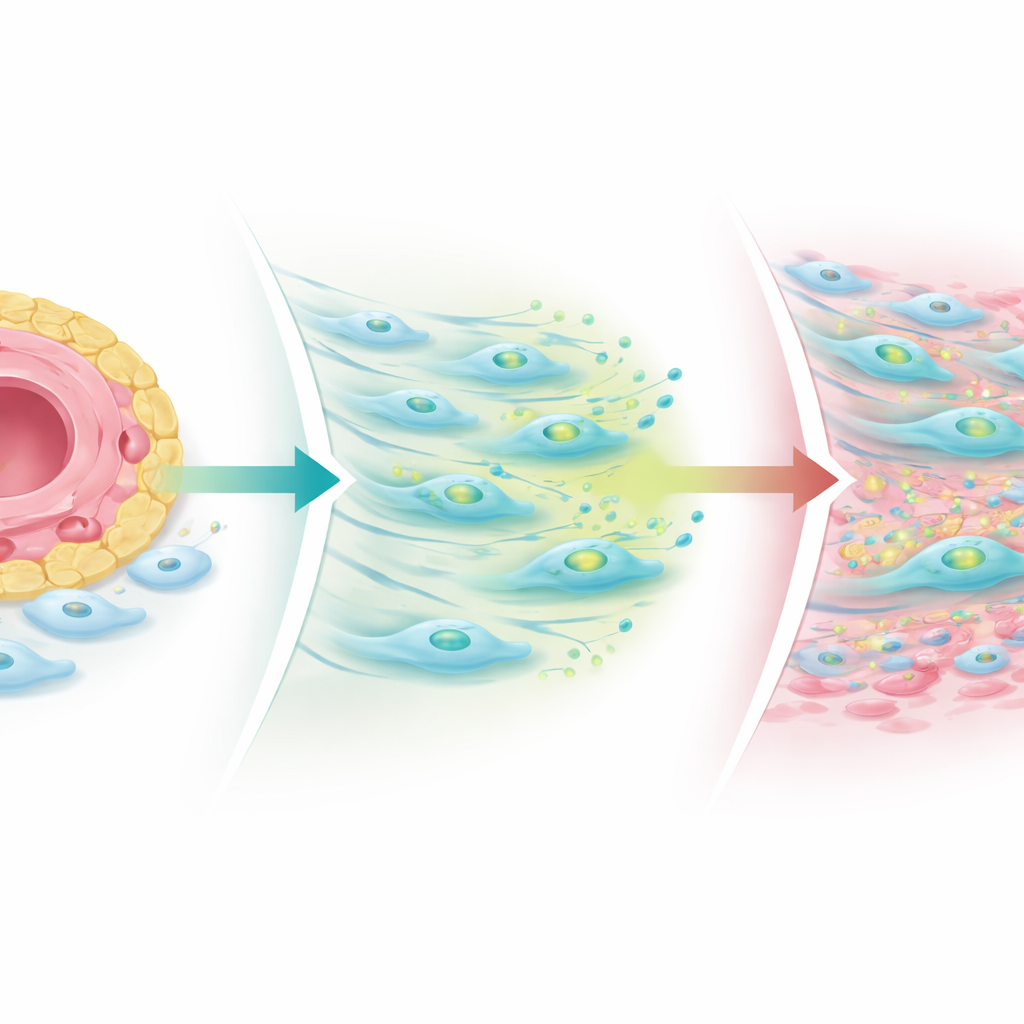
O que acontece quando o equilíbrio se rompe
Os pesquisadores construíram modelos articulares simplificados em placas de laboratório e organoides tridimensionais derivados de tecido de pacientes para investigar esse mecanismo. Quando reforçaram sinais Notch das células endoteliais, os fibroblastos aumentaram a produção de TGF‑beta, mas reduziram os níveis de receptores, limitando a formação de cicatriz. Quando bloquearam Notch ou perturbavam seu padrão estável, os fibroblastos recuperaram receptores de TGF‑beta — especialmente um co‑receptor chamado receptor III de TGF‑beta — e as células fibrogênicas positivas para COMP se expandiram afastando‑se dos vasos. Em biópsias de pacientes coletadas após o tratamento, os aglomerados de células imunes diminuíram em quase todos, mas nichos fibrogênicos, particularmente regiões ricas em COMP, frequentemente aumentaram, especialmente naqueles cuja dor articular persistiu. Isso sugere que os medicamentos anti‑inflamatórios padrão podem extinguir o “fogo” imune enquanto deixam para trás ou até revelam um processo de cicatrização que mantém as articulações rígidas e dolorosas.
Novas formas de acalmar articulações teimosas
Por fim, a equipe testou se interromper esse circuito fibrogênico poderia ser útil terapeuticamente. Em organoides derivados de pacientes, fármacos que inibem Notch ou bloqueiam a sinalização TGF‑beta reduziram a produção de COMP, outras proteínas relacionadas à cicatriz e colágenos-chave, e reprogramaram a atividade gênica nas zonas perivasculares. Para um observador leigo, a mensagem é que nem todo o dano na artrite reumatoide vem da inflamação visível: parte dele está “programado” nas células de suporte e nos vasos sanguíneos da articulação. Ao visar a conversa Notch–TGF‑beta que controla como os fibroblastos depositam tecido cicatricial, tratamentos futuros podem prevenir ou reverter uma forma fibrosa e persistente da doença que resiste aos medicamentos atuais focados no sistema imune.
Citação: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Palavras-chave: artrite reumatoide, fibrose, fibroblastos, sinalização TGF‑beta, via Notch