Clear Sky Science · pt
Engenharia de xilosiltransferase para manipular proteoglicanos em células de mamíferos
Por que as capas celulares importam
Cada célula do nosso corpo usa um “revestimento” molecular que a ajuda a comunicar‑se com vizinhas e a perceber o ambiente. Uma parte importante desse revestimento é formada por proteoglicanos—proteínas decoradas com longas cadeias de açúcares que funcionam como pequenas antenas para fatores de crescimento, sinais imunológicos e pistas estruturais. Quando essa decoração de açúcares falha, o desenvolvimento pode ser prejudicado e tecidos como osso e músculo podem ser gravemente afetados. Ainda assim, os cientistas têm tido dificuldade em mapear exatamente quais proteínas carregam essas cadeias e como componentes individuais da camada influenciam o comportamento celular. Este estudo apresenta uma estratégia química precisa para marcar e reconstruir essas cadeias de açúcar em células de mamíferos vivas, abrindo um caminho para ler e reescrever a informação codificada em suas superfícies. 
Redirecionando o primeiro passo da fixação de açúcares
A construção dos proteoglicanos começa quando uma família especial de enzimas, as xilosiltransferases XT1 e XT2, instala o primeiro açúcar numa proteína, marcando o ponto onde uma longa cadeia irá se formar. Como ambas as enzimas podem executar esse mesmo primeiro passo, tem sido difícil determinar em quais proteínas cada uma age dentro das células. Os autores usaram um desenho “saliente‑e‑furo” — comum na biologia química moderna — para resolver isso. Eles remodelaram ligeiramente o sítio ativo de XT1, criando espaço extra (o “furo”), e introduziram um bloco de açúcar correspondente, um pouco mais volumoso, o 6AzGlc (o “saliente”). A XT1 modificada agora pode usar esse açúcar alterado, enquanto a enzima natural não consegue, permitindo aos pesquisadores marcar apenas as proteínas modificadas pela enzima redesenhada.
Contrabandeando um açúcar projetado para dentro das células
Para fazer essa abordagem funcionar em células vivas, a equipe precisou entregar o açúcar com saliência em uma forma reconhecível pelo metabolismo celular. Em vez de depender das vias normais de captação de açúcares — que não processam bem análogos de xilose — eles construíram uma versão protegida do 6AzGlc carregando um grupo fosfato oculto. Uma vez dentro do citosol, enzimas celulares desmascaram esse grupo e convertem a molécula em UDP‑6AzGlc, a forma ativada necessária para as xilosiltransferases engenheiradas. Cromatografia cuidadosa confirmou que células tratadas com o composto protegido corretamente configurado produziram quantidades substanciais do açúcar projetado ativado, enquanto um controle imagem‑espeelho produziu quase nenhum. 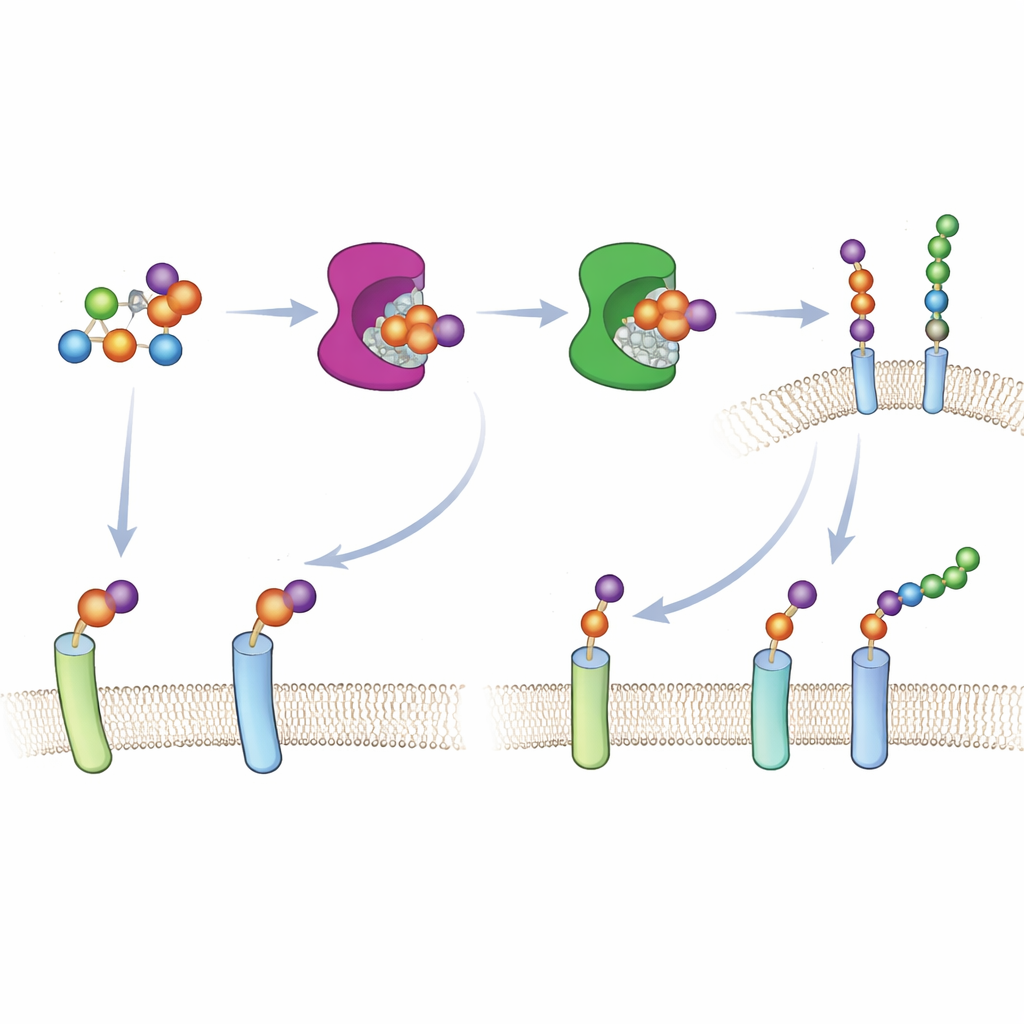
Marcando e identificando os atores ocultos
Com a enzima modificada e o açúcar ativado no lugar, os pesquisadores mostraram que apenas células expressando a XT1 ou XT2 engenheirada incorporaram a etiqueta 6AzGlc em seus proteoglicanos de superfície. O grupo azida no 6AzGlc serve como uma pequena alça química que pode ser “clicada” a corantes fluorescentes ou biotina, permitindo a visualização e o enriquecimento das proteínas marcadas. Espectrometria de massas de amostras enriquecidas revelou uma coleção rica de proteoglicanos conhecidos—incluindo decorina, múltiplos glicopicanos, sindecan‑4, CD44 e versican—confirmando que o sistema marca proteínas genuinamente portadoras de açúcar. Importante, as enzimas engenheiradas preservaram as mesmas preferências de sequência que suas contrapartes naturais, o que significa que a etiqueta química é instalada em sítios de ancoragem autênticos e não em posições artificiais novas.
Construindo proteoglicanos sob medida
Um bônus inesperado da etiqueta 6AzGlc é que, ao contrário do açúcar inicial natural, ela não pode ser estendida em uma cadeia de comprimento total pelas enzimas subsequentes. Isso efetivamente limita a cadeia e simplifica a estrutura molecular que deve ser analisada por espectrometria de massas. Os autores transformaram essa característica em uma ferramenta: depois que XT1 instala o 6AzGlc no sítio de ancoragem natural, eles usam química de clique para acoplar fragmentos sintéticos de heparina, criando “proteoglicanos sob medida” com cadeias de açúcar precisamente definidas. Em células de câncer de mama que carecem de seu próprio sindecan‑1, a restauração com essas versões projetadas recuperou a disseminação normal sobre uma superfície recoberta por proteína, provando que o proteoglicano reconstruído quimicamente pode substituir funcionalmente o natural.
O que isso significa para a biologia e a medicina
Este trabalho fornece um conjunto poderoso de ferramentas para rotular e manipular seletivamente as cadeias de açúcar que controlam como as células se comunicam. Ao separar os papéis de XT1 e XT2 e marcar apenas seus alvos diretos, os pesquisadores podem agora mapear quais proteoglicanos atuam em tecidos e estados de doença específicos. A capacidade de interromper o crescimento natural da cadeia e substituí‑la por açúcares construídos sob medida também permite aos cientistas dissecar quanto da função de um proteoglicano é carregada por seu esqueleto proteico versus sua cobertura de açúcar. A longo prazo, esse nível de engenharia pode ajudar a decodificar a sinalização complexa na superfície celular e inspirar terapias que reparem ou reprogramem revestimentos celulares defeituosos em distúrbios do desenvolvimento, câncer e outras doenças.
Citação: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Palavras-chave: proteoglicanos, glicosaminoglicanos, xilosiltransferase, biologia química, sinalização na superfície celular