Clear Sky Science · pt
Um único sítio alostérico une ativação, modulação e inibição em TRPM5
Como um pequeno porteiro molda paladar e metabolismo
Os alimentos de que gostamos e a forma como nossos corpos processam o açúcar dependem de proteínas “porteiras” microscópicas nas nossas células. Uma dessas porteiras, um canal chamado TRPM5, nos ajuda a sentir sabores doces, amargos e umami e auxilia o pâncreas a liberar insulina. Este estudo revela como uma pequena cavidade no TRPM5 pode agir como um botão de controle mestre, ligando o canal, ajustando sua sensibilidade e até mesmo desligando-o — percepções que podem orientar tratamentos futuros para diabetes, obesidade e transtornos intestinais.
Um canal na encruzilhada do paladar e da glicemia
O TRPM5 está nas membranas de células gustativas na língua, de células produtoras de hormônios no intestino e de células secretoras de insulina no pâncreas. Quando os níveis de cálcio dentro dessas células aumentam, o TRPM5 se abre e permite a passagem de íons carregados positivamente, alterando brevemente a voltagem da célula. Nas papilas gustativas, esse sinal elétrico informa ao cérebro que algo doce, amargo ou umami está na língua. No pâncreas, ajuda a ajustar os pulsos de insulina após uma refeição. Pessoas e animais com função prejudicada de TRPM5 apresentam problemas na liberação de insulina e no controle da glicemia, o que sugere que fármacos que atinjam o TRPM5 podem um dia auxiliar no tratamento de doenças metabólicas. Ainda assim, até recentemente, os pesquisadores não dispunham de ferramentas precisas para ligar ou desligar esse canal.
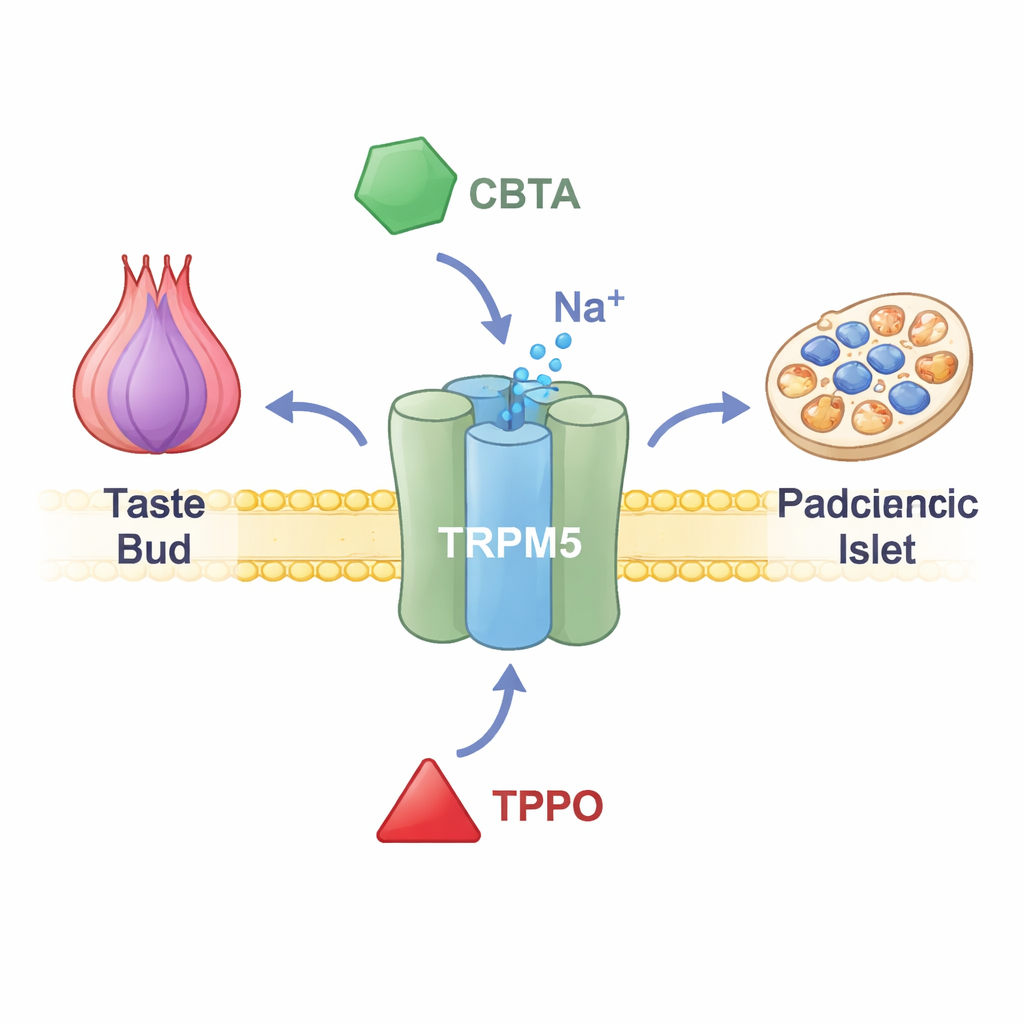
Um novo comutador químico que supercarrega o canal
Os pesquisadores focaram em um composto sintético chamado CBTA, previamente conhecido por estimular o TRPM5, mas pouco compreendido. Usando registros elétricos de células geneticamente modificadas para produzir TRPM5, demonstraram que o CBTA pode abrir o canal mesmo quando o cálcio está quase ausente, provando que ele age como um verdadeiro ativador e não apenas potencializa os efeitos do cálcio. Quando pequenas quantidades de cálcio estão presentes — níveis que normalmente mantêm o TRPM5 inativo — o CBTA e o cálcio atuam em conjunto, gerando correntes muito maiores do que qualquer um sozinho. Isso significa que o CBTA torna o TRPM5 extraordinariamente sensível, de modo que níveis de cálcio próximos ao repouso passam subitamente a ser suficientes para abrir amplamente o canal.
Uma cavidade de controle oculta revelada por crio-EM
Para ver como isso funciona em detalhe atômico, a equipe usou crio-microscopia eletrônica para capturar instantâneos tridimensionais do TRPM5 em diferentes condições. Eles descobriram que o CBTA se acomoda em uma cavidade anteriormente despercebida na parte superior de uma região sensora de voltagem do canal, logo acima de onde o cálcio normalmente se liga. Essa cavidade, formada por um aglomerado de aminoácidos, atua como um sítio de encaixe preciso. Quando os cientistas mutaram blocos construtivos chave que revestem esse bolso, o CBTA não conseguiu mais ativar o TRPM5, embora o cálcio ainda funcionasse, confirmando que essa pequena cavidade é essencial para a ação da droga. Notavelmente, a ligação do CBTA rearranja sutilmente partes próximas da proteína de forma a facilitar que o cálcio ocupe seu local habitual, explicando a sinergia dramática observada nas medidas elétricas.
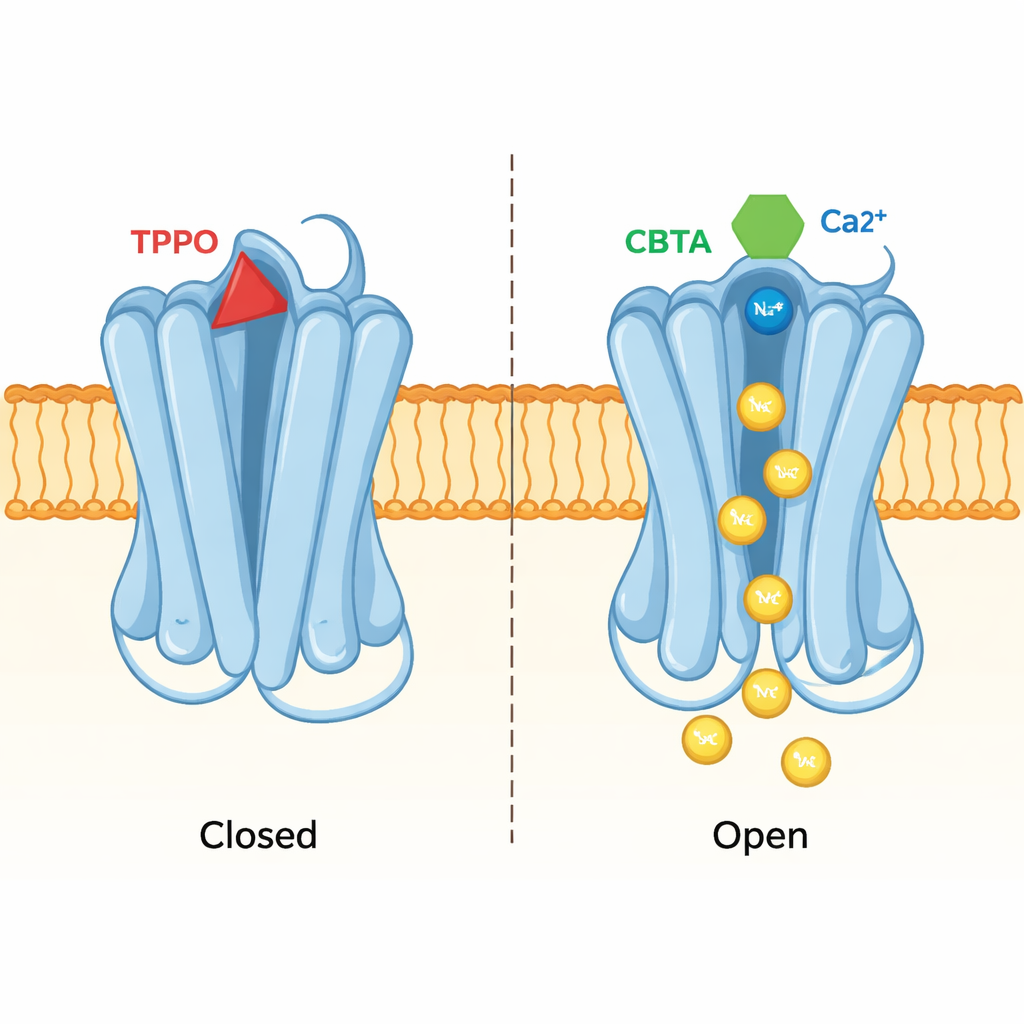
Um bolso, dois resultados opostos
A mesma abordagem estrutural revelou como um inibidor chamado TPPO usa exatamente o mesmo bolso para produzir o efeito oposto. Quando o TPPO se liga, ambos os sítios de cálcio no TRPM5 permanecem ocupados, mas o poro central do canal fica comprimido e nenhum íon passa. A comparação das estruturas ligadas ao TPPO e ao CBTA mostrou que suas formas diferentes empurram segmentos proteicos próximos em direções opostas. O CBTA incentiva movimentos que se espalham até o poro e o abrem; o TPPO, em vez disso, interrompe a comunicação entre o bolso e o poro, mantendo a porta fechada. Em essência, esse único bolso pode funcionar tanto como acelerador quanto como freio, dependendo de qual molécula o ocupa.
Redirecionando a fiação interna do canal
O estudo também mostra que esse bolso de controle pode assumir funções normalmente desempenhadas por uma região separada de ligação ao cálcio dentro da célula. Em canais mutantes onde o sítio interno de cálcio habitual está desativado, o cálcio sozinho não conseguiu abrir o TRPM5. Ainda assim, o CBTA conseguiu ativar esses mutantes e remodelou um elemento estrutural chave que liga as partes interna e externa do canal. Em outros mutantes que quebram a conexão entre a ligação do cálcio e a abertura do poro, a adição de CBTA restaurou o comportamento normal. Esses resultados revelam que o sítio recém-identificado pode redirecionar ou reparar a comunicação entre diferentes domínios do canal, atuando como um hub flexível para sinalização de longo alcance dentro da proteína.
Por que isso importa para futuros medicamentos
Para não especialistas, a mensagem central é que os pesquisadores encontraram um único bolso sensível a fármacos no TRPM5 que pode integrar ativação, ajuste fino e desligamento. Um pequeno ativador como o CBTA pode tanto mimetizar o cálcio quanto aumentar muito a sensibilidade do canal, enquanto outro composto, o TPPO, pode manter o mesmo canal preso fechado, tudo ao se ancorarem no mesmo local. Essa visão unificada de como o TRPM5 é controlado abre a porta para projetar moléculas sob medida que aumentem ou diminuam sua atividade em tecidos específicos, com aplicações potenciais que vão desde melhorar terapias baseadas no paladar e fármacos para motilidade intestinal até desenvolver novas estratégias para controlar a glicemia e doenças metabólicas.
Citação: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Palavras-chave: canal TRPM5, percepção do paladar, secreção de insulina, controle de canais iônicos, modulação alostérica