Clear Sky Science · pt
O estudo HUNT identifica fatores genéticos do hospedeiro reproduzivelmente associados à composição da microbiota intestinal humana
Por que seus genes e as bactérias do intestino importam
Cada um de nós carrega trilhões de microrganismos no intestino que ajudam a digerir alimentos, treinam nosso sistema imunológico e podem até influenciar nosso risco de doenças. Este estudo faz uma pergunta aparentemente simples: quanto desse ecossistema interno está escrito em nosso DNA? Ao escanear os genomas de dezenas de milhares de pessoas e compará-los com a composição detalhada de seus micróbios intestinais, os pesquisadores mostram que genes humanos específicos inclinam de forma consistente o microbioma em direções particulares — e que essas mudanças se conectam a condições como doença celíaca, hemorróidas e problemas cardíacos, bem como ao peso corporal.
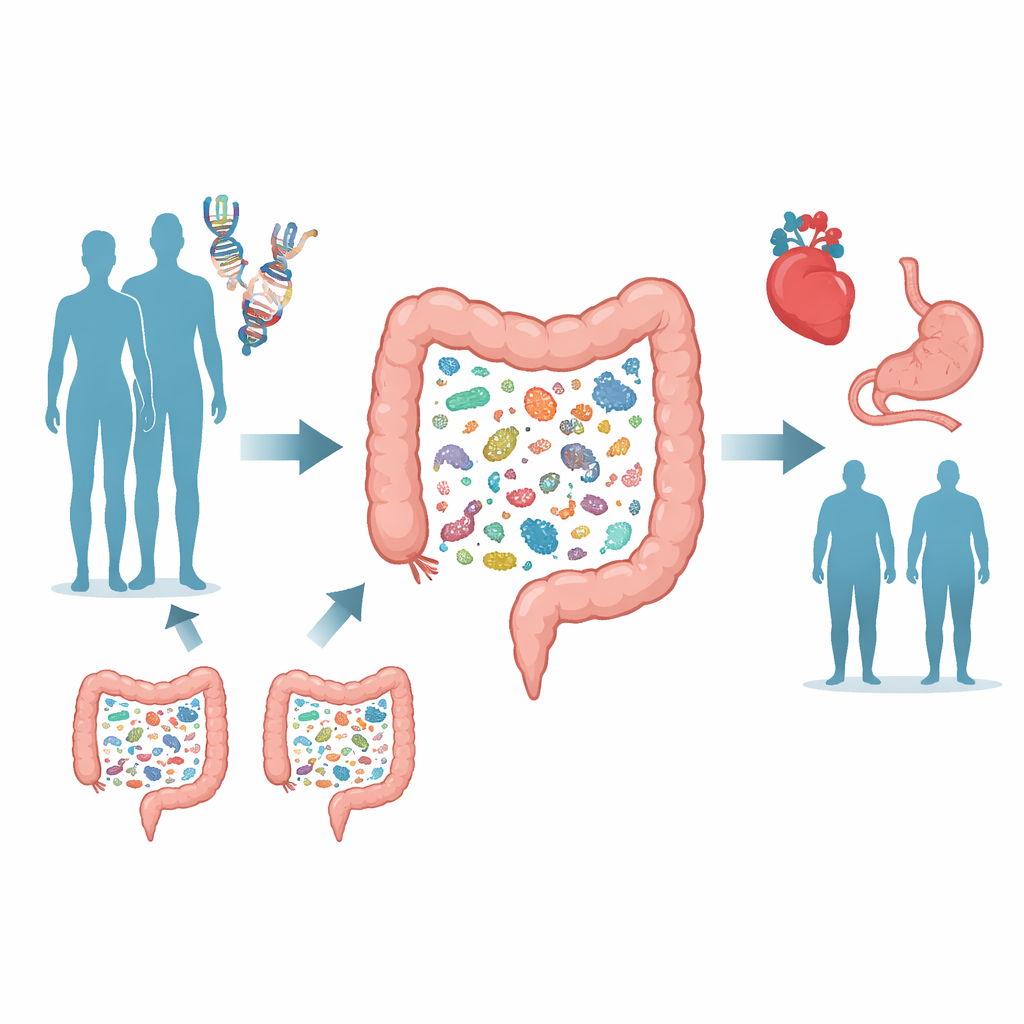
Procurando padrões em uma multidão
Para localizar ligações entre genes e micróbios, a equipe utilizou o Estudo de Saúde de Trøndelag, na Noruega, onde mais de 12.000 adultos forneceram tanto sangue para análise de DNA quanto amostras de fezes para perfilagem microbiana. Ao contrário de muitos projetos anteriores que usaram impressões bacterianas relativamente grosseiras, este trabalho contou com sequenciamento metagenômico profundo, que lê grande parte do DNA de cada amostra e pode distinguir centenas de espécies bacterianas distintas e suas capacidades metabólicas. Em seguida, os cientistas realizaram um estudo de associação em escala genômica, examinando quase oito milhões de variantes genéticas humanas para ver quais se alinhavam com diferenças na abundância relativa de 546 espécies intestinais comuns e com medidas de diversidade microbiana geral.
Seis pontos quentes genéticos que moldam o intestino
A análise revelou uma impressão genética surpreendentemente forte. Doze associações robustas emergiram entre variantes do DNA humano e espécies bacterianas específicas, agrupadas em seis regiões do genoma. Duas dessas regiões, próximas ao gene LCT, envolvido na digestão da lactose, e ao gene do grupo sanguíneo ABO, já haviam sido implicadas antes, mas quatro — próximas a HLA-DQB1, MUC12, SLC37A2 e FUT2 — eram novas ou recém-confirmadas. Por exemplo, pessoas com a versão persistente da lactase do gene LCT tendiam a carregar menos Bifidobacterium adolescentis, uma espécie que se beneficia da lactose não totalmente digerida que permanece no intestino. A região FUT2, que afeta se os açúcares do grupo sanguíneo são exibidos na superfície do revestimento intestinal, foi associada a várias espécies bacterianas que aparentam se alimentar dessas superfícies cobertas por açúcares.
Dos micróbios ao risco de doença
A história ficou mais intrigante quando os pesquisadores sobrepuseram esses resultados genéticos com grandes bancos de dados de doenças humanas. Variantes na região HLA-DQB1 que estavam ligadas a níveis mais altos de uma espécie de Agathobacter também foram associadas a um risco menor de condições autoimunes, incluindo a doença celíaca. Pessoas com doença celíaca na coorte norueguesa tendiam a apresentar níveis especialmente baixos desse micróbio, sugerindo que a doença pode, em parte, remodelar a comunidade intestinal. Outra região, próxima ao gene MUC12, estava conectada tanto à abundância de uma bactéria chamada Coprobacillus cateniformis quanto a um risco reduzido de doença hemorroidária. Experimentos em laboratório mostraram que MUC12 é fortemente produzido nas células que revestem o cólon, sugerindo que alterações sutis nessa barreira de muco podem influenciar quais bactérias prosperam e como elas, por sua vez, afetam vasos sanguíneos delicados e tecidos no reto.
Funções microbianas, saúde cardíaca e peso corporal
Além das espécies individuais, a equipe examinou o que os micróbios eram capazes de fazer agrupando seus genes em módulos funcionais, como sistemas de transporte e circuitos regulatórios. As mesmas regiões genéticas humanas — LCT, ABO e FUT2 — também influenciaram essas funções microbianas, sugerindo que nosso DNA molda não apenas quem está presente no intestino, mas o que esses micróbios estão fazendo. No sítio FUT2, por exemplo, variantes associadas ao status de "não-secretor" andavam de mãos dadas com bactérias ligadas a metabólitos potencialmente prejudiciais e com um risco elevado de colesterol alto e pressão arterial alta. Por fim, usando uma técnica chamada randomização mendeliana, que aproveita variantes genéticas como experimentos naturais, os pesquisadores encontraram evidências de que um índice de massa corporal mais alto altera causalmente o microbioma: pessoas geneticamente predispostas a maior peso tendiam a ter menor diversidade microbiana geral e mudanças consistentes em muitas espécies.
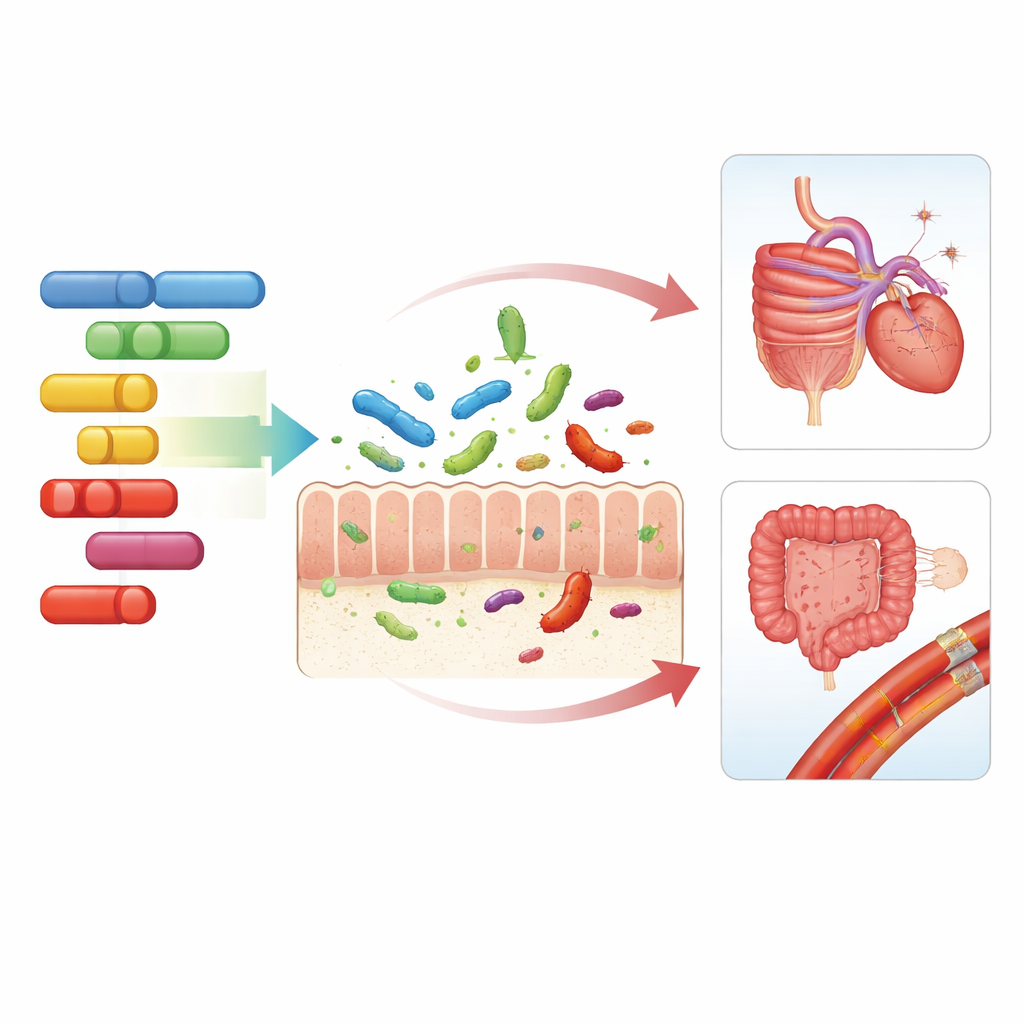
O que isso significa para a saúde cotidiana
Em conjunto, esses achados pintam o quadro de uma conversa a três entre nossos genes, nossos micróbios intestinais e nossa saúde. Certos trechos do DNA humano favorecem ou desencorajam, de forma sutil, moradores bacterianos e atividades microbianas específicas, que então se cruzam com riscos de doenças digestivas, problemas cardíacos e vasculares e os efeitos do excesso de peso corporal. Embora essas influências genéticas expliquem apenas uma parte da enorme variação nas comunidades intestinais — e ainda não se traduzam em testes clínicos — elas ajudam a esclarecer por que as pessoas respondem de maneira diferente à mesma dieta ou ambiente e apontam para abordagens mais personalizadas de nutrição e prevenção de doenças que considerem tanto o genoma quanto o microbioma.
Citação: Moksnes, M.R., Coward, E., Nethander, M. et al. The HUNT study identifies host genetic factors reproducibly associated with human gut microbiota composition. Nat Genet 58, 530–539 (2026). https://doi.org/10.1038/s41588-026-02502-4
Palavras-chave: microbioma intestinal, genética humana, microbiota e doença, peso corporal e micróbios, associação em escala genômica