Clear Sky Science · pt
GlycoRNA complexado com heparan sulfato regula o sinal VEGF-A
Como as células ajustam finamente os sinais para os vasos sanguíneos do corpo
Vasos sanguíneos não surgem apenas onde aparecem sinais de crescimento—eles precisam ser controlados com precisão para nutrir tecidos sem alimentar tumores ou causar perda de visão. Este artigo revela um “freio” inesperado em um sinal principal que promove o crescimento de vasos, chamado VEGF-A. Os autores mostram que pequenos pedaços de RNA, exibidos na superfície das células em parceria com açúcares e proteínas, podem reduzir a intensidade da mensagem do VEGF-A, reformulando nossa compreensão da linguagem que as células usam em suas superfícies.
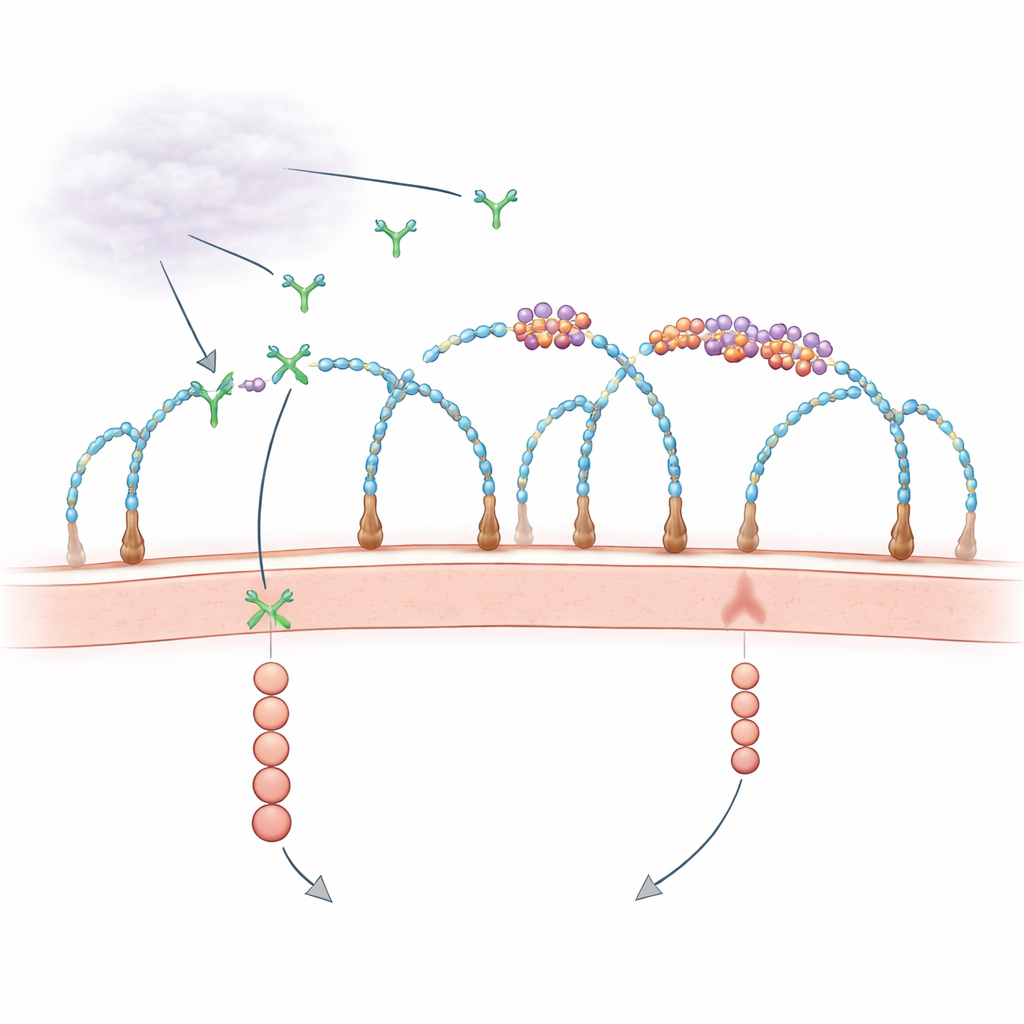
Um papel surpreendente para o RNA na superfície celular
Durante décadas, biólogos souberam que a camada externa da célula, rica em proteínas decoradas por açúcares chamadas proteoglicanos de heparan sulfato, ajuda a capturar fatores de crescimento e apresentá-los a seus receptores. Ao mesmo tempo, observações esparsas sugeriam que fragmentos de RNA fora das células poderiam influenciar o crescimento de vasos, mas os atores e mecanismos eram incertos. Trabalhos recentes revelaram que alguns pequenos RNAs estão quimicamente ligados a açúcares complexos para formar “glycoRNAs”, e que certas proteínas ligadoras de RNA também aparecem na superfície celular, agrupando-se com esses RNAs. O novo estudo faz uma pergunta direta: esses minúsculos ilhéus de RNA–proteína na membrana realmente controlam como sinais de crescimento como o VEGF-A são recebidos?
Construindo ilhas agrupadas de RNA–proteína com cadeias de açúcar
Usando triagens CRISPR de perda de função em todo o genoma e microscopia de alta resolução, os pesquisadores descobriram que cadeias de açúcar específicas—heparan sulfato com decorações de sulfato particulares—são andaimes essenciais para a montagem desses aglomerados de RNA–proteína, que eles chamam de ribonucleoproteínas de superfície celular (csRNPs). Quando enzimas-chave que constroem ou sulfatar o heparan sulfato foram removidas, os aglomerados de glycoRNA e suas proteínas parceiras desapareceram da superfície celular, mesmo que os RNAs e as proteínas ainda estivessem presentes dentro das células. Enzimas que cortam as cadeias de heparan sulfato da superfície ou bloqueiam quimicamente a sulfatação tiveram o mesmo efeito. Esses resultados mostram que cadeias intactas e corretamente sulfatadas de heparan sulfato organizam os csRNPs em ilhas nanoscópicas na membrana.
Os aglomerados de RNA atuam como freios em um poderoso sinal de crescimento de vasos
A equipe então se voltou para células endoteliais humanas, que revestem os vasos sanguíneos e respondem ao VEGF-A. Eles descobriram que essas células também exibem aglomerados de csRNPs ancorados por heparan sulfato. Tratar células vivas com RNases, enzimas que degradam RNA, removeu a componente de RNA sem perturbar as cadeias de açúcar subjacentes. Nessas condições, a forma mais comum de VEGF-A que se liga ao heparan (VEGF-A165) desencadeou uma ativação muito mais forte da via de sinalização ERK a jusante, enquanto uma forma mais curta sem a cauda de ligação ao heparan (VEGF-A121) permaneceu inalterada. Mais moléculas de VEGF-A165 se ligaram à superfície celular após a remoção do RNA, embora os níveis dos receptores tenham permanecido os mesmos. Em dispositivos microfluídicos 3D, células endoteliais expostas à RNase cresceram mais profundamente em geles de colágeno e formaram estruturas tubulares de maneira mais robusta, indicando que destruir o RNA de superfície libera um comportamento pró-angiogênico.
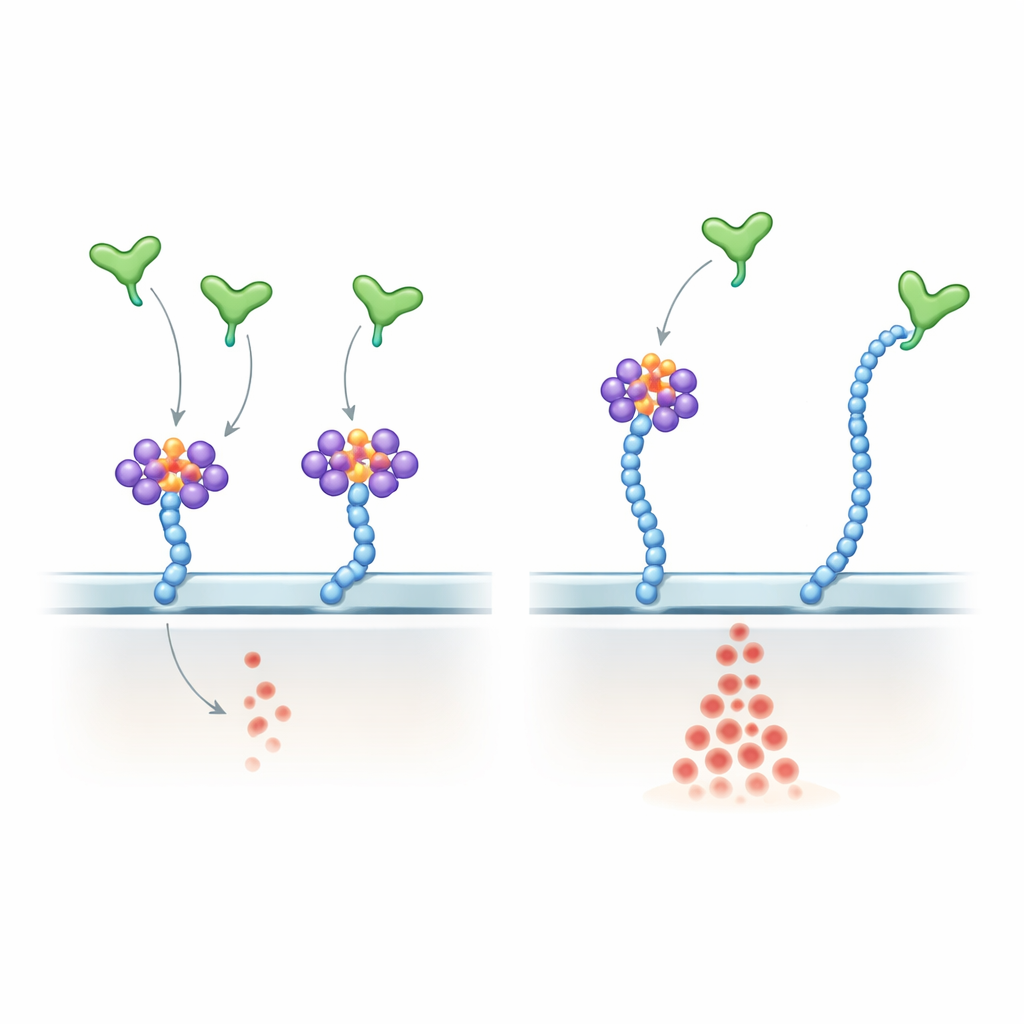
Dissecando como o VEGF-A percebe RNA versus açúcar
Para sondar o mecanismo, os autores mostraram que o VEGF-A165 se liga diretamente a pequenos RNAs selecionados, incluindo muitos glycoRNAs conhecidos, por meio de sua região C-terminal carregada positivamente—a mesma região que se liga ao heparan sulfato. Eles criaram uma versão sutil do VEGF-A165 na qual resíduos-chave de arginina nessa cauda foram trocados por lisinas. Esse mutante manteve sua carga positiva global e ainda se ligou às cadeias de heparan sulfato, mas ligou-se pobremente ao glycoRNA e tornou-se largamente insensível ao tratamento com RNase. Em células endoteliais, o mutante produziu uma ativação da via ERK mais forte e mais resistente à RNase do que o VEGF-A165 normal, imitando de perto o efeito da remoção do RNA da superfície celular. Em camundongos vivos, injetar o mutante no olho causou um crescimento vascular retiniano mais exuberante do que a proteína normal. Em embriões de zebrafish, a superexpressão da versão mutante de Vegfa interrompeu o padrãoamento vascular normal e aumentou o número de células endoteliais.
Do mecanismo básico às implicações mais amplas
Finalmente, os autores mostraram que fundir a cauda de ligação ao heparan do VEGF-A a uma proteína sinalizadora não relacionada, Wnt3a, podia redirecionar a atividade do Wnt: anexar a cauda normal reduziu mudanças desenvolvimentistas dirigidas por Wnt, enquanto anexar a cauda insensível ao RNA as aumentou. Juntos, esses experimentos sustentam um modelo no qual aglomerados csRNP, ancorados por heparan sulfato especificamente sulfatado, ligam o VEGF-A e fatores relacionados para moderar sua atividade. Quando a componente de RNA é removida ou quando fatores de crescimento perdem sua capacidade de detectar RNA, o equilíbrio tende a uma sinalização mais forte e a um desenvolvimento vascular alterado em múltiplas espécies.
Por que isso importa para a saúde e terapias futuras
Para um não especialista, a mensagem central é que as células usam não apenas proteínas e açúcares, mas também pequenos RNAs exibidos em sua superfície para ajustar finamente sinais de crescimento potentes como o VEGF-A. Esses aglomerados de RNA–proteína ancorados por açúcares funcionam como freios ajustáveis na formação de vasos sanguíneos, ajudando a garantir que novos vasos brotem onde e quando são necessários. Discutir esse equilíbrio—degradando o RNA de superfície ou alterando as propriedades de ligação ao RNA dos fatores de crescimento—pode exagerar ou desviar o crescimento vascular. Compreender essa camada de controle recém-revelada pode abrir caminho para terapias que regulem com mais precisão a angiogênese em câncer, doenças oculares, cicatrização de feridas e medicina regenerativa, ao direcionar os RNAs de superfície, seus andaimes de açúcar ou as regiões de captação de RNA dos fatores de crescimento.
Citação: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Palavras-chave: angiogênese, fator de crescimento endotelial vascular, heparan sulfato, RNA na superfície celular, glycoRNA