Clear Sky Science · pt
Convergência e divergência do desenvolvimento em modelos de células-tronco humanas do autismo
Por que esta pesquisa importa para famílias e para a sociedade
O transtorno do espectro autista é notoriamente complexo: centenas de genes distintos foram associados ao aumento do risco, e ainda assim muitas pessoas autistas compartilham desafios semelhantes na comunicação, interação social e comportamento. Este estudo faz uma pergunta aparentemente simples, mas de grandes implicações: quando alterações genéticas muito diferentes aumentam a probabilidade de autismo, elas acabam por perturbar o cérebro em desenvolvimento humano de maneiras semelhantes? Usando minúsculos modelos do córtex humano cultivados em laboratório a partir das próprias células dos pacientes, os pesquisadores rastreiam como falhas iniciais na atividade gênica podem canalizar-se em vias comuns que alteram como as células cerebrais nascem, amadurecem e se conectam.
Cultivando tecido cerebral humano em miniatura no laboratório
Para abordar essa questão, a equipe coletou células da pele ou do sangue de 55 pessoas: algumas tinham mutações raras bem caracterizadas e fortemente ligadas ao autismo, outras tinham autismo sem uma mutação maior conhecida e outras eram controles não afetados. Essas células foram reprogramadas em células-tronco pluripotentes induzidas, que podem se tornar quase qualquer tipo celular. Em seguida, os cientistas as guiaram para formar “organoides corticais” tridimensionais – pequenas esferas de tecido que imitam o desenvolvimento inicial do córtex cerebral humano. Ao longo de 100 dias, esses organoides progrediram de células progenitoras semelhantes a células-tronco para redes ricas em neurônios jovens. Em quatro pontos dessa linha do tempo (dias 25, 50, 75 e 100), a equipe mediu quais genes estavam ligados ou desligados em centenas de organoides, criando um filme detalhado das mudanças moleculares durante o desenvolvimento cerebral inicial.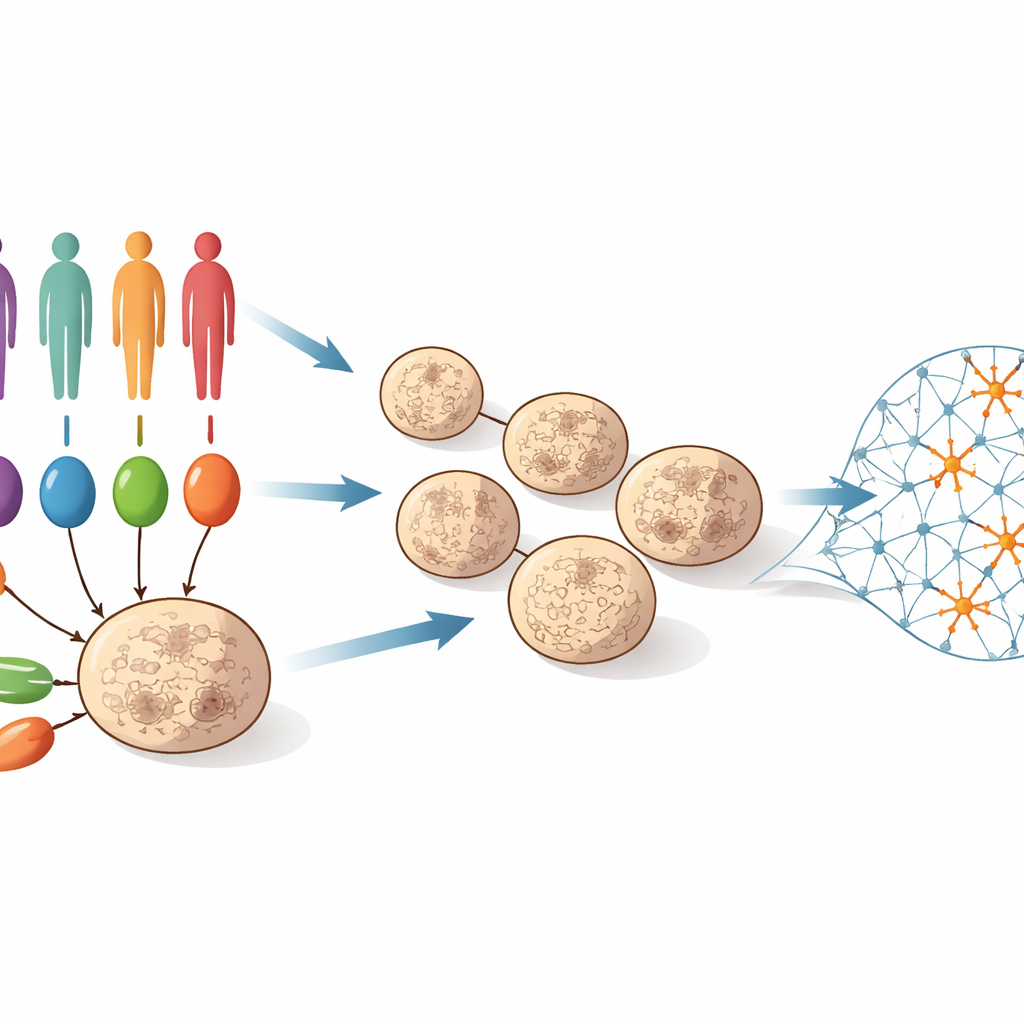
Muitos caminhos genéticos, desvios iniciais compartilhados
Embora as mutações ligadas ao autismo fossem muito diferentes – incluindo grandes segmentos de DNA ausentes ou duplicados e alterações gênicas específicas – os organoides que carregavam a mesma mutação exibiram padrões de atividade gênica altamente reprodutíveis. No início do desenvolvimento, especialmente por volta do dia 25, cada mutação produziu sua própria assinatura forte: centenas a mais de mil genes estavam desregulados em comparação com os controles. Ainda assim, mesmo nesse estágio inicial, várias mutações alteraram conjuntos sobrepostos de genes envolvidos em como o DNA é embalado e lido dentro das células. Essas mudanças compartilhadas afetaram genes de alto risco conhecidos para autismo e outros genes associados a transtornos do neurodesenvolvimento, sugerindo que mutações diferentes começam a perturbar maquinarias celulares semelhantes muito cedo na formação do cérebro.
Convergência à medida que o modelo cerebral amadurece
À medida que os organoides se desenvolveram em direção a neurônios mais maduros (por volta dos dias 75 e 100), o quadro mudou. As diferenças específicas de cada mutação tornaram-se menos distintas, enquanto as semelhanças se fortaleceram. Em quase todas as formas genéticas de autismo estudadas, os pesquisadores observaram redução da atividade de genes importantes para a sinalização elétrica nas sinapses – os pontos de comunicação entre neurônios – e aumento da atividade de genes ligados ao crescimento celular e à produção de proteínas. Surgiram mudanças sutis nas proporções e nos estágios de maturação de diferentes tipos celulares, apontando para alterações no tempo de nascimento e maturação dos neurônios, em vez de perda generalizada de tipos celulares específicos. No ponto temporal mais tardio, milhares de genes exibiram um padrão compartilhado de desregulação entre as várias mutações raras, mesmo que as próprias mutações afetassem genes originais diferentes.
Um núcleo de controle central que conecta muitos genes do autismo
Aprofundando a análise, a equipe usou análises de rede para agrupar genes que tendiam a ligar e desligar juntos em “módulos”. Um módulo em particular, chamado M5, destacou-se. Seus genes são mais ativos no início do desenvolvimento e estão fortemente enriquecidos por genes de risco para autismo, especialmente aqueles que controlam como outros genes são ativados ou desativados e como o DNA é compactado. Em organoides de vários grupos com mutações associadas ao autismo, esse módulo foi consistentemente reduzido. Os pesquisadores demonstraram que muitas das proteínas em M5 interagem fisicamente, formando um núcleo regulatório. Usando ferramentas baseadas em CRISPR para reduzir seletivamente 26 desses reguladores de M5 em células progenitoras neurais humanas, eles confirmaram que esse núcleo controla diretamente grandes conjuntos de genes a jusante, incluindo muitos genes adicionais de risco para autismo e para transtornos do neurodesenvolvimento, e que sua perturbação pode alterar vias envolvidas na formação de neurônios e na função sináptica.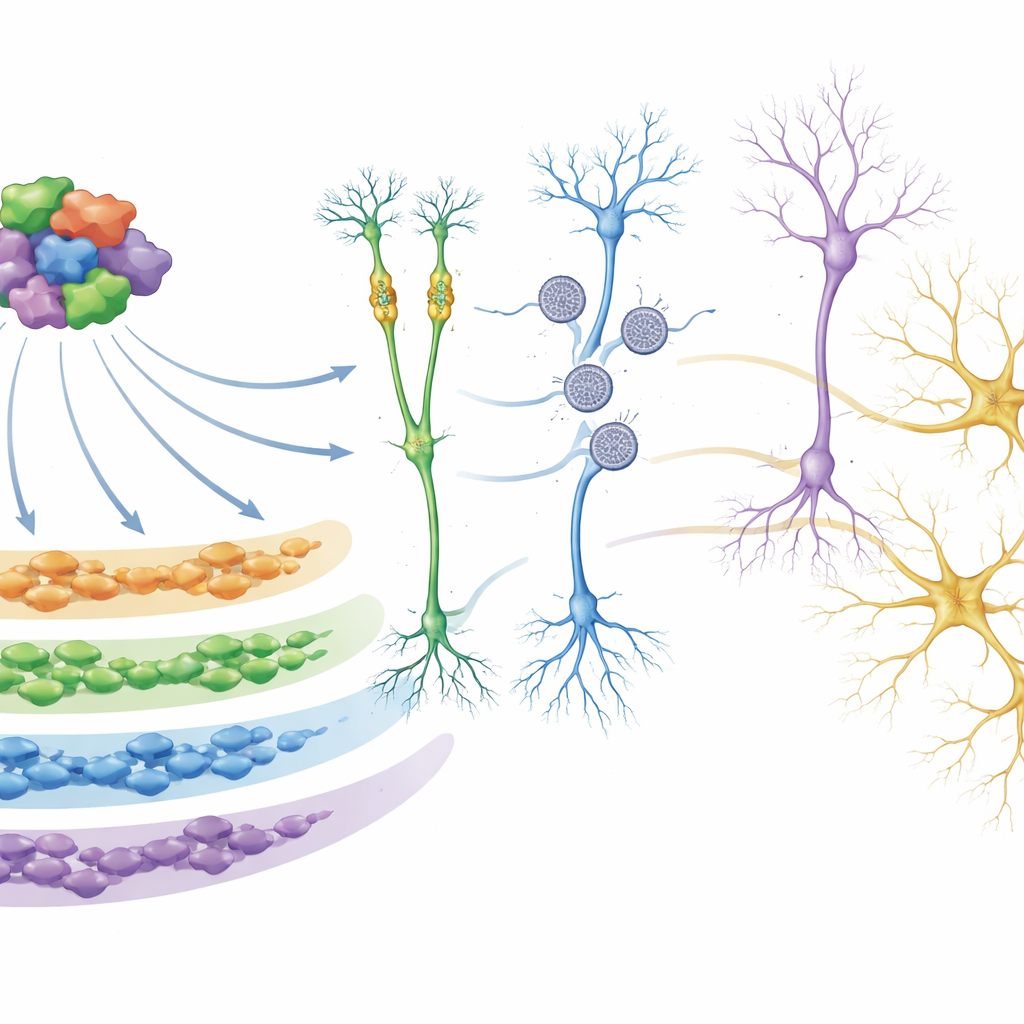
O que isso significa para a compreensão do autismo
Este trabalho sugere uma imagem unificadora: mutações raras e potentes ligadas ao autismo começam perturbando diferentes partes do genoma, mas seus efeitos se propagam através de uma rede de controle precoce compartilhada que governa como os neurônios corticais são gerados e conectados. Com o tempo, essas perturbações convergem para desfechos comuns – maturação neuronal retardada ou alterada e programas sinápticos disruptivos – mesmo que as causas genéticas iniciais sejam distintas. Para famílias, isso significa que diagnósticos muito diferentes ao nível do DNA ainda podem influenciar vias biológicas sobrepostas no cérebro em desenvolvimento. Para pesquisadores e clínicos, a rede regulatória identificada oferece um conjunto focalizado de alvos moleculares para futuras terapias voltadas a restaurar padrões mais típicos de desenvolvimento cerebral em uma ampla gama de condições genéticas relacionadas ao autismo.
Citação: Gordon, A., Yoon, SJ., Bicks, L.K. et al. Developmental convergence and divergence in human stem cell models of autism. Nature 651, 707–719 (2026). https://doi.org/10.1038/s41586-025-10047-5
Palavras-chave: transtorno do espectro autista, organoides cerebrais, modelos com células-tronco, regulação gênica, neurodesenvolvimento