Clear Sky Science · pt
Sequenciamento em escala populacional esclarece determinantes do DNA persistente do EBV
Por que um vírus comum ainda importa
A maioria dos adultos carrega o vírus Epstein–Barr (EBV), muitas vezes sem sequer saber. Para alguns, porém, esse passageiro silencioso está ligado a doenças que vão desde mononucleose até cânceres e doenças autoimunes. Este estudo faz uma pergunta simples, porém de amplo alcance: podemos usar os enormes depósitos de dados de DNA já coletados do público para identificar quem carrega mais EBV no sangue e se seus genes ajudam a determinar quem mantém o vírus sob controle e quem não?
Lendo uma marca viral oculta em nosso DNA
Biobancos modernos, como o UK Biobank e o programa All of Us dos EUA, sequenciaram o DNA completo de centenas de milhares de voluntários. Esses projetos focaram nos genes humanos, mas os dados brutos também contêm fragmentos dispersos de DNA de vírus. Os pesquisadores perceberam que o genoma humano de referência usado para alinhamento inclui um “cromossomo” extra para o EBV. Ao reexaminar leituras que mapeavam para esse segmento do EBV, eles puderam estimar quantas cópias do genoma do EBV estavam presentes no sangue de cada pessoa no momento da amostragem. Após mascarar cuidadosamente algumas regiões repetitivas enganosas, definiram como tendo “DNAemia por EBV” as pessoas com níveis claramente detectáveis — uma quantidade mensurável de DNA do EBV circulando no sangue.
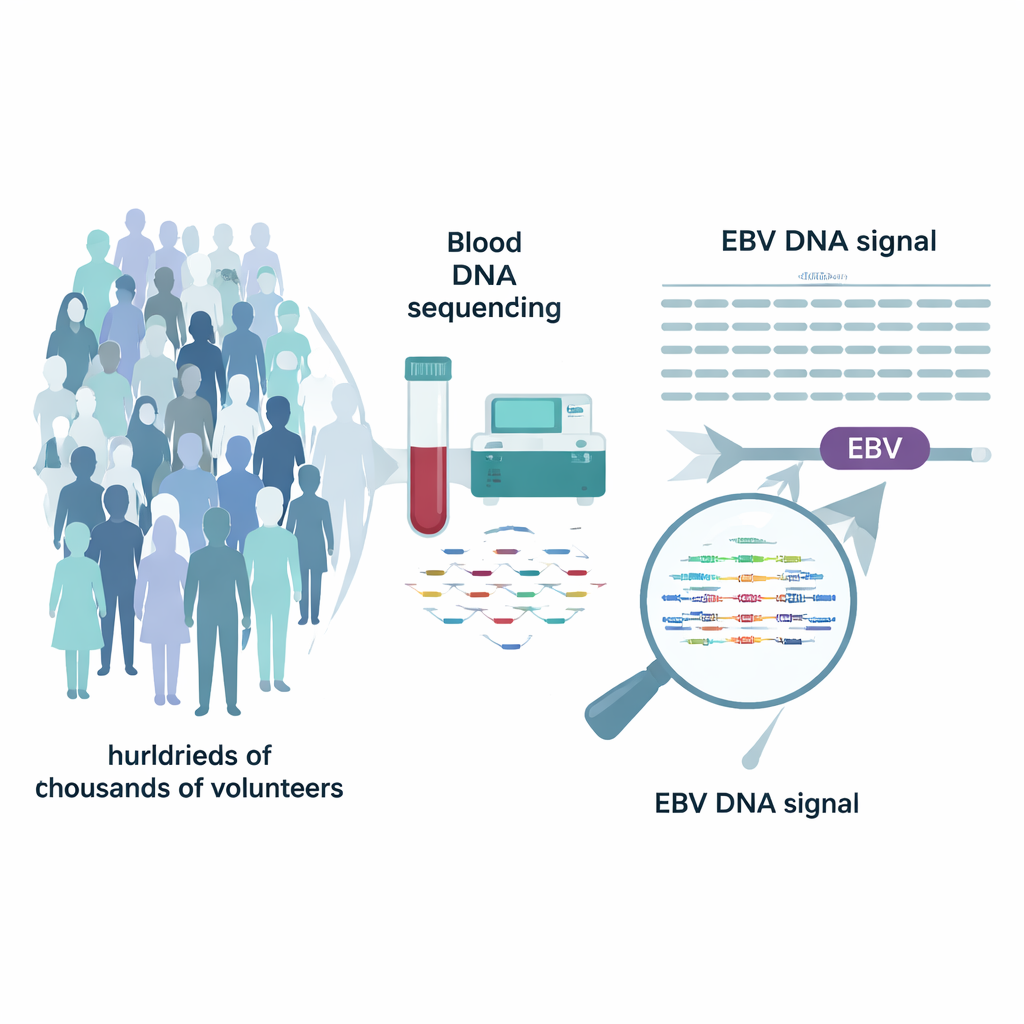
Uma pequena minoria carrega alta carga viral
Analisando quase meio milhão de pessoas no UK Biobank e um quarto de milhão no All of Us, a equipe constatou que a maioria dos adultos não tinha EBV detectável no sangue, embora mais de 90% apresentassem evidência de infecção passada em testes de anticorpos. Cerca de 10% dos participantes, no entanto, caíram em uma cauda da distribuição com níveis claramente elevados de DNA do EBV. Essas pessoas tendiam a ser mais velhas, mais frequentemente do sexo masculino e apresentavam uma probabilidade ligeiramente maior de estar usando medicamentos imunossupressores. Padrões semelhantes apareceram em ambas as coortes, e em um conjunto separado de amostras de saliva o vírus era muito mais comum, ressaltando que o EBV ocupa diferentes reservatórios no corpo e que medições no sangue capturam apenas um deles.
Relações entre persistência viral e doença
Com esse novo biomarcador em mãos, os autores investigaram como a persistência do DNA do EBV no sangue se relaciona com a saúde. Eles vasculharam milhares de códigos de diagnóstico e medições laboratoriais para ver quais eram mais frequentes em pessoas com DNAemia por EBV. Emergiram associações fortes com condições já suspeitas de ligação ao EBV, incluindo linfoma de Hodgkin, artrite reumatoide, lúpus, doença pulmonar obstrutiva crônica e certos cânceres de pulmão. Também houve sinais para problemas cardiovasculares, insuficiência renal, depressão e fadiga, e associações sugestivas com desordens neurológicas raras, como a neuromielite óptica. Muitos desses padrões foram reproduzidos na coorte independente All of Us. O estudo não pode provar que o EBV causa esses problemas, mas mostra que níveis altos de DNA do EBV no sangue são um marcador de riscos de saúde mais amplos e de distúrbios imunológicos.
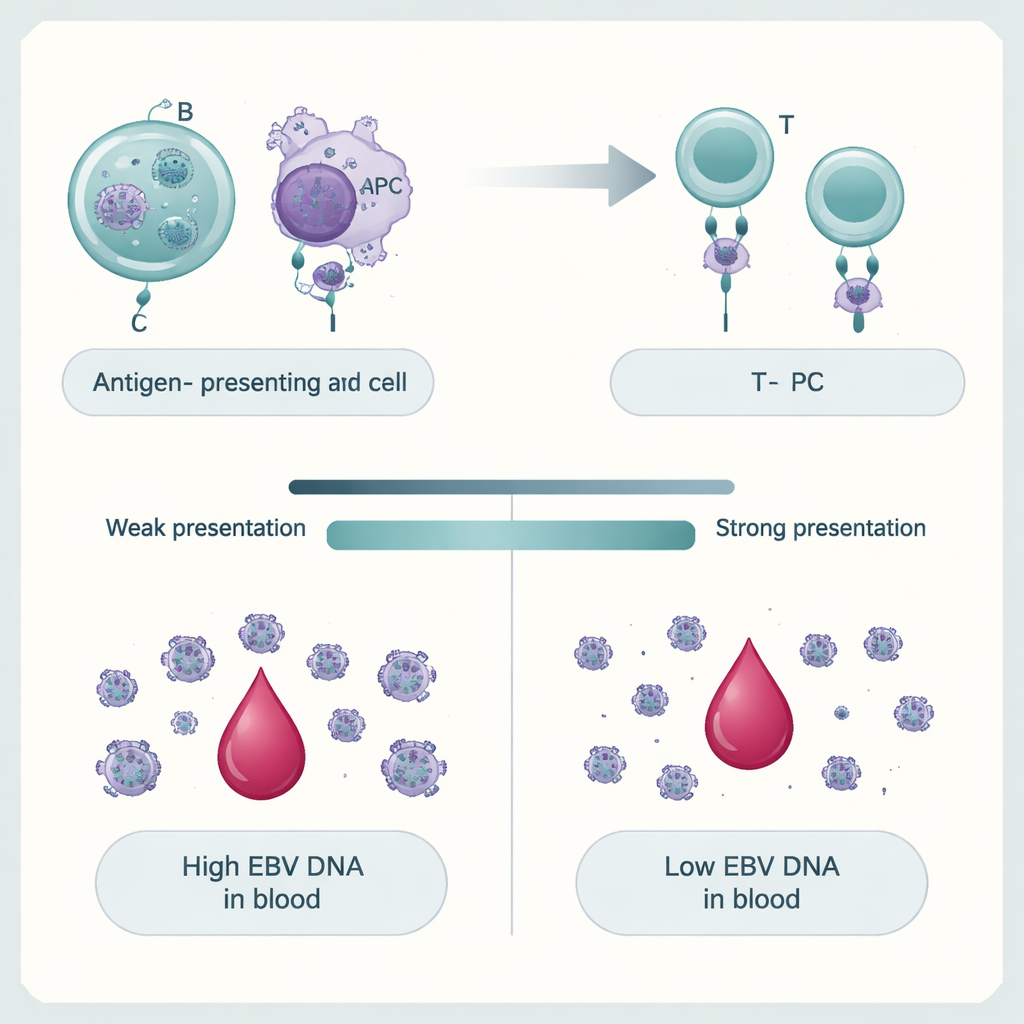
Como nossos genes moldam o controle do vírus
A equipe então investigou por que apenas algumas pessoas apresentam altos níveis de DNA do EBV. Ao examinar milhões de variantes genéticas pelo genoma, eles mostraram que a DNAemia por EBV é um traço poligênico: muitas pequenas diferenças no DNA, em conjunto, deslocam os níveis virais para cima ou para baixo. Os sinais mais fortes se agruparam em e ao redor de genes do complexo de histocompatibilidade principal (MHC), que ajudam as células imunes a exibir fragmentos virais para os linfócitos T. Variantes que alteram essas proteínas, particularmente as moléculas do MHC classe II, estiveram fortemente ligadas à persistência do DNA do EBV. Genes ativos em células B — o principal lar de longo prazo do EBV — e em outras células apresentadoras de antígeno foram especialmente enriquecidos. Usando modelos computacionais de como diferentes variantes humanas do MHC ligam pedaços do proteoma do EBV, os autores encontraram que versões previstas para apresentar fragmentos do EBV mais fortemente tendiam a proteger contra altos níveis de DNA do EBV, enquanto apresentadoras mais fracas se associavam à persistência.
O que isso significa para entender a infecção
Para não especialistas, a mensagem central é que nosso equilíbrio de longo prazo com o EBV não é aleatório. Ao minerar dados de DNA em escala populacional já existentes, o estudo mostra que a composição genética de uma pessoa — especialmente em genes imunes que exibem pedaços virais aos linfócitos T — ajuda a determinar quanto tempo o EBV persiste em seu sangue. Níveis altos marcam um subconjunto de pessoas com risco aumentado para uma variedade de doenças imunológicas, respiratórias e possivelmente neurológicas. O trabalho oferece um roteiro para transformar dados de sequenciamento antigos em novos insights sobre muitos vírus que compartilham nossos corpos e sugere que estratégias direcionadas para estimular ou imitar uma apresentação eficaz de antígenos podem, um dia, ajudar a manter infecções crônicas como o EBV sob melhor controle.
Citação: Nyeo, S.S., Cumming, E.M., Burren, O.S. et al. Population-scale sequencing resolves determinants of persistent EBV DNA. Nature 650, 664–672 (2026). https://doi.org/10.1038/s41586-025-10020-2
Palavras-chave: Vírus Epstein–Barr, persistência viral, genética humana, doença autoimune, sequenciamento de biobancos