Clear Sky Science · pt
Vacinas de mRNA individualizadas evocam imunidade duradoura de células T em TNBC adjuvante
Nova esperança após o tratamento do câncer de mama
Para muitas mulheres com uma forma agressiva de câncer de mama chamada câncer de mama triplo‑negativo, o medo não termina quando a quimioterapia e a cirurgia acabam. Esse câncer tem alto risco de recidiva e de espalhamento, frequentemente dentro de apenas alguns anos. O estudo descrito aqui testa uma vacina altamente personalizada, construída a partir das próprias mutações do tumor de cada paciente, para avaliar se ela pode treinar o sistema imunológico a ficar de guarda por anos e reduzir a probabilidade de recaída após o término do tratamento padrão.
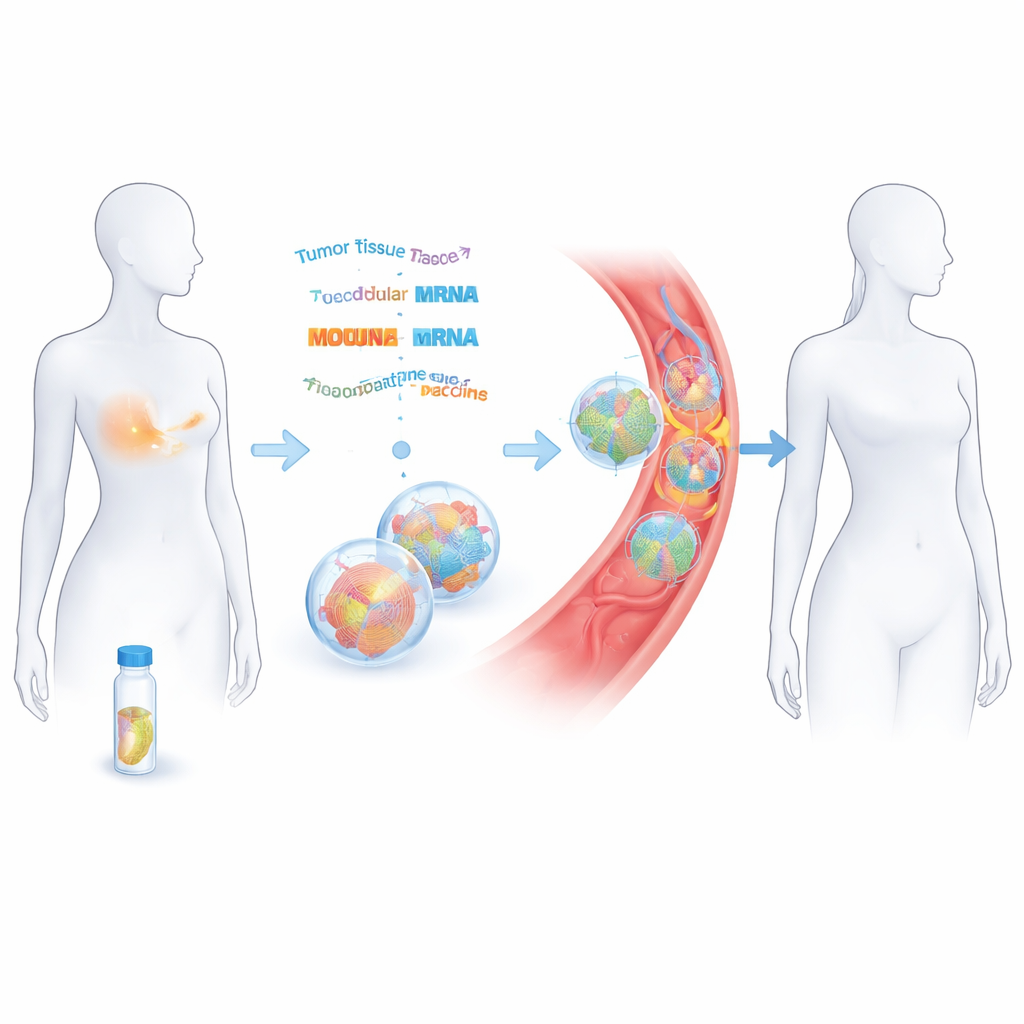
Transformando um tumor removido em uma vacina personalizada
Os pesquisadores trabalharam com 14 mulheres que tinham câncer de mama triplo‑negativo em estágio inicial e que já haviam recebido cirurgia e quimioterapia com intenção curativa. A partir do tecido tumoral removido, eles sequenciaram o DNA e o RNA para catalogar as mutações únicas do câncer. Usando ferramentas computacionais, previram quais dessas alterações poderiam ser reconhecidas como estranhas pelas células imunes. Até 20 desses “neoantígenos” foram então concatenados e codificados em duas fitas de RNA mensageiro (mRNA), semelhante em princípio às vacinas contra a COVID‑19, mas adaptadas a cada paciente. Essas fitas de mRNA foram embaladas em pequenas bolhas de gordura e administradas por via venosa em oito doses ao longo de cerca de dois meses.
Como a vacina estimula os defensores imunológicos
Uma vez no organismo, o mRNA instrui sentinelas imunes chamadas células dendríticas a produzir brevemente as proteínas neoantigênicas e exibir fragmentos delas em sua superfície. Isso atua como um cartaz de mais procurados para as células T, a principal força do sistema imunológico na defesa contra o câncer. A equipe coletou sangue antes da vacinação e em vários pontos posteriores para testar se surgiam células T específicas para os neoantígenos e quão fortes eram essas respostas. Usando ensaios laboratoriais sensíveis, descobriram que todas as pacientes desenvolveram respostas de células T novas ou reforçadas contra pelo menos uma das mutações selecionadas, e a maioria respondeu a várias. Em muitos casos, grandes frações das células T circulantes — níveis geralmente observados apenas com terapias celulares potentes — passaram a reconhecer alvos específicos do tumor.
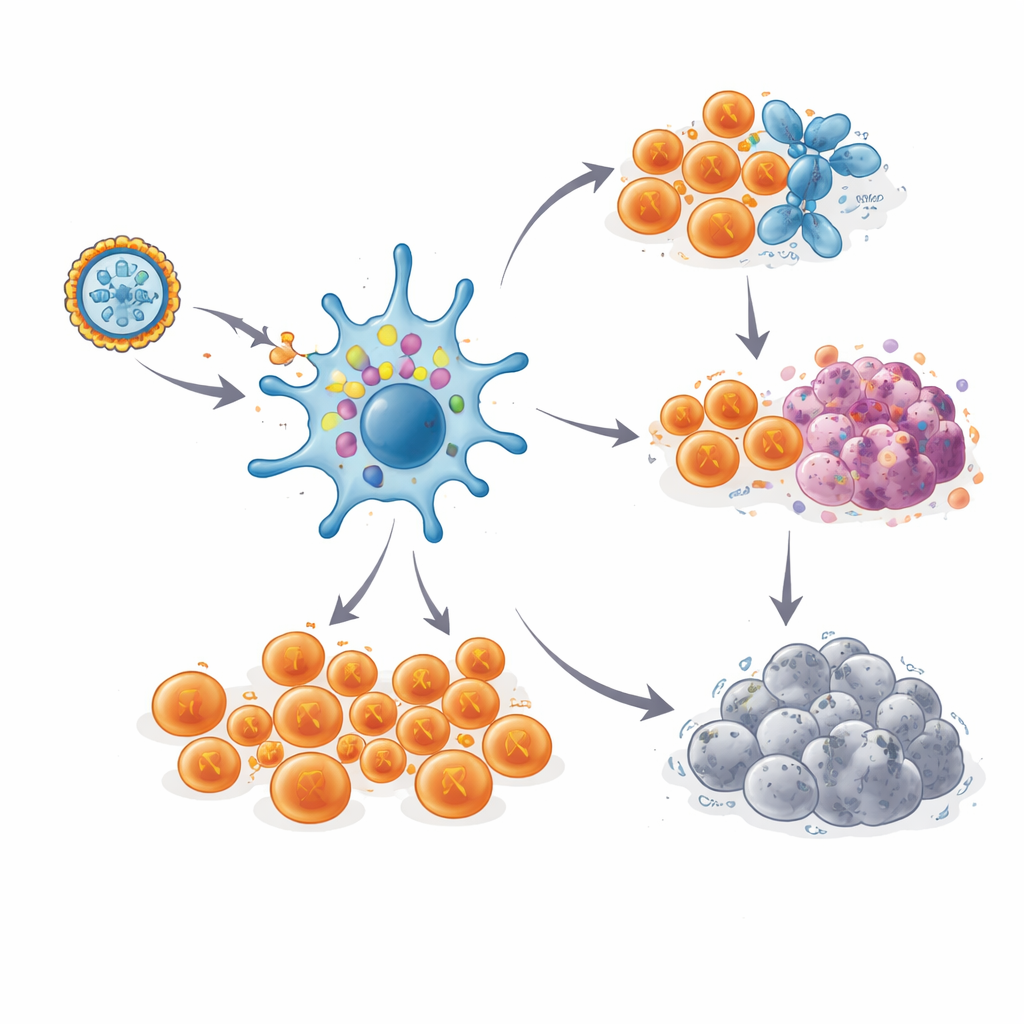
Memória imunológica de longa duração
Importante, essas respostas de células T não desapareceram rapidamente. Na maioria das pacientes, respostas fortes atingiram pico durante o período de vacinação, caíram ligeiramente e depois permaneceram em níveis elevados por um a três anos e meio, mesmo sem doses de reforço. Ao rastrear os “códigos de barra” únicos dos receptores de clones individuais de células T, os cientistas puderam acompanhar células reativas a neoantígenos específicos por até seis anos em uma paciente que permaneceu sem câncer. Análises detalhadas em célula única mostraram dois destinos principais para essas células. Muitas tornaram‑se células T citotóxicas altamente armadas, prontas para destruir qualquer célula que exibisse o neoantígeno correto. Outras evoluíram para um raro pool de memória com características de célula‑tronco e marcadores de autorrenovação, sugerindo um reservatório capaz de regenerar novas ondas de combatentes caso células cancerosas reapareçam.
O que aconteceu com as pacientes
Após mediana de pouco mais de cinco anos de acompanhamento desde a primeira dose da vacina, onze das quatorze mulheres não tiveram recidiva do câncer; uma delas morreu por causas não relacionadas enquanto ainda estava em remissão. Três mulheres recidivaram, e seus casos oferecem pistas sobre por que uma vacina personalizada às vezes pode falhar. Uma paciente desenvolveu apenas uma resposta fraca de células T e depois teve benefício com um medicamento imunoterápico diferente, um anticorpo anti‑PD‑1, antes de eventualmente sucumbir a doença disseminada. Uma segunda paciente tinha risco hereditário e tumores em ambas as mamas; apenas um tumor foi usado para projetar a vacina, e evidências posteriores mostraram que a recidiva veio do tumor geneticamente distinto e não vacinado. A terceira paciente apresentou células T induzidas pela vacina que infiltraram o tumor recorrente, mas as células cancerosas haviam perdido em grande parte moléculas-chave necessárias para apresentar neoantígenos na superfície, escondendo‑se efetivamente do ataque imune.
Por que este trabalho importa para o futuro
Este estudo de fase inicial foi pequeno e não teve grupo controle, portanto não pode provar que a vacina sozinha preveniu recidivas. Não obstante, demonstra que construir uma vacina complexa e personalizada de mRNA a partir do próprio tumor de um paciente é viável em ambientes hospitalares de rotina, é geralmente bem tolerada e pode desencadear exércitos potentes e duradouros de células T contra múltiplos alvos específicos do câncer. Os achados também destacam rotas de escape que os tumores podem usar, como a perda da maquinaria de apresentação de antígenos ou o surgimento a partir de lesões não alvoadas, apontando para combinações com outras terapias imunológicas e a necessidade de sequenciamento tumoral mais extenso. Para pacientes enfrentando câncer de mama triplo‑negativo, este trabalho sugere que uma vacina sob medida, administrada após o tratamento padrão, poderia um dia ajudar a evitar o retorno da doença ao transformar seu próprio sistema imunológico em uma linha de defesa durável e altamente específica.
Citação: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Palavras-chave: câncer de mama triplo‑negativo, vacinas de mRNA contra o câncer, imunoterapia com neoantígenos, imunidade de células T, recorrência tumoral