Clear Sky Science · pt
Trajetórias de ativação específicas do ligante ditam o sinalização de GPCRs em células
Como Um Receptor Pode Se Comportar Como Muitos Interruptores
Muitos dos medicamentos atuais atuam sobre uma enorme família de proteínas de superfície celular chamadas receptores acoplados à proteína G, ou GPCRs. Esses receptores influenciam a frequência cardíaca, o humor, a respiração e inúmeras outras funções do corpo. Durante décadas foram tratados como interruptores simples liga–desliga: um fármaco se liga, o interruptor vira e um sinal flui para o interior da célula. Este artigo mostra que a realidade é muito mais rica. Usando um novo tipo de "espião" fluorescente integrado diretamente no receptor, os autores observam, em células vivas, como diferentes fármacos conduzem o mesmo receptor por trajetórias de ativação distintas — como escolher rotas diferentes por uma cidade — para produzir padrões diferentes de sinalização. Entender essas rotas ocultas pode ajudar a projetar medicamentos que forneçam o benefício desejado evitando efeitos colaterais.
Observando a Campainha da Célula em Tempo Real
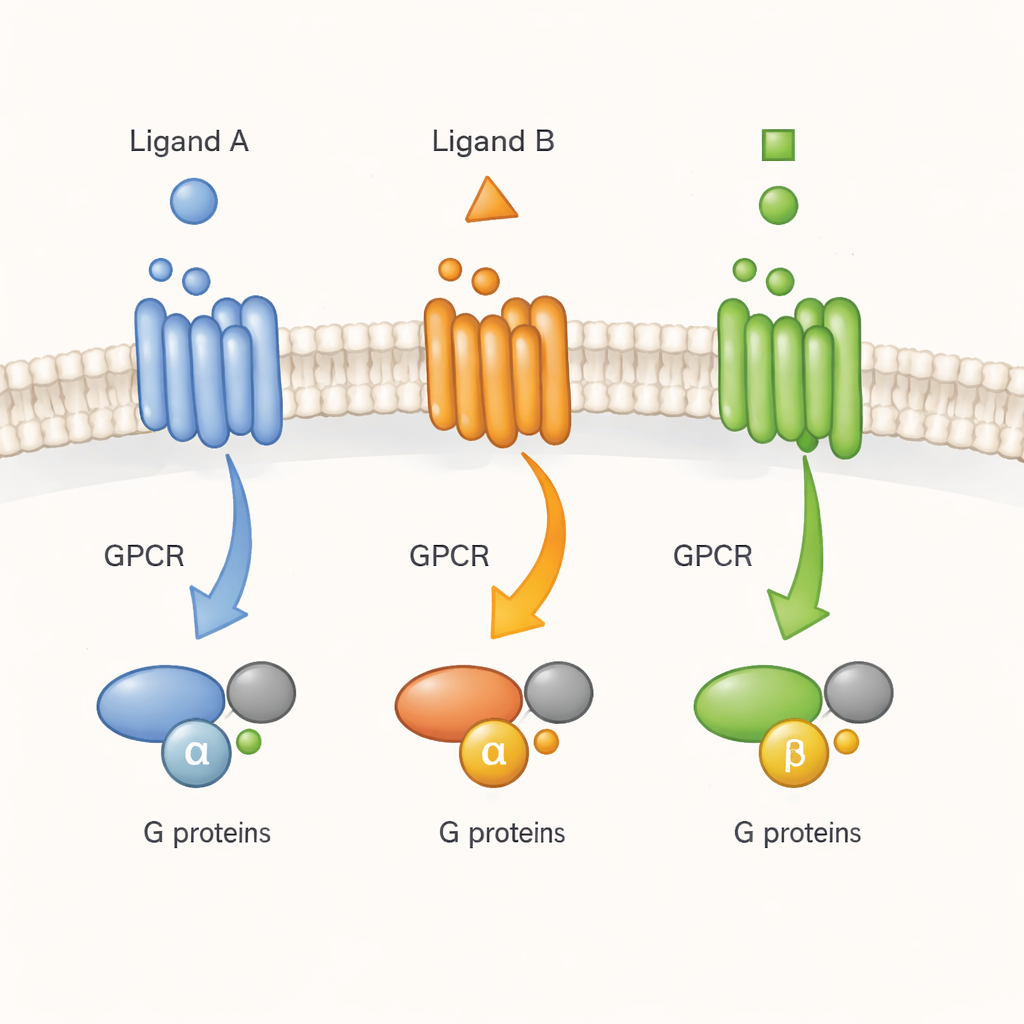
GPCRs costumam ser descritos como campainhas moleculares: uma molécula sinalizadora (um ligante) toca do lado de fora, e o receptor passa a mensagem para proteínas G do lado de dentro. Trabalhos anteriores com receptores purificados em detergentes haviam sugerido que os GPCRs não simplesmente alternam entre uma forma inativa e uma ativa. Em vez disso, eles amostram muitas conformações que os fármacos podem estabilizar em graus diferentes. Mas não estava claro se essa mesma complexidade existia no ambiente congestionado e dinâmico de uma célula viva. Aqui, os autores se concentram em um receptor representativo, o receptor muscarínico de acetilcolina M2, um importante regulador da atividade do coração e dos nervos, e perguntam se diferentes ligantes o conduzem a formas ativas distintas que importam para a sinalização celular real.
Construindo Pequenos Repórteres Luminosos na Superfície do Receptor
Para seguir os movimentos do receptor sem perturbar sua função normal, a equipe usou expansão do código genético, uma tecnologia que permite inserir um aminoácido artificial em posições selecionadas na superfície externa do receptor. Essa "âncora" química pode ser clicada a uma pequena corante fluorescente em células vivas. Ao escanear 72 posições e manter apenas aquelas que ainda se comportavam como receptores normais, eles construíram um painel de sete variantes do receptor M2, cada uma com um único corante em um sítio diferente do laço externo. Quando o mensageiro natural acetilcolina foi aplicado, o brilho do corante nesses sítios aumentou ou diminuiu de maneiras características, revelando como cada parte da superfície externa do receptor se deslocou quando a sinalização começou. Crucialmente, esses receptores etiquetados ainda podiam ativar proteínas G e sofrer internalização normal, mostrando que os repórteres eram fiéis em vez de disruptivos.
Fármacos Deixam "Impressões Digitais Conformacionais" Distintas
Os pesquisadores então compararam vários fármacos que todos ativam o receptor M2, mas com diferentes intensidades: a própria acetilcolina do organismo, um agonista sintético super-forte chamado iperoxo, e dois agonistas parciais mais fracos, arecolina e pilocarpina. Cada fármaco produziu um padrão único de mudanças de fluorescência ao longo dos sete sítios dos repórteres — uma impressão digital conformacional. Na maioria das posições, a magnitude do movimento acompanhou o quão fortemente o fármaco ativava o receptor. Em dois sítios, entretanto, a relação foi invertida: os fármacos mais fracos produziram as maiores mudanças, e o fármaco mais forte produziu quase nenhuma. Tal comportamento não pode ser explicado por um único estado ativo. Em vez disso, indica que o mesmo receptor, em células vivas, pode adotar várias formas ativas distintas, algumas favorecidas por fármacos fortes, outras por fármacos fracos.
Complexos Múltiplos e Rotas Temporizadas para a Sinalização
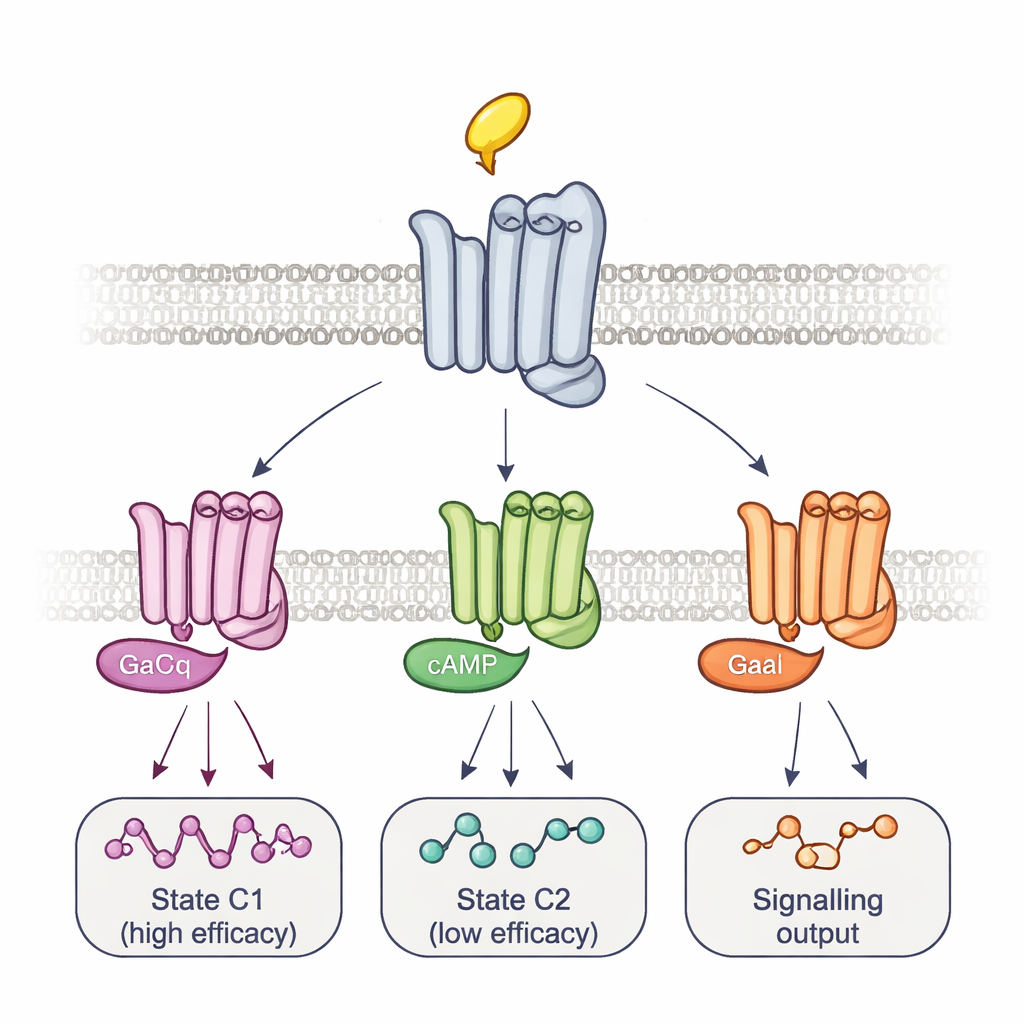
Para conectar essas conformações à sinalização real, a equipe alterou as próprias proteínas G. A sobreexpressão de uma proteína G mutante que forma complexos muito estáveis e de longa duração com receptores apagou seletivamente o sinal de alguns sítios repórteres enquanto aumentava outros. Esse padrão, juntamente com o tempo das mudanças de fluorescência, revelou pelo menos dois principais complexos receptor–proteína G: um complexo de formação rápida e alta eficácia e outro mais lento e de baixa eficácia. Diferentes fármacos deslocaram o equilíbrio entre esses complexos e até usaram etapas intermediárias distintas para chegar lá, traçando trajetórias de ativação específicas do fármaco. Usando um ensaio separado de bioluminescência que monitora um painel de 14 subtipos de proteínas G, os autores mostraram que esses equilíbrios ajudam a determinar não apenas quão fortemente um fármaco ativa a sinalização no geral, mas quais proteínas G exatas são ativadas. Por exemplo, a arecolina ativou preferencialmente certos proteins Go, enquanto a pilocarpina favoreceu fortemente o complexo de baixa eficácia.
Por Que Isso Importa para Medicamentos Melhores
Para não especialistas, a mensagem-chave é que um único receptor não é apenas um interruptor, mas um conjunto de interruptores relacionados, cada um alcançável por caminhos diferentes e cada um conectado a efeitos downstream ligeiramente distintos. Este estudo fornece uma visão direta dessas rotas e estados em células intactas, em vez de em sistemas simplificados de tubo de ensaio. Ao mapear como fármacos particulares tendenciam o receptor a estados que favorecem complexos específicos e parceiros de proteínas G, os pesquisadores obtêm um roteiro para projetar medicamentos "mais inteligentes" — compostos que direcionam receptores a estados que geram sinais úteis enquanto evitam aqueles ligados a efeitos colaterais. A estratégia de biossensor fluorescente desenvolvida aqui deve ser adaptável a muitos outros receptores, abrindo uma janela para a coreografia em tempo real da ação de fármacos em células vivas.
Citação: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Palavras-chave: Sinalização de GPCR, eficácia do ligante, proteínas G, biossensores conformacionais, descoberta de fármacos