Clear Sky Science · pt
Tolerância à doença e patogênese da infecção: compromissos relacionados à idade em camundongos
Por que algumas infecções são mais letais com a idade
Por que adultos mais velhos frequentemente se saem pior durante infecções graves, mesmo quando são expostos aos mesmos micróbios que pessoas mais jovens? Este estudo usa camundongos para explorar esse enigma, com foco na sepse — uma reação à infecção que ameaça a vida. Os pesquisadores mostram que os programas protetores do próprio corpo podem inverter-se com a idade: genes que protegem o coração e outros órgãos na juventude podem, mais tarde na vida, promover dano. Compreender essa mudança dependente da idade pode alterar a forma como projetamos tratamentos para infecções em crianças, adultos e idosos.
Caminhos diferentes a partir da mesma infecção
Para imitar uma emergência humana comum, a equipe infectou camundongos jovens e idosos com uma mistura de duas bactérias frequentes causadoras de sepse, Escherichia coli e Staphylococcus aureus. Eles escolheram cuidadosamente uma dose que matou cerca de metade dos animais (uma LD50), de modo que alguns camundongos sobreviveriam e outros não, apesar de terem a mesma exposição inicial. Surpreendentemente, ambos os grupos etários apresentaram quantidades semelhantes de bactérias nos órgãos. O que diferiu foi como seus corpos lidaram com o dano. Camundongos jovens e idosos seguiram “jornadas de saúde” distintas durante a sepse: temperatura corporal, sinais visíveis de doença e o momento do declínio ou recuperação dividiram‑se em trajetórias claras de sobreviventes e não sobreviventes. 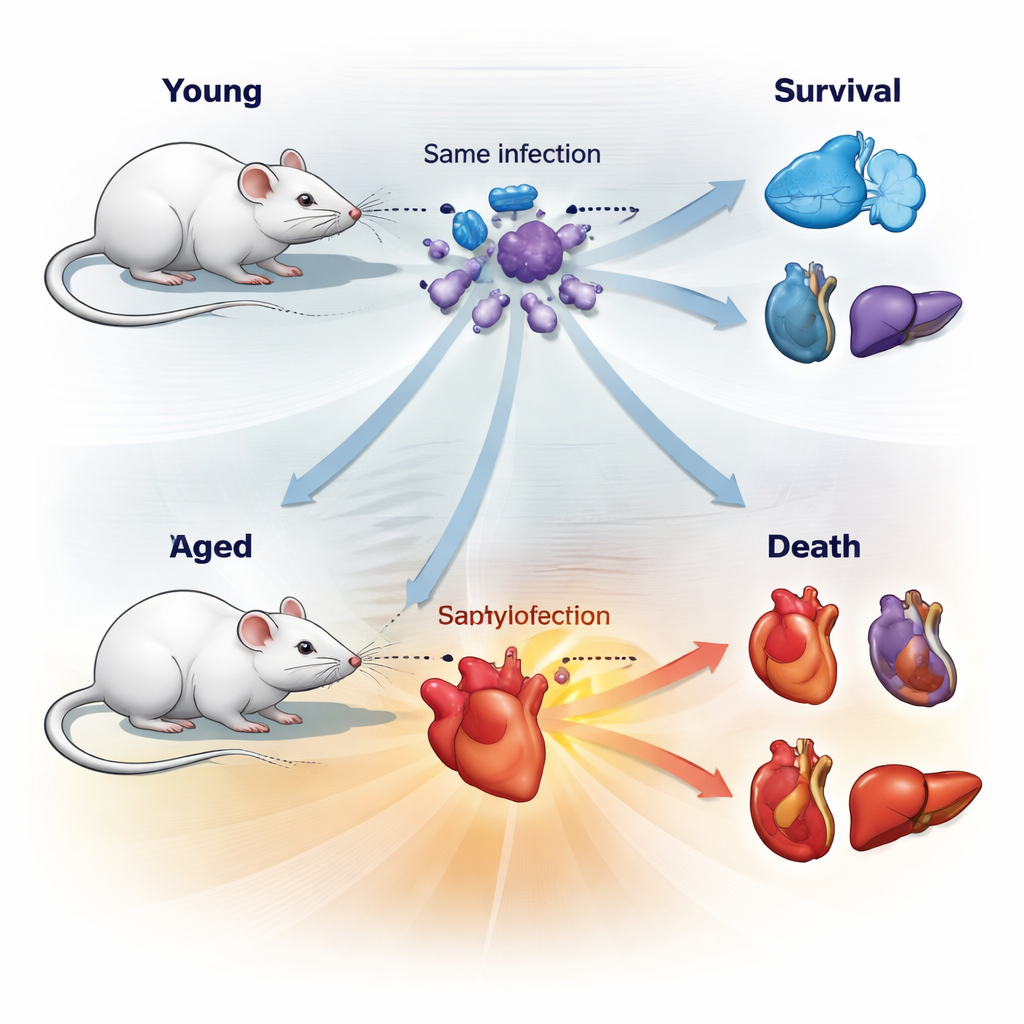
Mudanças cardíacas contam duas histórias específicas da idade
Quando os cientistas examinaram os órgãos, o coração emergiu como um ator central. Camundongos jovens que morreram de sepse desenvolveram corações aumentados e inchados com câmaras dilatadas — sinais de esforço severo — e apresentaram níveis elevados de marcadores sanguíneos usados em hospitais para sinalizar lesão cardíaca e insuficiência. Seus rins e fígados também foram afetados, mas de forma menos dramática. Em contraste, camundongos idosos que morreram mostraram o padrão cardíaco oposto: seus corações tornaram‑se menores e atrofiados, mesmo com lesões renais e perda de função renal mais pronunciadas. Sobreviventes idosos, curiosamente, frequentemente tinham corações aumentados, porém com dano geral menor. O perfil de atividade gênica do tecido cardíaco confirmou que camundongos jovens e idosos ativavam programas de remodelamento diferentes: corações mais jovens ligaram vias associadas ao crescimento e mudança estrutural, enquanto corações mais velhos ativaram vias ligadas à degradação de proteínas e atrofia celular.
Um circuito protetor em corações jovens
Aprofundando nas assinaturas moleculares, os pesquisadores destacaram um gene controlador chamado Foxo1 e um de seus alvos, Trim63, que codifica uma proteína conhecida como MuRF1 envolvida em marcar proteínas musculares para reciclagem. Em corações de jovens sobreviventes, Foxo1 e Trim63 estavam fortemente ativados em comparação com camundongos jovens que morreram ou que nunca foram infectados. Bloquear FoxO1 com um fármaco, ou deletá‑lo especificamente nas células musculares cardíacas, tornou os camundongos jovens muito mais propensos a adoecer e morrer, embora seus níveis bacterianos e sinais inflamatórios permanecessem semelhantes. Da mesma forma, camundongos jovens sem Trim63 sofreram maior inchaço cardíaco, mais vazamento de marcadores de dano cardíaco para o sangue e lesões mais amplas em fígado e rim. Esses resultados indicam que, na juventude, a via FoxO1–Trim63 atua como um sistema de tolerância à doença: ela não combate diretamente os micróbios, mas ajuda o coração a se adaptar ao estresse e evita falência múltipla de órgãos.
Quando o protetor de ontem vira a ameaça de hoje
Os mesmos genes contaram uma história diferente na idade avançada. Em camundongos idosos, a sobrevivência deixou de depender da ativação de FoxO1 no coração. Em vez disso, desligar FoxO1 — seja geneticamente nas células musculares ou com um fármaco — na verdade protegeu os animais mais velhos contra a doença e a morte induzidas pela sepse. Camundongos idosos sem Trim63, ou tratados com um inibidor de MuRF1, também se saíram melhor: apresentaram corações aumentados, porém estruturalmente mais saudáveis, níveis mais baixos de marcadores sanguíneos que sinalizam esforço cardíaco e menos danos a rins e fígado. Em outras palavras, o mesmo circuito que promove adaptação saudável à infecção em corações jovens passou a impulsionar remodelamento prejudicial e lesão de órgãos em corações mais velhos. Essa inversão de função com a idade se encaixa em um conceito da biologia evolutiva chamado “pleiotropia antagônica”, em que traços que aumentam a aptidão cedo na vida carregam custos ocultos mais tarde.
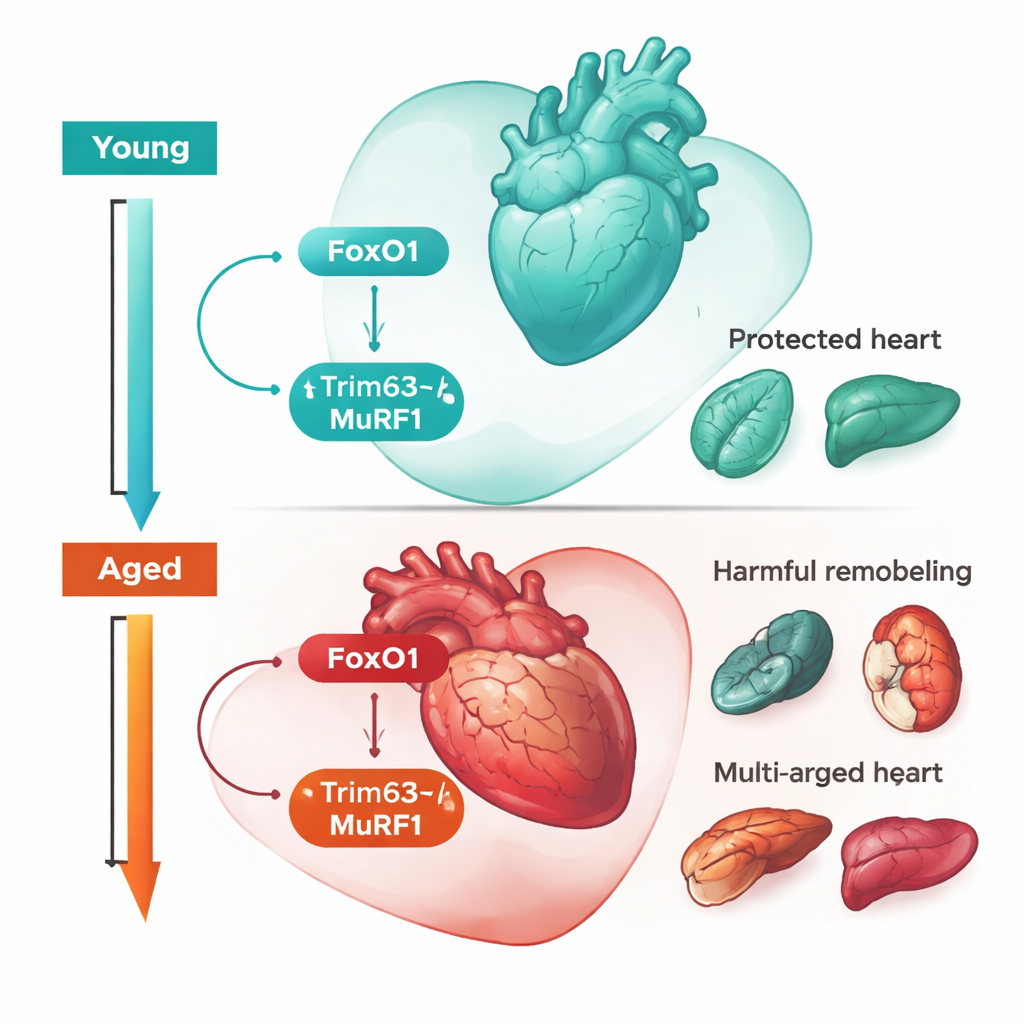
O que isso significa para tratar infecções ao longo da vida
Para um leitor leigo, a mensagem principal é que combater infecções graves como a sepse não se resume a matar germes — trata‑se também de como nossos órgãos resistem à tempestade. Este estudo mostra que a maquinaria de resposta ao estresse do coração, centrada em FoxO1 e Trim63, ajuda corpos jovens a tolerar a infecção, mas pode virar uma responsabilidade com a idade. Como resultado, um medicamento que bloqueia essa via pode salvar a vida de um paciente idoso enquanto seria perigoso para um mais jovem. O trabalho ressalta que terapias para doenças infecciosas podem precisar ser ajustadas conforme a idade, levando em conta que o mesmo gene pode ter duas faces: guardião na juventude, causador de problemas na velhice.
Citação: Sanchez, K.K., McCarville, J.L., Stengel, S.J. et al. Disease tolerance and infection pathogenesis age-related tradeoffs in mice. Nature 650, 727–735 (2026). https://doi.org/10.1038/s41586-025-09923-x
Palavras-chave: sepse, envelhecimento, tolerância à doença, remodelamento cardíaco, via FoxO1 Trim63