Clear Sky Science · pt
O estresse controla a herança da heterocromatina via ubiquitinação da histona H3
Como as Células Lembram do Estresse
Nossas células precisam de maneiras de “lembrar” estresses passados — como calor, falta de nutrientes ou exposição a medicamentos — para poderem responder mais rapidamente da próxima vez. Um sistema de memória poderoso depende da heterocromatina, DNA densamente compactado que mantém certos genes desligados por muitas divisões celulares. Este artigo explora como as células ajustam ativamente essa memória em resposta ao estresse, revelando um centro molecular que liga sinais ambientais a mudanças duradouras na atividade gênica. Entender esse sistema de controle pode ajudar a explicar como fungos evoluem resistência a medicamentos e como o estresse remodela o panorama epigenético de nossas próprias células.
Um Cadeado no Genoma
A heterocromatina pode ser vista como um cadeado molecular em trechos de DNA, mantendo genes próximos em silêncio. Esse cadeado é construído a partir de marcas químicas nas proteínas histonas, especialmente uma marca chamada H3K9me3. Uma vez estabelecida, ela pode se copiar a cada replicação do DNA, permitindo que padrões de repressão gênica sejam herdados sem alterar a sequência de DNA subjacente. Até agora, a maior parte do trabalho sugeria que essa autocópia depende principalmente de um ciclo de retroalimentação “ler–escrever”: um complexo enzimático reconhece as marcas H3K9me3 existentes e adiciona a mesma marca às histonas vizinhas, espalhando gradualmente o domínio silencioso. Mas esse modelo não explicava totalmente como condições ambientais aceleram, desaceleram ou redirecionam a propagação da heterocromatina.
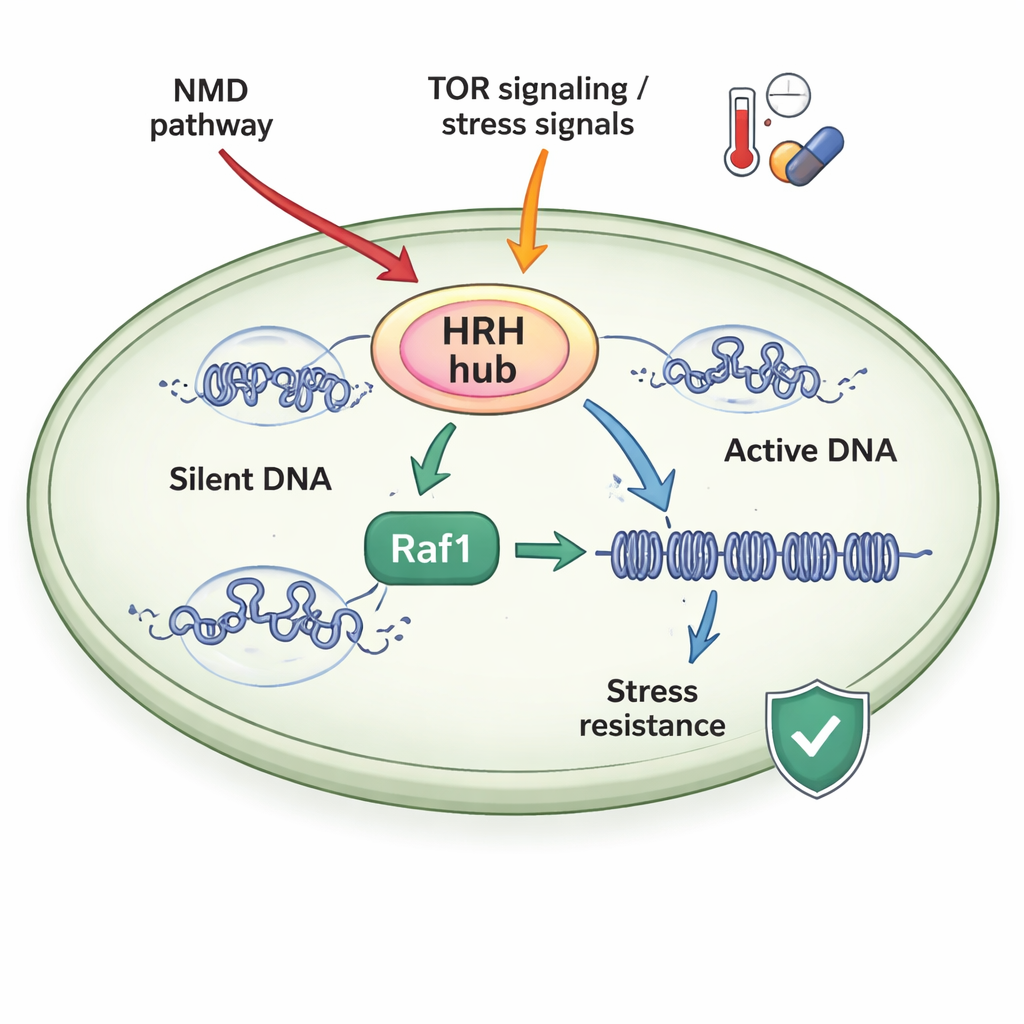
Um Centro de Controle Sensível ao Estresse
Os autores estudaram a levedura fission yeast, um organismo modelo simples cujo maquinário cromatínico se assemelha ao de organismos superiores. Eles se concentraram em um complexo chamado ClrC, que tanto escreve a marca H3K9me3 quanto anexa uma pequena proteína, ubiquitina, a outra posição na histona H3 (H3K14ub). Uma subunidade chave do ClrC, Raf1, age como um “porteiro” limitante: quando Raf1 é escasso, grande parte da principal enzima (Clr4) fica livre em vez de se juntar ao complexo na cromatina, e os domínios silenciosos deixam de se espalhar. Quando Raf1 é abundante, mais ClrC é montado e fixado de forma estável ao DNA, permitindo que as marcas H3K14ub e H3K9me3 se estendam ao longo dos cromossomos e reforcem o silenciamento gênico.
Ajustando o Cadeado com Ubiquitina
Ao mapear marcas de cromatina pelo genoma, a equipe mostrou que H3K14ub está fortemente enriquecida onde a heterocromatina se forma e que essa marca praticamente desaparece se Raf1 é removido. Quando as células carregam uma mutação que bloqueia a etapa de adição de ubiquitina (mantendo H3K9me3 intacta no ponto inicial), os domínios silenciosos são incapazes de se espalhar para fora. Em outras palavras, H3K14ub não é apenas decorativa; ela é necessária para empurrar a frente da heterocromatina adiante. Experimentos bioquímicos e de imagem revelam o porquê: H3K14ub aumenta muito a atividade da enzima Clr4 e ajuda a manter o complexo inteiro ancorado na cromatina, elevando a densidade local de H3K9me3 acima do limiar necessário para herança estável. Notavelmente, aumentar os níveis de Raf1 pode contornar vários outros fatores normalmente necessários para manter esses domínios silenciosos, enfatizando que a ubiquitinação dirigida por Raf1 é uma alavanca central de controle.
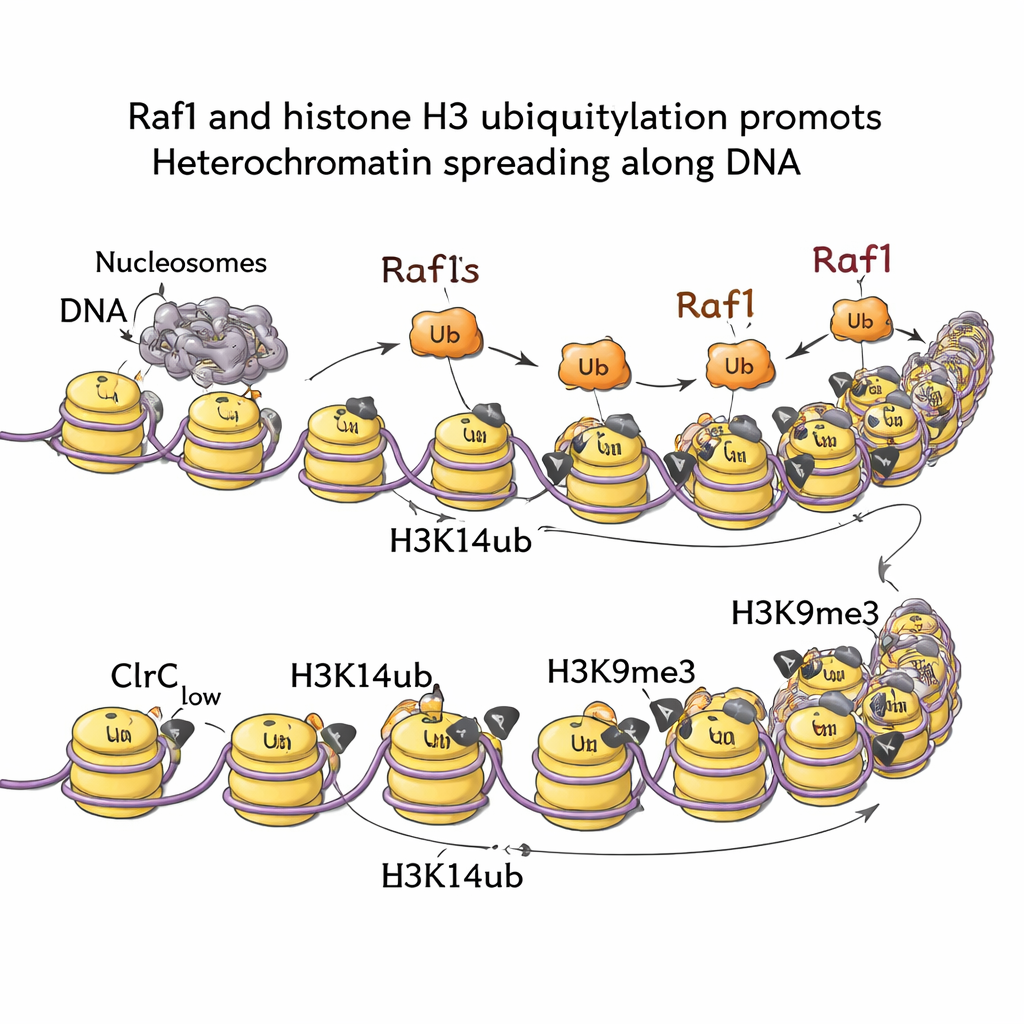
Sinais da Degradação de RNA e de Vias de Crescimento
As células não deixam os níveis de Raf1 ao acaso. O estudo mostra que dois grandes sistemas responsivos ao estresse alimentam o que os autores denominam de hub regulatório da herdabilidade da heterocromatina (HRH), centrado em Raf1. Primeiro, a via de degradação mediada por nonsense (NMD) — mais conhecida por destruir RNAs mensageiros defeituosos — tem como alvo o mensageiro que codifica Raf1, mantendo os níveis de Raf1 baixos em condições normais. Desabilitar a NMD estabiliza o RNA de Raf1, eleva a abundância da proteína Raf1 e restaura a propagação da heterocromatina em mutantes que, de outra forma, não conseguem manter domínios silenciosos. Em segundo lugar, um sensor de crescimento e estresse chamado TORC2, atuando por meio da quinase Gad8, promove a expressão de Raf1. Temperaturas altas desligam essa via, reduzindo os níveis de Raf1, enfraquecendo a heterocromatina e tornando mais difícil para as células manterem estados silenciosos, a menos que Raf1 seja experimentalmente aumentado.
Estresse, Resistência a Medicamentos e Implicações Mais Amplas
Os autores então conectam esse hub molecular à adaptação do mundo real. Expor leveduras à cafeína, um estresse também conhecido por atenuar a NMD em outros sistemas, eleva os níveis de Raf1 e potencializa a propagação da heterocromatina para novos locais, incluindo genes cujo silenciamento confere resistência à cafeína e a antifúngicos. Da mesma forma, células com níveis artificialmente elevados de Raf1 tornam‑se mais resistentes ao fluconazol e ao clotrimazol, antifúngicos comuns. Por outro lado, quando Raf1 é reduzido — pelo calor ou pela perda da sinalização TORC2–Gad8 — a heterocromatina torna‑se instável e a memória epigenética se esvai, a menos que Raf1 seja restaurado. Como proteínas semelhantes a Raf1, o complexo ClrC e a marca H3K14ub têm equivalentes em fungos patogênicos e em mamíferos, essas descobertas sugerem que um hub epigenético sensível ao estresse semelhante pode moldar resistência a medicamentos, desenvolvimento e doença em muitas espécies.
Por Que Isso Importa
Em termos cotidianos, este trabalho mostra que o silenciamento gênico pela cromatina não é um cadeado rígido, mas um sistema inteligente e ajustável. As células usam um hub central para ler sinais ambientais — mudanças de temperatura, estado nutricional, estresses químicos — e regular Raf1 para cima ou para baixo. Isso, por sua vez, governa quanto do genoma fica envolto em silêncio duradouro e quão facilmente as células podem “reprogramar” a si mesmas sem mutar seu DNA. Ao descobrir o papel-chave da ubiquitinação da histona H3 e da dosagem de Raf1 nesse processo, o estudo fornece um roteiro de como o estresse pode remodelar rapidamente o panorama epigenético — e sugere novas maneiras de influenciar a resistência a medicamentos em fungos ou o silenciamento gênico aberrante em doenças humanas.
Citação: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Palavras-chave: heterocromatina, herança epigenética, ubiquitinação de histonas, adaptação ao estresse, resistência fúngica a medicamentos