Clear Sky Science · pt
Resolvendo a integridade estrutural e farmacocinética de DNA origami in vivo
Observando minúsculas máquinas de DNA dentro do corpo
O DNA pode ser dobrado como papel em pequenas formas tridimensionais, uma técnica conhecida como DNA origami. Essas nanostruturas podem ser programadas para transportar medicamentos, vacinas ou moléculas sinalizadoras com precisão extrema. Mas, uma vez injetadas no corpo, elas permanecem intactas tempo suficiente para funcionar ou se desfazem rapidamente? Este artigo apresenta uma nova forma de observar essas máquinas de DNA em ação dentro de animais vivos, revelando quanto tempo sobrevivem, como se deslocam pela corrente sanguínea e até quais partes de cada estrutura se rompem primeiro.
Por que dobrar DNA pode mudar a medicina
O DNA origami aproveita as mesmas regras de pareamento de bases que armazenam nossa informação genética, mas as reorienta para construir objetos na escala nanométrica. Pesquisadores podem dispor proteínas, medicamentos ou sinais que estimulam o sistema imune sobre esses objetos como pinos em uma placa de Lego, criando terapias altamente controladas para câncer, doenças autoimunes e infecções. Para que tratamentos tão precisos sejam seguros e eficazes, reguladores e cientistas precisam saber quão intactas essas estruturas permanecem no corpo e com que rapidez são eliminadas—conhecido coletivamente como farmacocinética. Métodos de rastreamento existentes normalmente prendem corantes fluorescentes ou simplesmente contam fragmentos de DNA, o que pode fazer com que detritos desmontados pareçam nanostruturas totalmente intactas. Até agora, não havia uma maneira prática de dizer, em animais vivos, se as formas originais de DNA origami ainda estão inteiras.
Um “teste de integridade” molecular para DNA origami
A equipe desenvolveu um método que chama PLASTIQ, abreviação de proximity ligation assay for structural tracking and integrity quantification. A ideia chave é deixar o próprio DNA origami reportar seu estado. Em posições específicas de cada estrutura, os pesquisadores colocam pares de pequenos “staples” de DNA que ficam lado a lado ao longo de um hélice quando o origami está corretamente dobrado. Um de cada par carrega uma pequena etiqueta química que permite que sejam unidos enzimaticamente, ou ligados, mas somente se ainda estiverem mantidos próximos por uma fita de andaime intacta. Se a estrutura derreter, quebrar ou for degradada por enzimas, essas duas peças se afastam e não podem mais ser ligadas. Após a ligação, os pares unidos são amplificados usando reação em cadeia da polimerase padrão e quantificados por qPCR sensível ou sequenciamento, transformando a presença de segmentos locais intactos em sinais mensuráveis a partir de meros microlitros de sangue.
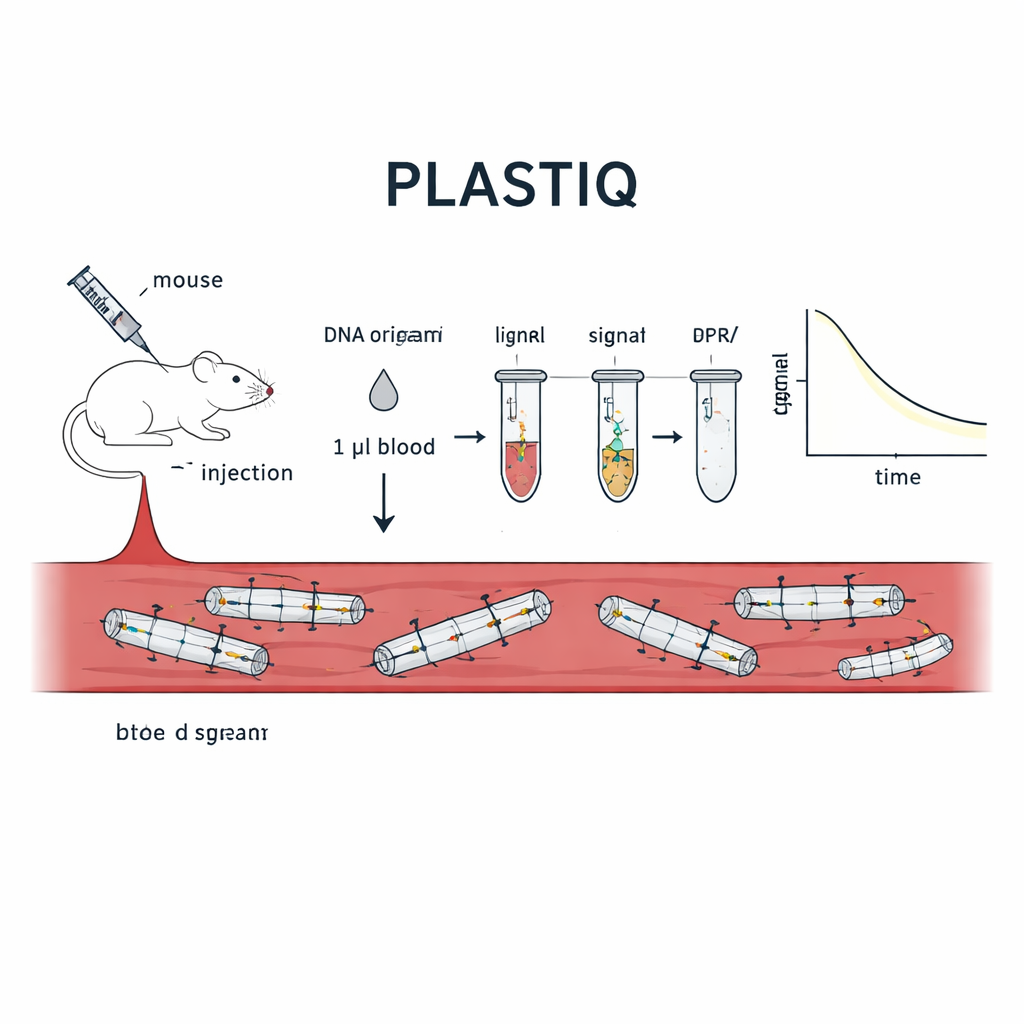
Colocando o teste em prática em camundongos vivos
Para provar que o PLASTIQ realmente mede integridade estrutural, os autores primeiro o aplicaram a designs simples de DNA origami em forma de bastão em tubos de ensaio. Os sinais apareceram apenas quando os bastões estavam intactos e desapareceram após o desdobramento induzido por calor, enquanto ensaios tradicionais baseados em DNA ainda registravam DNA independentemente da forma. Em seguida, injetaram esses bastões em camundongos por diferentes vias—diretamente na corrente sanguínea, na cavidade abdominal, no músculo e sob a pele—and coletaram apenas um microlitro de sangue em vários tempos. O PLASTIQ revelou como a concentração de estruturas intactas aumentava e depois caía, dependendo da via de injeção, correspondendo às expectativas gerais da farmacologia de fármacos, mas com detalhes estruturais muito mais finos. O método foi sensível até 0,01 femtomolar, exigindo quantidade mínima de sangue e permitindo amostragem repetida do mesmo animal ao longo de horas.
Testando revestimentos protetores e pontos fracos ocultos
Muitos grupos tentam proteger o DNA origami revestindo-o com polímeros como PEG, entrelaçando fitas com luz ultravioleta ou adicionando ligantes químicos, mas tem sido difícil avaliar quanto esses artifícios realmente ajudam in vivo. Usando o PLASTIQ, os autores mostraram que bastões revestidos com PEG na corrente sanguínea permanecem intactos um pouco mais tempo do que os nus, mas também são eliminados mais rapidamente uma vez na circulação, e que o revestimento não impede que as enzimas do PLASTIQ façam seu trabalho. Combinando o PLASTIQ com modelos matemáticos simples, eles extraíram taxas de absorção e eliminação para diferentes vias de injeção e revestimentos, e puderam até simular regimes de dosagem repetida. Foi levado adiante com um origami em forma de barril de dupla parede, mais densamente empacotado por dentro do que por fora. Medições PLASTIQ mostraram que os staples na superfície externa exposta perdiam integridade mais rápido do que os voltados para a cavidade interna, confirmando diretamente que hélices enterradas são protegidas das enzimas degradantes no sangue.
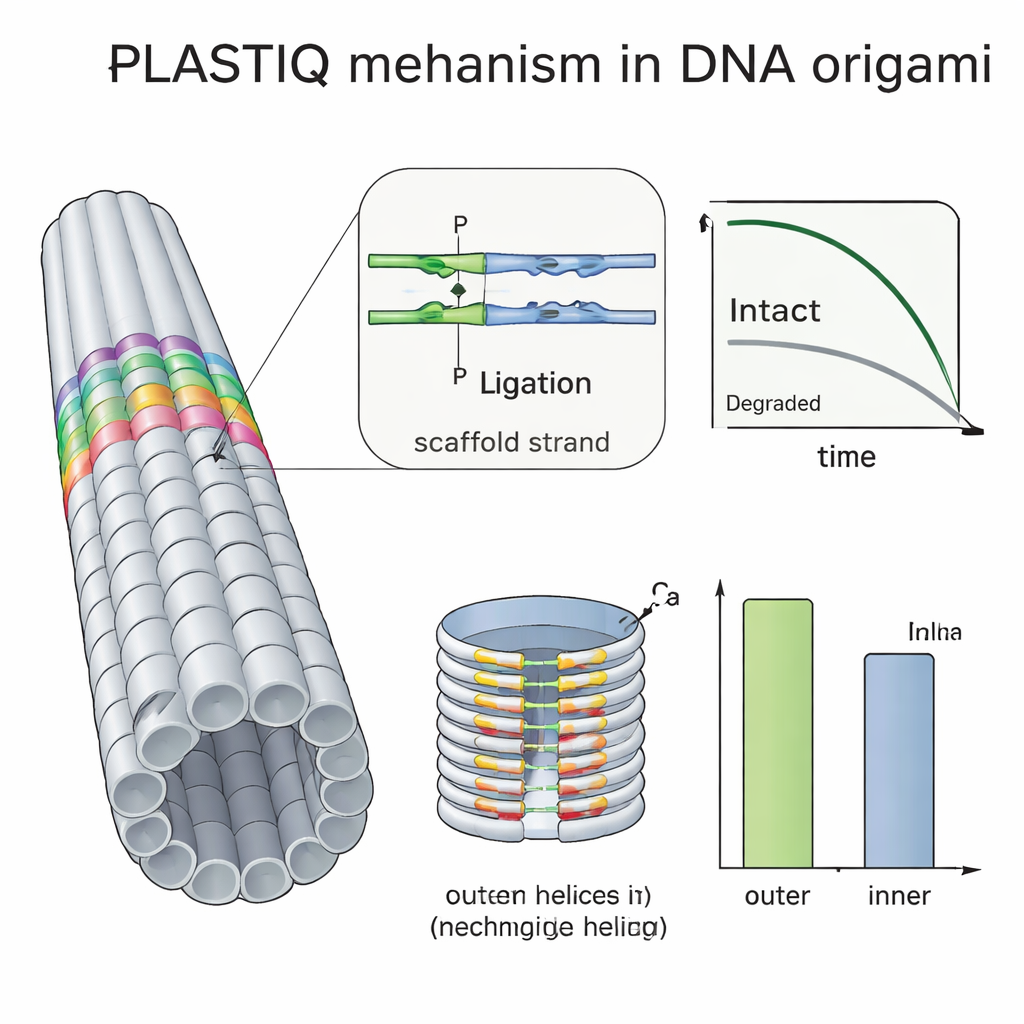
O que isso significa para futuras terapias à base de DNA
Para um não-especialista, o PLASTIQ pode ser visto como um check-up estrutural para dispositivos de DNA na escala nanométrica que viajam pelo corpo. Em vez de apenas perguntar “há DNA aqui?”, ele pergunta “esse DNA ainda está dobrado no objeto preciso que projetamos?”. Ao responder a essa pergunta com alta sensibilidade a partir de pequenas amostras de sangue, o PLASTIQ fornece aos desenvolvedores de fármacos uma forma de otimizar o projeto, o revestimento e a dosagem de medicamentos e vacinas baseados em DNA origami. Com o tempo, esse insight detalhado e quantitativo sobre como essas nanostruturas se comportam em ambientes biológicos reais pode ajudar a transformar o DNA origami de um conceito elegante de laboratório em terapêuticas confiáveis e prontas para regulação.
Citação: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Palavras-chave: DNA origami, nanomedicina, entrega de medicamentos, farmacocinética, nanotecnologia