Clear Sky Science · pt
A perturbação da triptofananase promove mutualismo inseto–bactéria
Como pequenos parceiros intestinais podem fazer ou destruir um inseto
Muitos animais, incluindo humanos, dependem de trilhões de micróbios que vivem em seus intestinos. Esses parceiros ocultos podem ajudar a digerir alimentos, produzir vitaminas ou, em alguns casos, nos adoecer. Este estudo examina uma alteração genética simples, porém surpreendente, em bactérias que transforma um microbe comum em um parceiro que salva a vida de uma percevejo que se alimenta de plantas. Ao focalizar um único gene bacteriano, o trabalho revela como uma mudança microscópica pode dar início a uma amizade estável entre formas de vida muito diferentes.
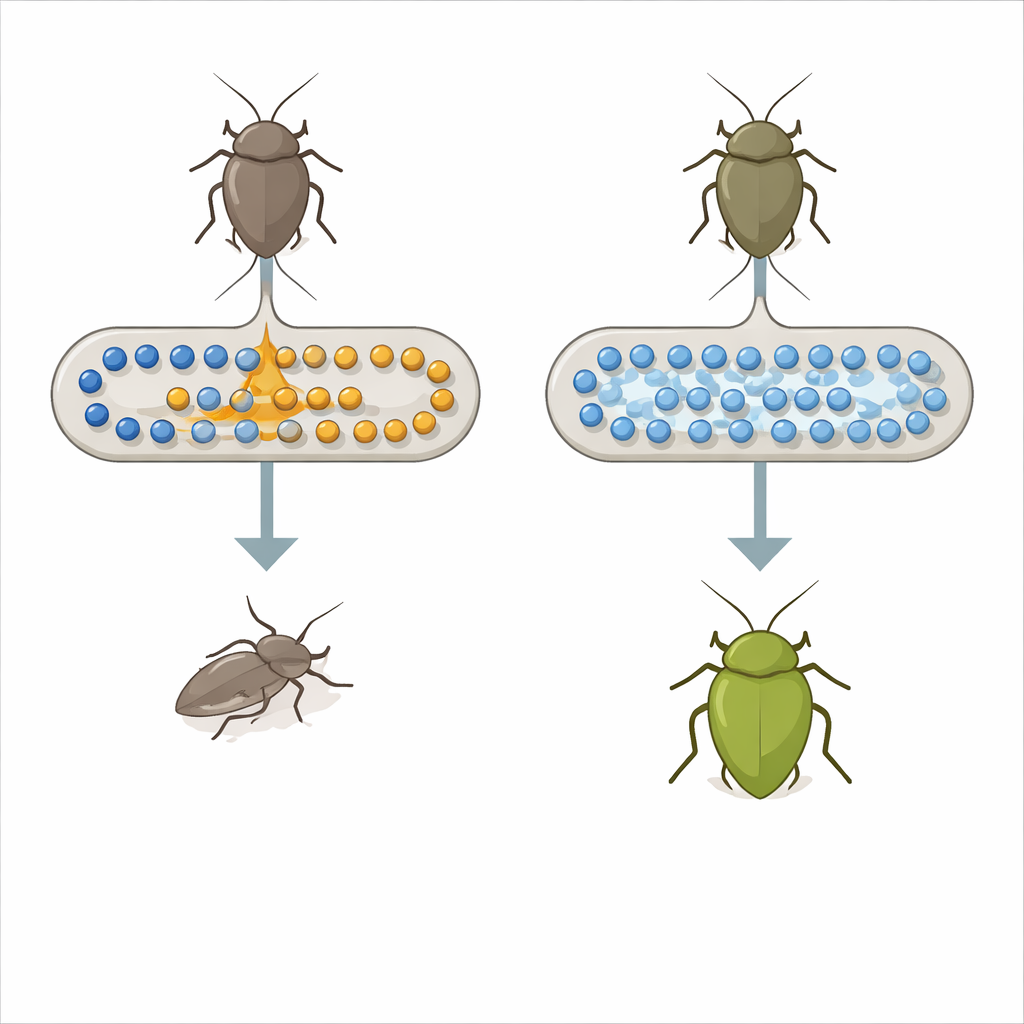
Um percevejo, uma bactéria e uma aliança improvável
O percevejo Plautia stali depende de bactérias especiais que vivem em uma bolsa do intestino médio para crescer e sobreviver. Na natureza, esses parceiros costumam ser membros do gênero Pantoea, que fornecem nutrientes que o inseto não consegue obter apenas da seiva das plantas. Trabalhos de laboratório já haviam mostrado que uma estirpe comum de laboratório de Escherichia coli, uma bactéria típica do intestino de mamíferos, pode rapidamente evoluir para um parceiro útil desse percevejo após uma única mutação em um sistema global de controle chamado repressão catabólica de carbono. Essa descoberta anterior levantou uma grande questão: será que uma mudança regulatória tão drástica é realmente como surgem simbioses úteis na natureza, ou existe um interruptor genético mais focado em ação?
Seguindo o rastro de um único bloco construtor
Para responder, os pesquisadores compararam percevejos que carregavam E. coli comum com aqueles que hospedavam mutantes evoluídos e benéficos de E. coli. Eles mediraram muitas pequenas moléculas no sangue e no intestino dos insetos. Um aminoácido essencial, o triptofano, destacou‑se: seus níveis foram mais de dez vezes maiores em insetos que hospedavam os mutantes úteis do que naqueles com E. coli normal. Entre dezenas de genes bacterianos afetados pela mutação regulatória anterior, dois estavam ligados ao processamento do triptofano. Um, chamado tnaA, produz uma enzima que decompõe o triptofano em um composto chamado indol, além de outros subprodutos; o outro ajuda a transportar o triptofano para dentro da célula. Quando a equipe deletou o gene tnaA de E. coli, os percevejos de repente se saíram muito melhor, com maior sobrevivência e uma cor corporal verde intensa característica de insetos saudáveis e bem nutridos.
Quando menos destruição significa mais ajuda
A mudança chave não se revelou no sentido de que as bactérias passassem a produzir mais triptofano, mas que elas deixaram de destruí‑lo e de produzir indol em excesso. Insetos que carregavam E. coli deficientes em tnaA apresentaram alto triptofano e quase nenhum indol circulando em seus corpos. Em contraste, insetos com E. coli normal tinham baixo triptofano e muito mais indol. Experimentos de alimentação sustentaram esse quadro: fornecer indol na água de beber prejudicou os insetos, especialmente aqueles com bactérias produtoras de indol, enquanto triptofano extra foi prejudicial apenas quando as bactérias podiam convertê‑lo em mais indol. Uma estirpe separada de E. coli, projetada para superproduzir triptofano, deu aos percevejos um impulso modesto, reforçando a ideia de que mais desse bloco construtor, e menos produto de degradação tóxico, melhora a saúde do inseto.
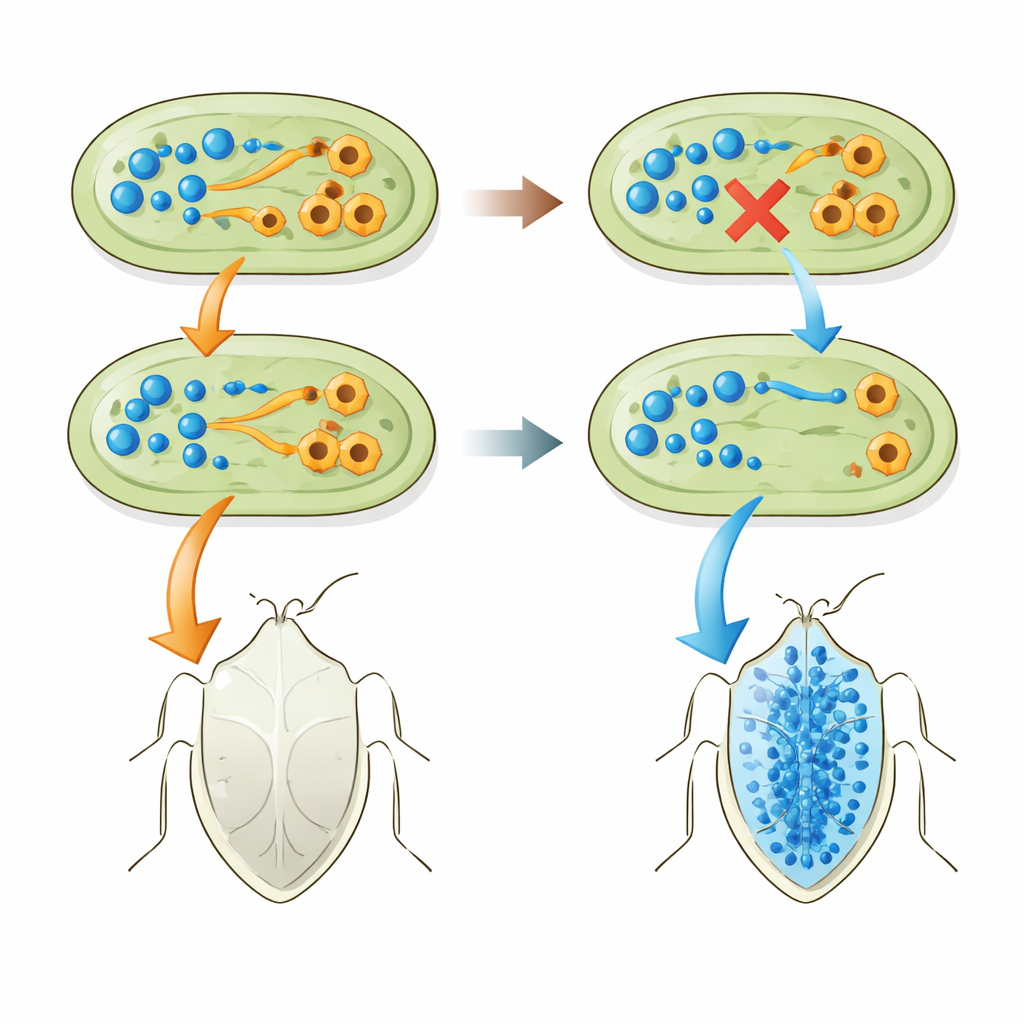
Parceiros naturais compartilham a mesma perda genética
A equipe então perguntou se essa mesma perda de gene aparece em simbioses do mundo real. Eles sequenciaram genomas de muitas bactérias Pantoea que vivem dentro de P. stali e percevejos relacionados pelas Ilhas Ryukyu, no Japão, bem como cepas de Pantoea isoladas do solo que podiam ser induzidas a ajudar os percevejos. De forma marcante, todo simbionte bem‑sucedido ou potencialmente bem‑sucedido carecia do gene tnaA e não mostrou atividade da enzima que quebra o triptofano. Em contraste, várias cepas de Pantoea ananatis de vida livre que ainda carregavam tnaA não conseguiam sustentar o desenvolvimento dos percevejos. Quando os pesquisadores nocauteavam tnaA em uma dessas cepas de P. ananatis, sua capacidade de ajudar os insetos melhorou, embora não atingisse o nível dos parceiros naturais. E quando forçaram um simbionte natural a carregar um operon tnaA ativo, os insetos se saíram pior e apresentaram menor triptofano e maior indol no sangue.
O que isso significa para as parcerias ocultas da vida
Em conjunto, os resultados apontam para uma regra simples, porém poderosa: bactérias que deixam de quebrar o triptofano, e assim evitam inundar seu hospedeiro com indol, têm mais probabilidade de se tornar parceiras confiáveis para percevejos que se alimentam de plantas. Em laboratório, isso pode ser desencadeado por uma mutação em um sistema regulatório global; na natureza, manifesta‑se como uma perda direta do próprio gene que cliva o triptofano. De qualquer forma, desligar essa única enzima ajuda a alinhar os interesses do inseto e do microbo. O estudo sugere que o caminho de uma associação frouxa para um mutualismo estreito pode, às vezes, depender de passos genéticos surpreendentemente pequenos, e que perdas de função semelhantes no metabolismo bacteriano podem estar por trás de muitas outras alianças ocultas pela árvore da vida.
Citação: Wang, Y., Moriyama, M., Koga, R. et al. Tryptophanase disruption promotes insect–bacterium mutualism. Nat Microbiol 11, 759–769 (2026). https://doi.org/10.1038/s41564-026-02264-z
Palavras-chave: microbioma de insetos, mutualismo bacteriano, metabolismo do triptofano, evolução da simbiose, simbiotos do Pantoea