Clear Sky Science · pt
Vacinação com mRNA supera o prejuízo mediado por hemozoína em vacinas antimaláricas de parasita inteiro em camundongos
Por que malária prévia reduz a eficácia das vacinas
A malária mata centenas de milhares de pessoas todo ano, e uma das vacinas mais promissoras usa parasitas inteiros enfraquecidos para treinar o sistema imunológico. Ainda assim, curiosamente, essa abordagem “padrão-ouro” funciona muito melhor em pessoas que nunca tiveram malária do que naquelas que cresceram em regiões onde a doença é comum. Este estudo, feito em camundongos, faz uma pergunta simples mas crucial: o que há nas infecções anteriores por malária que faz com que uma vacina altamente eficaz falhe — e uma nova vacina à base de mRNA pode resolver o problema?
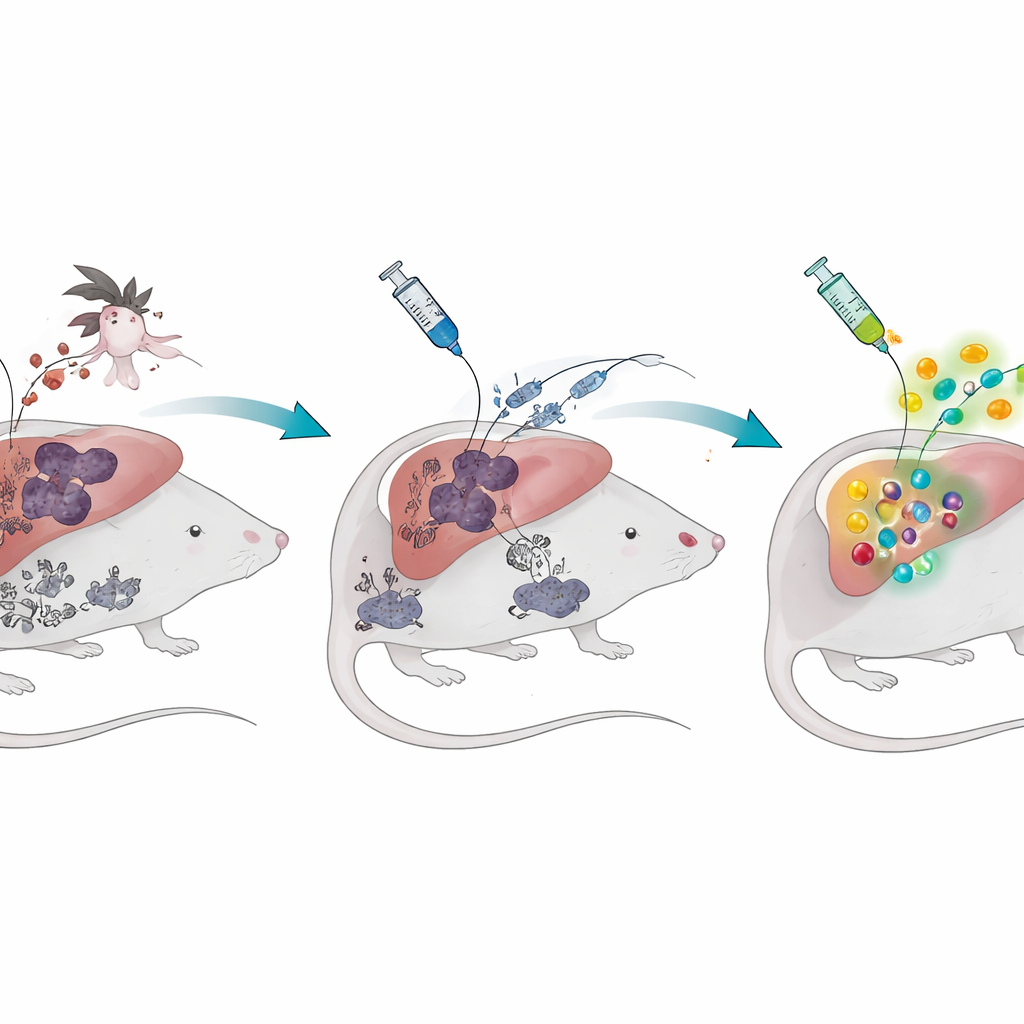
Uma história de dois estágios da malária
O parasita da malária tem dois estágios principais no organismo humano. Primeiro, após a picada de um mosquito, infecta silenciosamente o fígado. Depois, invade os glóbulos vermelhos, causando febre e doença. Vacinas de parasita inteiro chamadas esporozoítos atenuados por radiação têm como alvo o estágio silencioso no fígado: os parasitas entram nas células hepáticas, mas não conseguem completar seu ciclo de vida, oferecendo ao sistema imunológico uma prévia segura. Em camundongos sem exposição prévia à malária, essa estratégia gera grande número de células T citotóxicas especializadas que se instalam no fígado e podem eliminar os parasitas antes que causem doença. Mas quando os pesquisadores primeiro submeteram camundongos a uma infecção em estágio sanguíneo e a deixaram se resolver, a mesma vacina produziu muito menos células T protetoras, e os animais ficaram muito menos protegidos quando desafiados com parasitas vivos.
Um pigmento persistente que não desaparece
A equipe então investigou o que era diferente nesses camundongos “com experiência em malária”. Um suspeito destacado foi a hemozoína, um pigmento escuro em forma de cristal que o parasita forma dentro dos glóbulos vermelhos para detoxificar os resíduos ricos em ferro da digestão da hemoglobina. Esse pigmento não desaparece quando a infecção é resolvida; pode permanecer no fígado, baço e medula óssea por muitos meses. Os cientistas descobriram que, mesmo mais de um ano após o fim de uma infecção em estágio sanguíneo, os camundongos ainda apresentavam hemozoína armazenada e uma resposta de células T enfraquecida ao vacino contra o estágio hepático. Administrar hemozoína sintética purificada a camundongos saudáveis — sem quaisquer parasitas vivos — foi suficiente para imitar essa fraqueza vacinal de longa duração e reduzir a proteção contra um desafio malárico posterior.
Como a hemozoína atrapalha os sentinelas imunológicos
Aprofundando, os pesquisadores focaram nas células dendríticas, os sentinelas do sistema imunológico que capturam fragmentos de patógenos e os apresentam às células T. Para que a vacina de parasita inteiro contra o fígado funcione, as células dendríticas devem capturar material do parasita proveniente de células hepáticas infectadas e mostrá-lo às células T citotóxicas. Em experimentos em cultura celular, a equipe demonstrou que a hemozoína interfere diretamente nessa etapa de captação: quanto mais as células dendríticas tinham sido expostas à hemozoína, menos eficientemente englobavam antígenos proteicos. Esse defeito apareceu tanto em células de camundongo quanto em células imunológicas humanas derivadas de doadores de sangue, e não dependia de um sensor inflamatório bem conhecido, sugerindo que a hemozoína age como um bloqueio físico ou bioquímico ao manuseio normal de antígenos.
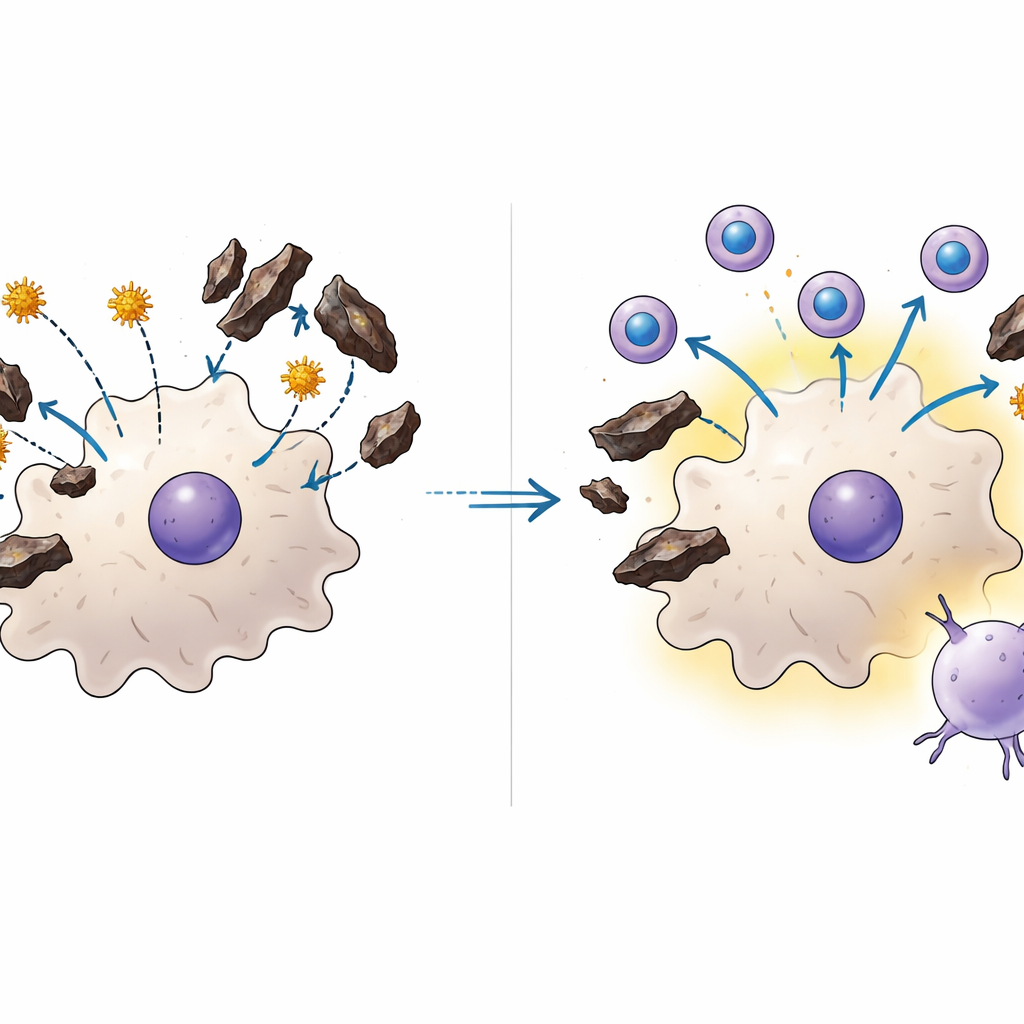
Vacinas de mRNA contornam o bloqueio
Para ver se um formato vacinal diferente poderia evitar esse problema, os cientistas projetaram uma vacina de mRNA encapsulada em nanopartículas lipídicas. Em vez de fornecer proteínas do parasita externamente, essa abordagem entrega às células do hospedeiro instruções genéticas para produzir dentro da célula pequenos trechos de várias proteínas do parasita. Em camundongos com ou sem malária prévia, a vacina de mRNA gerou respostas robustas de células T citotóxicas e melhor controle da infecção hepática. Surpreendentemente, quando a vacina de mRNA foi combinada com uma dose única da vacina de parasita inteiro contra o fígado, os camundongos desenvolveram pools especialmente grandes de células T que passaram a residir a longo prazo no fígado — uma população celular conhecida por ser chave para proteção rápida. Em cultivos, a hemozoína não bloqueou a captação nem a função das nanopartículas carregadas com mRNA, explicando como essa estratégia pode ter sucesso onde a vacina antiga sozinha falha.
O que isso significa para futuras vacinas contra malária
Em termos práticos, o estudo mostra que infecções anteriores por malária deixam detritos microscópicos semelhantes a minerais que entopem a forma como certas células imunológicas normalmente aprendem com vacinas, enfraquecendo uma das principais vacinas de parasita inteiro contra a malária. Mas, ao mudar para, ou combinar com, uma vacina baseada em mRNA que entrega as instruções para trechos do parasita diretamente às células, os cientistas podem contornar esses detritos e restaurar proteção forte em hospedeiros com experiência em malária — ao menos em camundongos. O trabalho aponta a hemozoína como um obstáculo importante para vacinas em pessoas que vivem em regiões endêmicas e sugere que regimes vacinais de mRNA ou mistos cuidadosamente projetados podem ser um caminho promissor rumo a uma imunização antimalárica mais eficaz e amplamente útil.
Citação: Hassert, M., Drewry, L.L., Pewe, L.L. et al. mRNA vaccination overcomes haemozoin-mediated impairment of whole-parasite malaria vaccines in mice. Nat Microbiol 11, 718–730 (2026). https://doi.org/10.1038/s41564-026-02263-0
Palavras-chave: vacinas contra malária, hemozoína, vacina de mRNA, imunidade por células T, infecção por Plasmodium