Clear Sky Science · pt
Análise comparativa de conjuntos de dados de varredura mutacional profunda em enterovírus A e B identifica divergência funcional e alvos terapêuticos
Por que vírus de RNA minúsculos importam para nós
Enterovírus constituem um grande grupo de vírus de RNA minúsculos que circulam silenciosamente pelo mundo, geralmente causando resfriados leves ou gastroenterites, mas às vezes desencadeando paralisia, danos cardíacos ou outras doenças graves. Temos poucas vacinas e ainda menos medicamentos que atuem de forma ampla contra eles, em parte porque esses vírus evoluem muito rápido. Este estudo investiga uma pergunta aparentemente simples, porém de grande importância prática: quando esses vírus mutam, quais partes de sua maquinaria podem mudar livremente e quais partes são tão vitais que a evolução as mantém quase imóveis? As respostas apontam para novas estratégias de projetar tratamentos que o vírus tenha dificuldade em driblar.
Lendo o manual do vírus, uma mutação de cada vez
Os pesquisadores se concentraram em dois enterovírus humanos que causam doenças muito diferentes: Enterovírus A71, associado a doenças neurológicas graves em crianças, e coxsackievírus B3, relacionado à inflamação cardíaca e até câncer pancreático. Usando uma técnica chamada varredura mutacional profunda, eles criaram bibliotecas virais nas quais quase todas as posições nas proteínas de cada vírus foram alteradas sistematicamente. Esses vírus mutantes foram então permitidos infectar células em cultura, e o sequenciamento de alto rendimento foi usado para medir como cada alteração afetou o crescimento viral. Comparando cada mutante com o vírus original, a equipe construiu um mapa detalhado de quais sítios no proteoma viral toleram mudanças e quais são fortemente restritos. 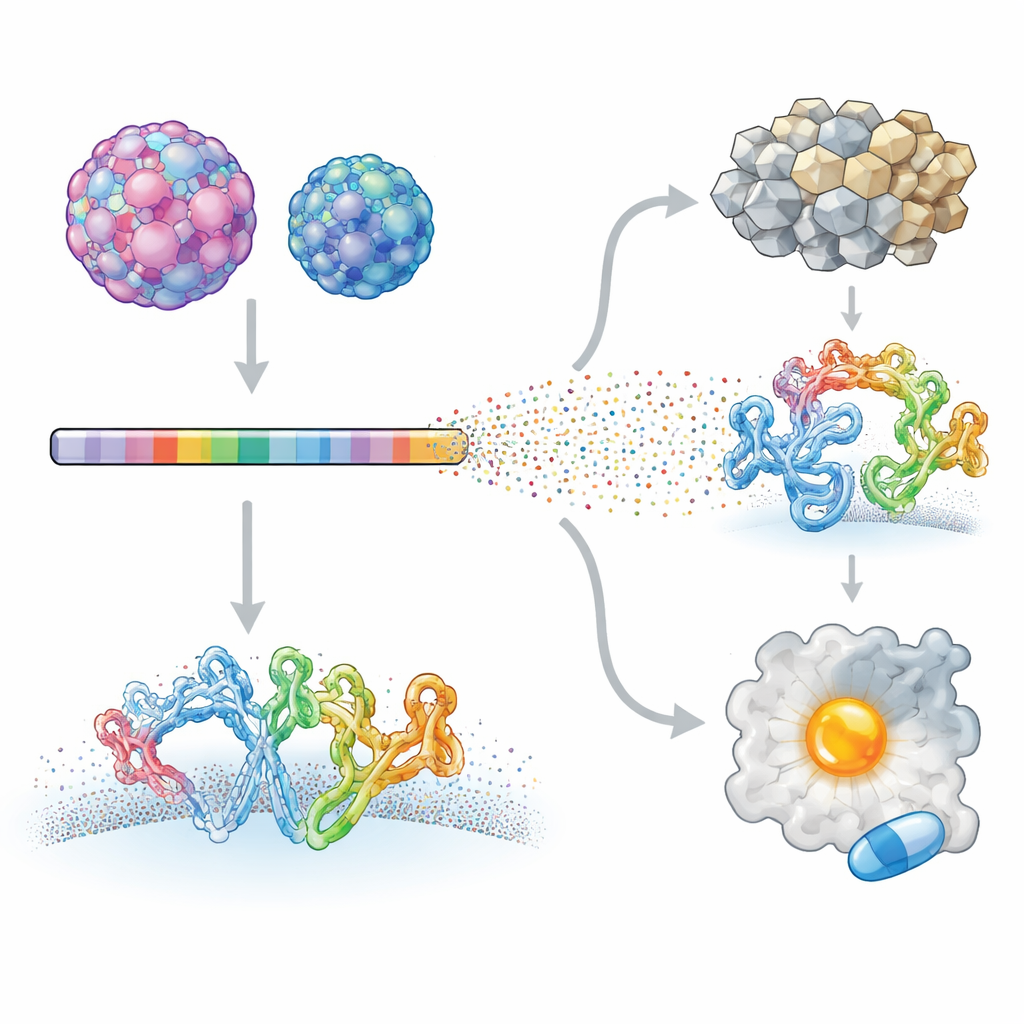
Limites rígidos compartilhados e flexibilidade específica do vírus
Apesar de compartilharem apenas cerca de metade de suas sequências de aminoácidos, os dois vírus mostraram padrões gerais de restrição surpreendentemente semelhantes. As “potências de trabalho” enzimáticas internas que copiam o genoma, cortam proteínas virais e desenrolam RNA foram altamente sensíveis à mutação em ambos os vírus. Da mesma forma, as superfícies internas que mantêm a casca proteica, ou capsídeo, unida mostraram ser difíceis de alterar sem comprometer o vírus. Em contraste, muitas regiões voltadas para fora e que interagem com o hospedeiro foram mais livres para mudar e frequentemente diferiram nitidamente entre as duas espécies. A análise estrutural mostrou que regiões conservadas e intolerantes a mutações se agruparam em torno de sítios ativos e interfaces de montagem, enquanto regiões que tocam receptores, membranas ou moléculas imunes do hospedeiro foram pontos quentes de flexibilidade específica por espécie.
Como os vírus encontram células e driblam defesas
A equipe então ampliou o foco para o aperto molecular entre vírus e hospedeiro. Enterovírus A71 e coxsackievírus B3 usam receptores celulares diferentes para entrar, e o estudo constatou que as pegadas de contato exatas na superfície do capsídeo estão entre as regiões mais divergentes em termos de tolerância à mutação. Resíduos que agarram o receptor para um vírus são fortemente restritos nesse vírus, mas relativamente permissivos no outro, refletindo como cada um afinou sua plataforma de acoplamento. Divergência semelhante surgiu em uma pequena proteína ligada à membrana chamada 3A, que ajuda a remodelar membranas celulares e recrutar fatores do hospedeiro para a replicação do genoma. Modelagem sugeriu que os dois vírus usam parciais diferentes de contato na 3A para engajar o mesmo fator do hospedeiro, GBF1, e podem também inserir essa proteína nas membranas em profundidades distintas. Essas diferenças ajudam a explicar por que vírus intimamente relacionados podem infectar tecidos diferentes e provocar padrões de doença distintos.
O que a evolução em laboratório perde — e o que ela acerta
Para situar seus experimentos em cultura celular no contexto do mundo real, os autores compararam seus mapas de mutação com milhares de sequências virais naturais obtidas de amostras de pacientes. No geral, sítios que foram flexíveis no laboratório tendiam também a ser variáveis na natureza, especialmente em comparações mais amplas ao nível de espécie. Entretanto, ao examinar quais aminoácidos específicos eram preferidos em cada sítio, a evolução natural e a seleção em laboratório concordaram mais estreitamente dentro de um único tipo viral. Notavelmente, os maiores desalinhamentos se aglomeraram na superfície externa do capsídeo e em regiões que interagem com o hospedeiro nas proteínas não estruturais 2A e 3A — exatamente onde respostas imunes e ambientes hospedeiros complexos tendem a importar mais. Isso sugere que a varredura mutacional profunda captura as restrições mecânicas básicas das proteínas virais, enquanto infecções reais sobrepõem pressões adicionais da imunidade e do tropismo tecidual que são mais difíceis de reproduzir in vitro.
Encontrando um ponto fraco compartilhado para futuros fármacos
Por fim, os pesquisadores perguntaram se esses mapas poderiam destacar um calcanhar de Aquiles comum para o desenvolvimento de fármacos. Usando ferramentas computacionais, eles buscaram em ambos os vírus bolsões na superfície das proteínas que pudessem, em princípio, ligar pequenas moléculas. Em seguida, sobrepuseram os dados mutacionais para ver quais bolsões eram formados por resíduos que o vírus não pode facilmente mudar sem se prejudicar. Um bolsão, localizado na helicase 2C — um motor em formato de anel que ajuda a desenrolar o RNA viral — destacou-se. Sua forma e resíduos constituintes são altamente conservados em quatro grandes espécies humanas de enterovírus, fica afastado de sítios ativos já conhecidos, e alterações ali são raras na natureza e fortemente deletérias em testes de laboratório. 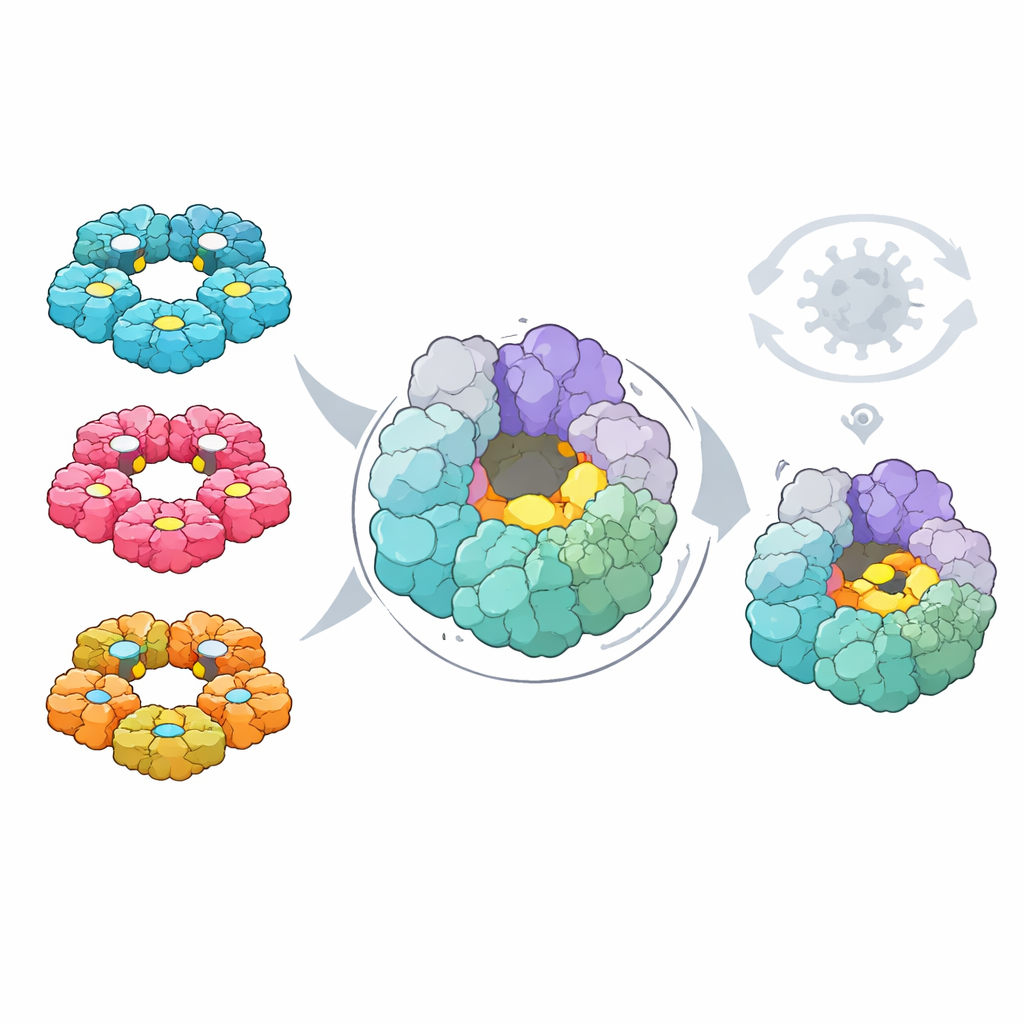
O que isso significa para tratamentos futuros
Ao sondar sistematicamente como cada possível alteração de uma só letra afeta dois enterovírus importantes, este estudo revela uma divisão clara entre um núcleo compartilhado e rígido da maquinaria viral e interfaces mais flexíveis e específicas ao hospedeiro. O núcleo conservado inclui um bolsão recém-destacado na helicase 2C que parece difícil para o vírus mutar sem perder aptidão, tornando-o um alvo atraente para antivirais de amplo espectro com alta barreira à resistência. Ao mesmo tempo, as superfícies externas mais adaptáveis e os sítios de contato com o hospedeiro explicam por que vírus relacionados se comportam de forma tão diferente no organismo e apontam onde vacinas e terapias baseadas na resposta imune devem lidar com evolução rápida. Em conjunto, essas descobertas fornecem um roteiro para projetar tratamentos que explorem os próprios limites evolutivos do vírus.
Citação: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Palavras-chave: enterovírus, evolução viral, varredura mutacional profunda, alvos antivirais, helicase 2C