Clear Sky Science · pt
Pseudo-produtos naturais monovalentes supercarregam a degradação de IDO1 pelo seu E3 nativo KLHDC3
Desligando uma Enzima Favorável ao Câncer
Nosso sistema imunológico patrulha constantemente em busca de células cancerosas, mas os tumores frequentemente reagem sequestrando a própria química do corpo. Um ator-chave nessa disputa é uma enzima chamada IDO1, que ajuda os tumores a desarmar as células imunes. Este estudo descreve uma nova classe de pequenas moléculas que faz mais do que apenas bloquear a atividade de IDO1 — ela convence as células a se livrar da enzima por completo. Ao aproveitar a maquinaria celular natural de descarte, esses compostos podem reavivar ataques imunes aos tumores de maneiras que drogas mais antigas não conseguiram.
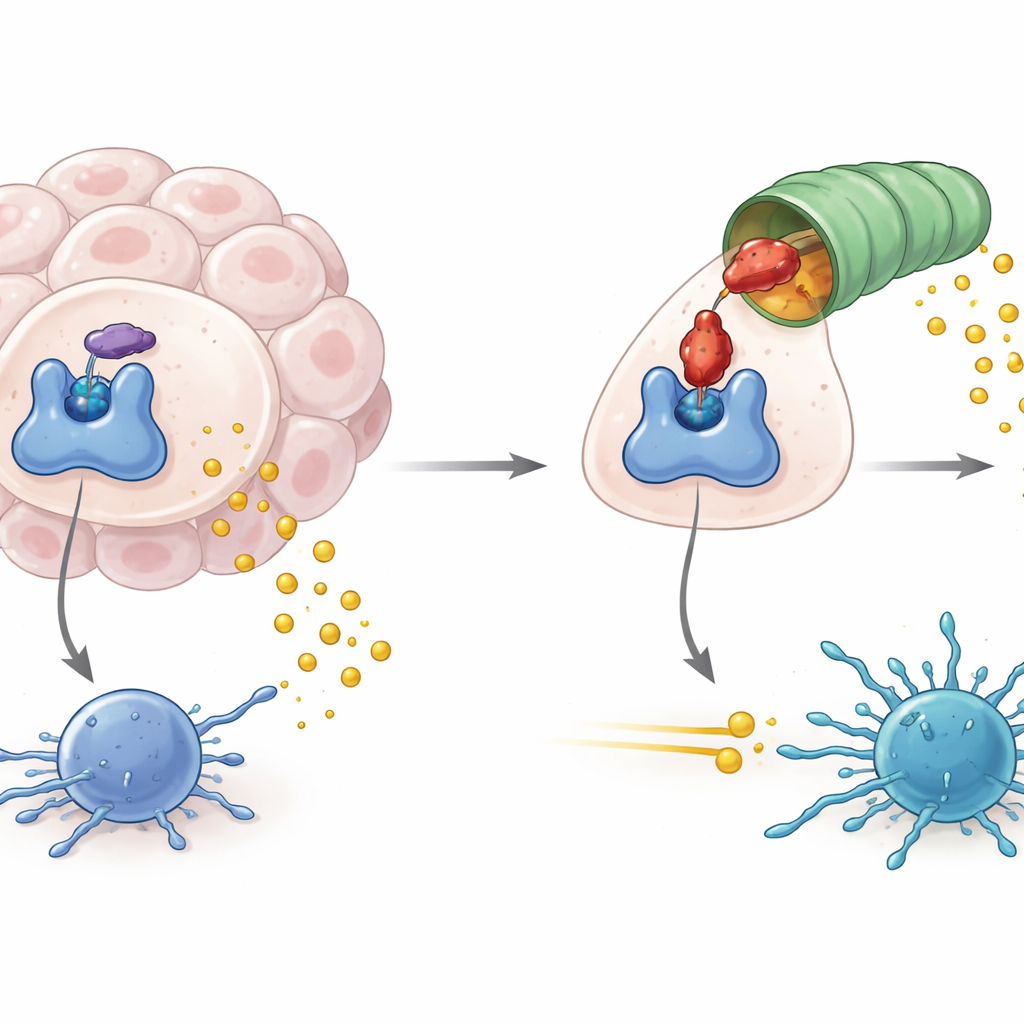
Como os Tumores Exploram um Guardião Metabólico
IDO1 fica na porta de entrada de uma via metabólica que degrada o aminoácido triptofano em um produto chamado quinurenina. Quando IDO1 está abundante e ativo, os níveis de triptofano caem e a quinurenina aumenta, criando um ambiente químico que reduz a atividade das células imunes, incluindo os linfócitos T que combatem tumores. Alta atividade de IDO1 tem sido associada não apenas a uma imunidade antitumoral mais fraca, mas também a linfomas induzidos por vírus e a algumas formas de neurodegeneração. Por isso, desenvolvedores de fármacos têm focado em bloquear a atividade enzimática de IDO1, na esperança de cortar esse sinal imunossupressor e ajudar as imunoterapias contra o câncer já existentes a funcionarem melhor.
Por Que Bloqueadores Enzimáticos Simples Falharam
Apesar de resultados promissores em animais, ensaios clínicos de inibidores tradicionais de IDO1 foram decepcionantes. Uma explicação emergente é que IDO1 é mais do que um catalisador simples. Mesmo quando sua química é bloqueada, a própria proteína pode atuar como um centro de sinalização que continua a promover o crescimento e a disseminação tumoral. Alguns inibidores até estabilizam IDO1, aumentando a quantidade da proteína presente nas células. Em outras palavras, desligar apenas a função catalítica pode deixar intocados os papéis pró-tumorais não enzimáticos — ou, pior, pode fortalecê-los.
Projetando Compostos que Disparam a Autodestruição
Os autores vasculharam uma grande biblioteca de moléculas “pseudo-naturais” — compostos sintéticos construídos a partir de fragmentos inspirados em produtos naturais, mas recombinados de novas maneiras. Eles encontraram uma família de moléculas, apelidada de iDegs, derivada de um bloco construtor do tipo vegetal chamado (−)-myrtanol. Esses compostos se ligam dentro do bolso habitual de IDO1 para seu cofator contendo ferro, o heme. Ao deslocar o heme, os iDegs tanto enfraquecem a capacidade de IDO1 de produzir quinurenina quanto, crucialmente, remodelam parte da região terminal da proteína. Estruturas cristalinas de alta resolução revelam que, quando os iDegs ocupam o sítio do heme, eles afrouxam e desordenam parcialmente uma hélice C-terminal que normalmente é mantida em uma conformação compacta e protegida.
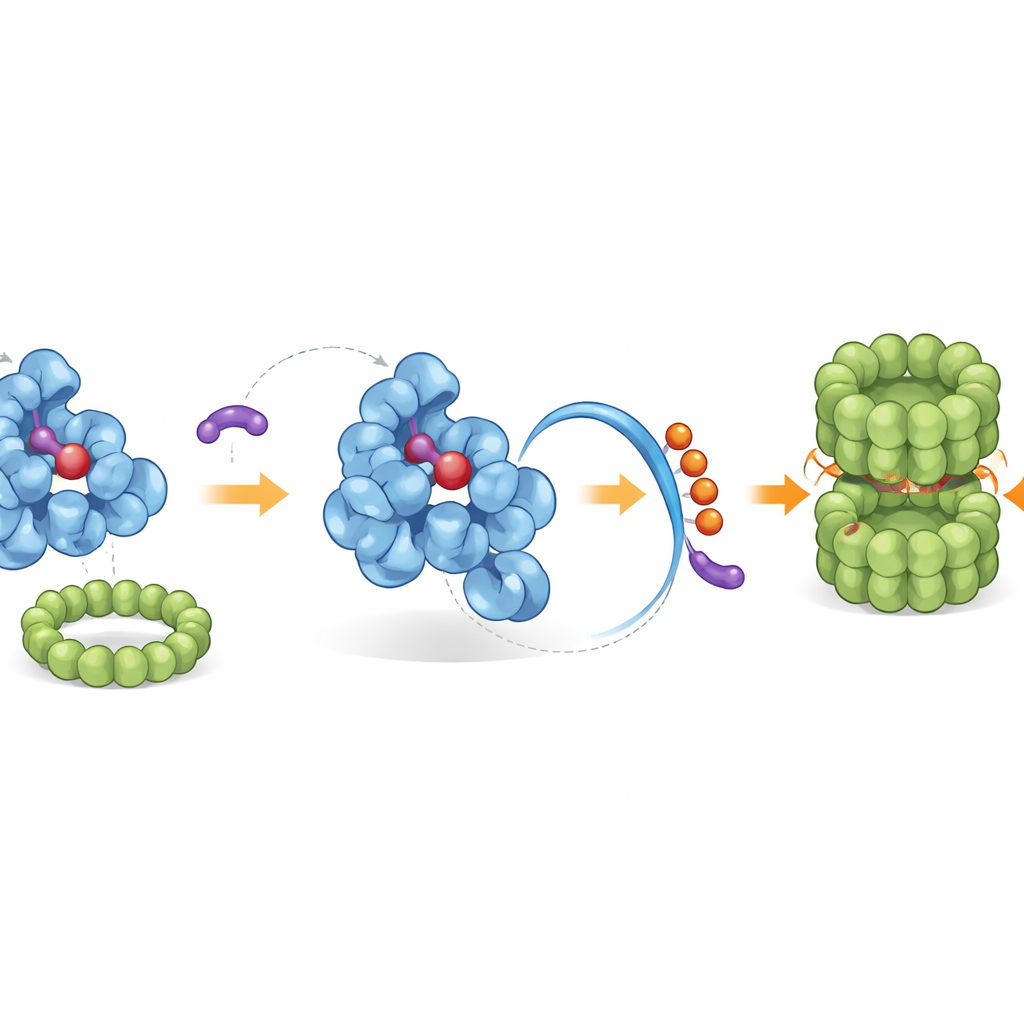
Recrutando a Equipe de Limpeza Nativa da Célula
A cauda reconfigurada expõe uma “etiqueta final” embutida que a maquinaria de descarte celular reconhece. Usando telas genéticas e reconstituição bioquímica, os pesquisadores identificaram um complexo de ligase específico, chamado CRL2–KLHDC3, que naturalmente anexa pequenas “bandeiras” de ubiquitina à cauda exposta de IDO1, marcando-a para destruição pelo proteassoma — o triturador molecular da célula. Em condições normais, apenas a forma de IDO1 livre de heme é marcada de forma eficiente dessa maneira, enquanto a forma ligada ao heme é protegida. Os iDegs puxam esse equilíbrio ao se ligarem apenas à forma sem heme, amplificando a via natural de degradação. Membros potentes da série não apenas bloqueiam a produção de quinurenina, mas também aumentam a marcação por ubiquitina em IDO1 e reduzem acentuadamente seus níveis proteicos em vários tipos de células cancerosas.
Mudando o Destino de IDO1 — e as Respostas Imunes
Esse comportamento de dupla ação tem consequências funcionais importantes. Em ensaios de migração com células de câncer de ovário, um inibidor de IDO1 explorado clinicamente que estabiliza a enzima na verdade acelerou o movimento celular, em consonância com o papel não enzimático pró-tumoral de IDO1. Em contraste, um composto iDeg retardou a migração, consistente tanto com a inibição enzimática quanto com a perda da própria proteína. O estudo, portanto, descobre uma nova maneira de manipular IDO1: não arrastando-a forçosamente para uma ligase não relacionada com uma molécula projetada volumosa, mas “supercarregando” uma via de degradação nativa que já existe nas células.
O Que Isso Pode Significar para Terapias Contra o Câncer Futuras
Para não especialistas, a mensagem principal é que a qualidade — não apenas a quantidade — da inibição enzimática importa. Essas novas pequenas moléculas atuam como interruptores de precisão: elas travam IDO1 em uma forma vulnerável que a célula está pronta para destruir, cortando tanto suas contribuições metabólicas quanto de sinalização para a sobrevivência tumoral. Como os iDegs são compactos, com características farmacológicas e dependem da ligase própria da célula para a remoção de IDO1, podem oferecer uma abordagem mais sutil e amplamente aplicável do que os anteriores “degradadores de proteínas”. Se estratégias semelhantes puderem ser aplicadas a outras proteínas problemáticas, este trabalho sugere uma nova geração de terapias que incentivam as células doentes a desmontar suas próprias armas moleculares.
Citação: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Palavras-chave: IDO1, imunoterapia contra o câncer, degradação direcionada de proteínas, ligase de ubiquitina, degradadores de pequenas moléculas