Clear Sky Science · pt
Equilíbrio de ligantes biocompatíveis na coordenação de metais de transição permite arilação de proteínas in‑cell benigno
Transformando metais em ferramentas suaves para células
Muitas reações químicas poderosas dependem de metais, mas aproximá‑los de células vivas geralmente traz problemas: danos, estresse e morte celular. Este estudo mostra que, com a “alça” molecular certa em torno de um átomo de níquel, é possível realizar uma reação sofisticada dentro de células vivas sem prejudicá‑las. Essa descoberta permite aos cientistas marcar milhares de sítios específicos em proteínas e até acompanhar o aparecimento de patógenos difíceis de rastrear, abrindo novas maneiras de mapear o que realmente acontece dentro das células em saúde e doença.
Por que os metais são amigos e inimigos
O níquel e outros metais já atuam discretamente em nossos corpos como partes de enzimas naturais, mas também podem ser tóxicos se se ligarem onde não devem. A natureza resolve isso envolvendo os metais com pequenas moléculas e proteínas cuidadosamente escolhidas, que os direcionam aos alvos corretos e bloqueiam reações indesejadas. Os químicos, por outro lado, costumam usar reagentes metálicos extremamente reativos e nada ajustados para a vida. Esses reagentes foram excelentes para construir moléculas complexas num frasco, mas muito agressivos para uso livre dentro de células, especialmente quando o objetivo é acoplar uma pequena “etiqueta” a um aminoácido específico numa proteína sem perturbar o restante da célula.
Projetando um reagente de níquel mais gentil
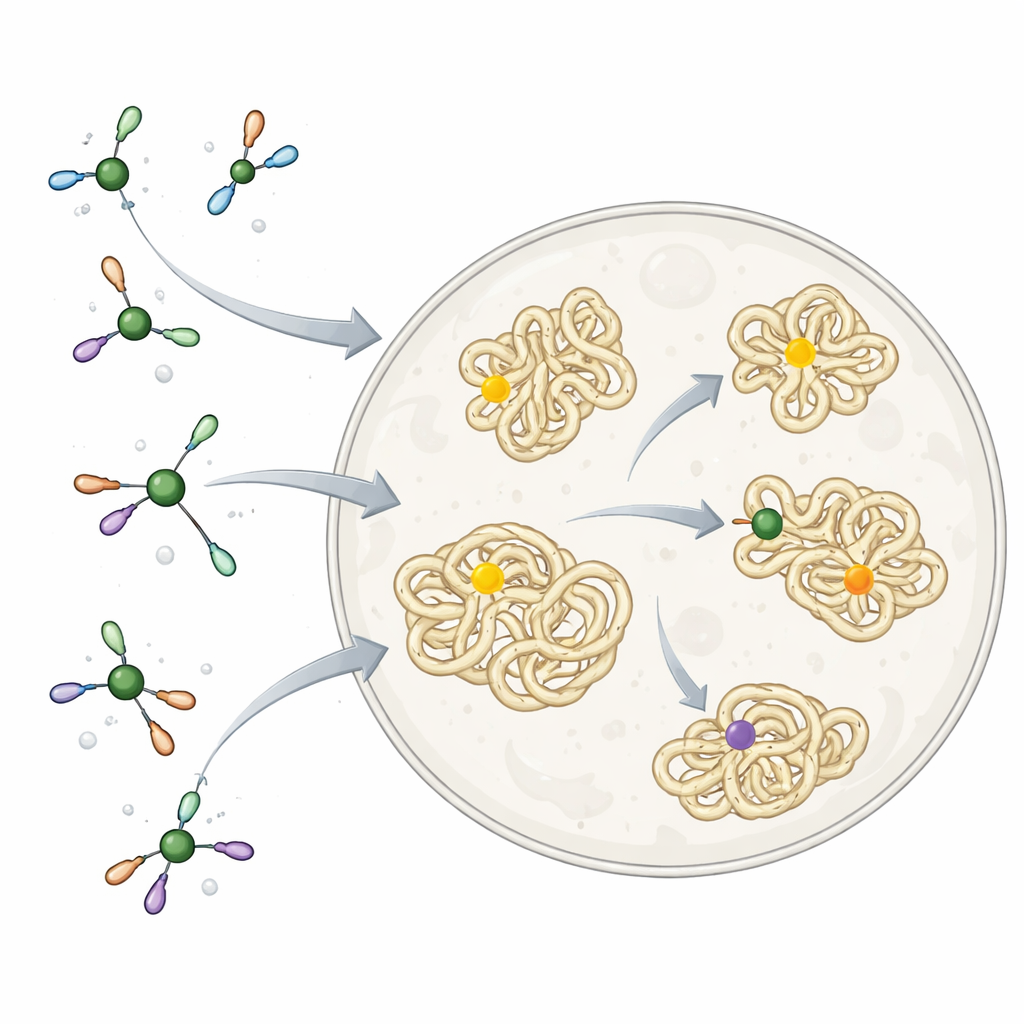
Os pesquisadores se inspiraram em como as próprias células lidam com o níquel. Eles construíram um conjunto de complexos de níquel envoltos num ligante simples e biocompatível chamado TMEDA. Essa pequena molécula age como uma braçadeira suave: firme o suficiente para impedir que o níquel se ligue a componentes celulares errados, mas frouxa o bastante para permitir que realize a reação chave. A reação junta um fragmento aril — um grupo plano em forma de anel comumente encontrado em fármacos — ao átomo de enxofre do aminoácido cisteína em proteínas. Em proteínas purificadas em solução, esses complexos de níquel rapidamente e seletivamente anexaram grupos aril a sítios de cisteína isolados, funcionando em muitas conformações e posições proteicas diferentes, o que mostra que a química é amplamente compatível com moléculas biológicas reais.
Editando proteínas dentro de células vivas
Em seguida, a equipe investigou se esses mesmos reagentes poderiam atuar dentro de células vivas sem ser venenosos. Compararam sais simples de níquel, conhecidos por serem prejudiciais, com os complexos de níquel ligados ao TMEDA. Em células de mamíferos, as fontes simples de níquel causaram morte celular substancial em doses relativamente baixas, enquanto os complexos com equilíbrio de ligante permaneceram bem tolerados mesmo em concentrações milimolares. Essa janela de segurança permitiu que os pesquisadores expusessem células bacterianas e de mamíferos aos reagentes de níquel tempo suficiente para que eles penetrassem e modificassem proteínas. Ao incorporar uma “alça” azida em uma versão do grupo aril, puderam ligar corantes fluorescentes ou etiquetas de biotina após a reação, revelando marcação clara e dependente da dose de proteínas por todo o citoplasma e núcleo de células vivas.
Mapeando sítios proteicos reativos pelo proteoma
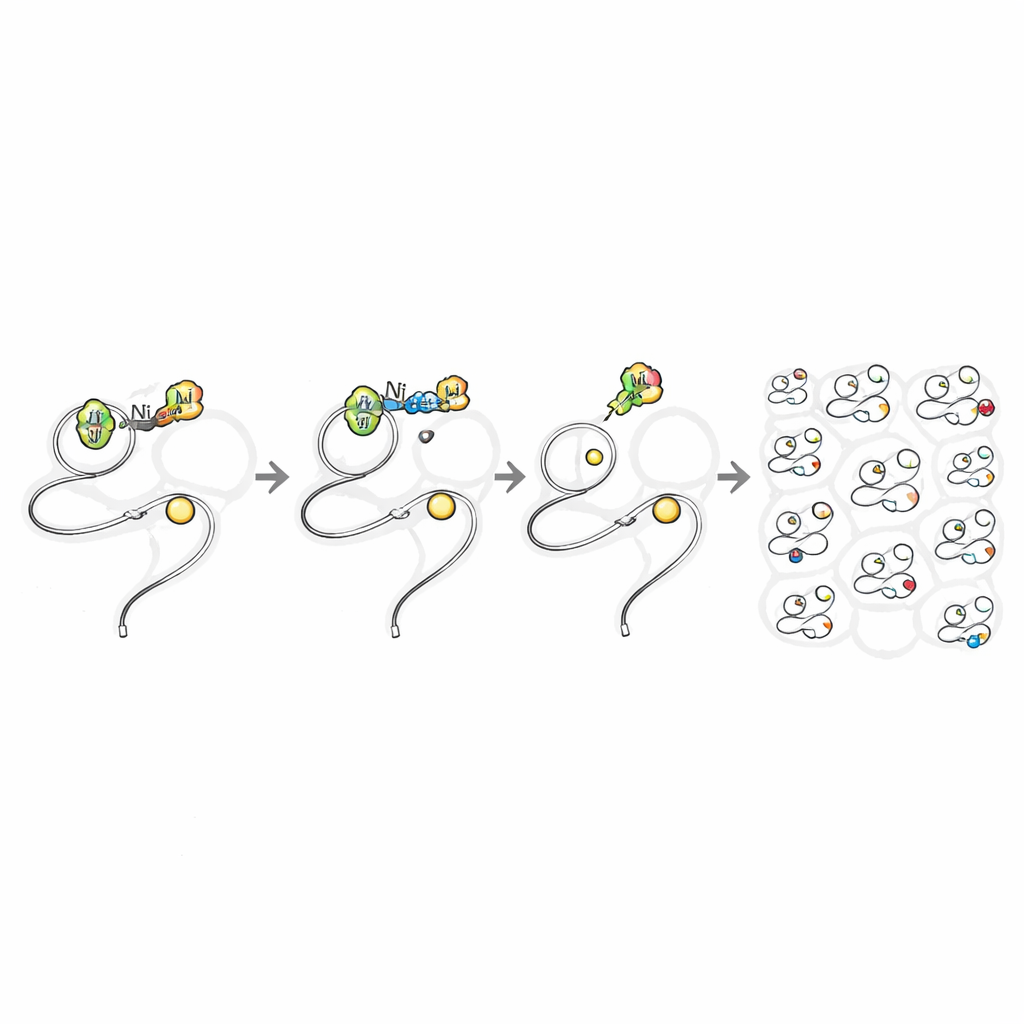
Com uma reação segura e rápida in‑cell em mãos, os autores a transformaram em uma ferramenta de descoberta. Trataram células humanas vivas com o reagente de níquel contendo azida, então usaram uma etiqueta de biotina fotoclavável e espectrometria de massas avançada para identificar exatamente quais cisteínas haviam sido modificadas. Em um único experimento detectaram quase 11.000 sítios de cisteína em cerca de 5.000 proteínas — aproximadamente o dobro do número de proteínas cobertas por todos os estudos anteriores de perfilamento de cisteína em células vivas somados. A marcação foi altamente seletiva para cisteína e mostrou pouco viés por tipos proteicos, localizações ou sítios ativos conhecidos. Notavelmente, muitas das proteínas alvo eram consideradas “não ligáveis” pelos padrões atuais de descoberta de fármacos, incluindo proteínas de sinalização de baixa abundância e chaves redox‑sensíveis que são difíceis de estudar apenas por genética.
Rastreando patógenos ocultos em tempo real
A mesma química também se mostrou sensível o bastante para captar proteínas estranhas produzidas durante a infecção. Em células humanas com sequências virais latentes, o método detectou fatores de transcrição virais presentes em níveis extremamente baixos, incluindo formas de splicing alternativas. A equipe então infectou células com dois patógenos muito diferentes: a bactéria intracelular Chlamydia trachomatis e o vírus Sindbis, um vírus de RNA relacionado ao chikungunya. Ao pulsar células infectadas com o reagente de níquel em diferentes momentos, conseguiram capturar sítios de cisteína em proteínas ribossomais e regulatórias bacterianas chave conforme a bactéria mudava entre estágios do ciclo de vida, e em proteínas virais não‑estruturais críticas que dirigem a replicação de RNA. Esses sítios marcados agora se destacam como possíveis pontos fracos para estratégias antivirais ou antibacterianas futuras.
O que isso significa para a química celular futura
Ao equilibrar cuidadosamente a casca de ligantes ao redor do níquel, este trabalho demonstra que um metal tradicionalmente arriscado pode realizar uma reação de edição covalente precisa em proteínas no interior de células vivas com dano mínimo. Isso possibilita pintar um mapa funcional detalhado de sítios reativos de cisteína através do proteoma, incluindo proteínas escassas, transitórias ou difíceis de serem moduladas por fármacos. Também oferece uma forma de rastrear e sondar patógenos dentro de suas células hospedeiras ao nível de aminoácidos individuais. Mais amplamente, o estudo sugere que muitas outras químicas metálicas “proibidas” podem ser domesticadas de modo semelhante, abrindo uma nova era em que as poderosas ferramentas da química sintética atuam de forma segura dentro de sistemas vivos.
Citação: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Palavras-chave: perfilamento de cisteína, bioconjugação com níquel, marcação de proteínas em células vivas, quimoproteômica, mapeamento do proteoma de patógenos