Clear Sky Science · pt
Ubiquitinação em lisina-11 impulsiona a indução de interferons tipo I/III pelo cGAS–STING e pelos receptores Toll-like 3 e 4
Como Nossas Células Soam o Alarme
Quando vírus ou moléculas perigosas invadem o corpo, nossas células precisam decidir em minutos se lançam sinais antivirais poderosos chamados interferons. Esses sinais podem nos salvar de infecções graves — mas, quando acionados de forma inadequada, também promovem doenças autoimunes prejudiciais. Este estudo revela um “quadro de comutação” molecular anteriormente oculto dentro das células que ajuda a decidir quando ativar respostas de interferon e quando contê-las. Entender esse quadro oferece pistas para vacinas melhores, terapias antivirais e tratamentos para doenças movidas por interferon.
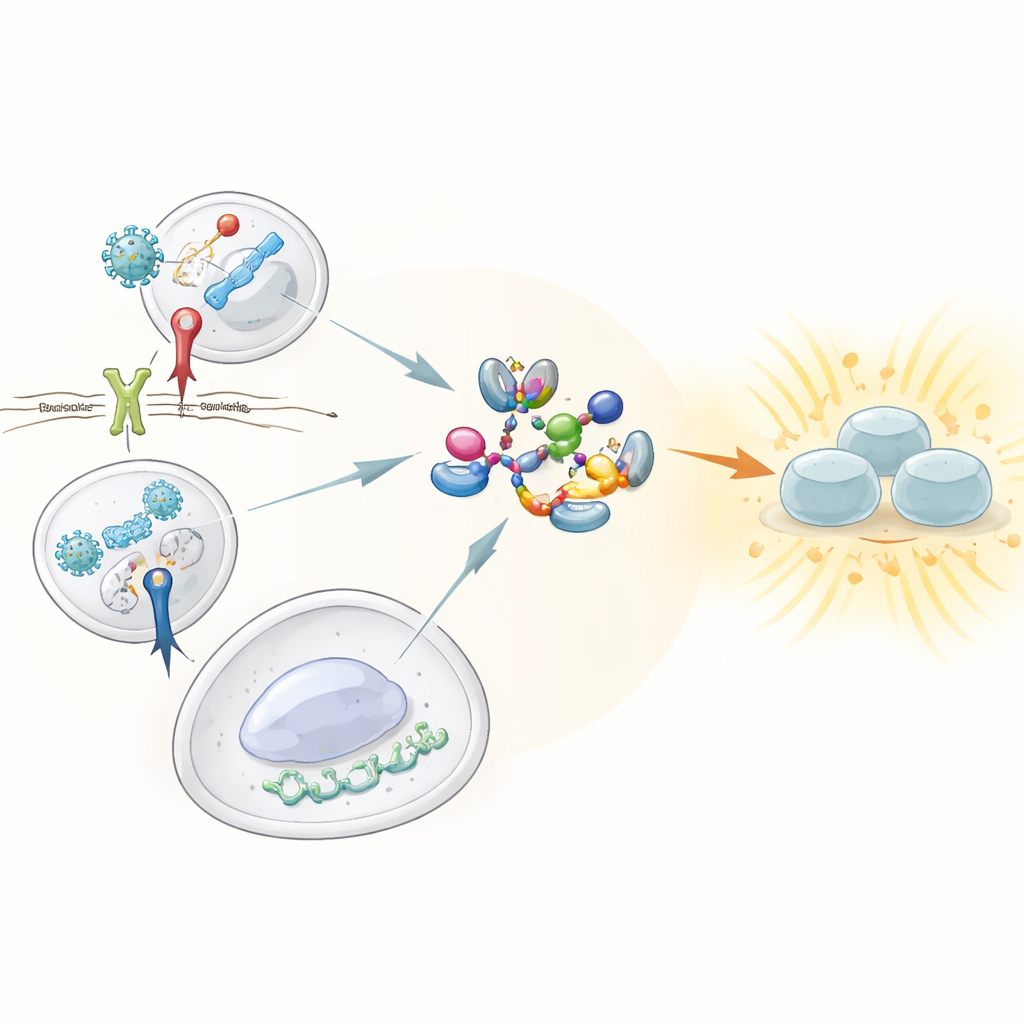
Guardiões que Sentem Perigo
Nosso sistema imune inato depende de sentinelas conhecidas como receptores de reconhecimento de padrões, que patrulham em busca de sinais característicos de vírus e bactérias. Entre eles, três se destacam por sua capacidade de disparar fortes respostas de interferon: o receptor Toll-like 3 (TLR3), que detecta RNA viral de dupla hélice; o receptor Toll-like 4 (TLR4), que percebe um componente da parede celular bacteriana; e a via cGAS–STING, que identifica DNA fora do lugar dentro das células. Todos três precisam ativar uma enzima central chamada TBK1, que por sua vez liga o fator de transcrição IRF3 para impulsionar a produção de interferons tipo I e III. Até agora, não se compreendia bem como esses sensores convergiam para ativar o TBK1.
Um Conector Molecular Oculto
Os pesquisadores descobriram que uma proteína chamada ANKIB1 atua como um conector crucial entre esses sensores e o TBK1. ANKIB1 é uma enzima que anexa pequenas etiquetas moleculares, conhecidas como cadeias de ubiquitina, a outras proteínas. Importante: ela constrói um tipo específico de cadeia, com ligação denominada “K11”, que antes era mais conhecida por papéis na divisão celular do que na imunidade. Em células humanas sem ANKIB1, a estimulação de TLR3 ou a ativação de STING deixou de promover a ativação adequada de TBK1 e IRF3, e genes de interferon mal foram ativados. Restaurar ANKIB1 trouxe a resposta de volta, demonstrando que essa única enzima é necessária e suficiente para conduzir esse ramo do alarme antiviral.
Construindo uma Plataforma de Acoplamento para Proteínas de Transmissão
Uma inspeção mais detalhada revelou como ANKIB1 exerce sua influência. Quando TLR3 ou STING detectam perigo, eles montam plataformas multiproteicas chamadas sinalossomos. ANKIB1 é recrutado a essas plataformas por meio de uma região que reconhece ubiquitina. Uma vez ali, ele etiqueta vários componentes-chave — incluindo os adaptadores TRIF e o próprio STING, além de outras moléculas de sinalização — com cadeias de ubiquitina ligadas por K11. Essas cadeias não marcam as proteínas para destruição; em vez disso, funcionam como um Velcro molecular. Outra proteína, Optineurina (OPTN), é atraída especificamente para esses locais modificados. Servindo como um adaptador de transmissão, a OPTN traz então o TBK1 para o complexo, permitindo sua ativação e a passagem do sinal para IRF3 e genes de interferon. Quando a OPTN foi removida, a ativação de TBK1 colapsou, ressaltando que a marcação por K11 feita por ANKIB1 e a ligação de OPTN formam um eixo único e essencial.
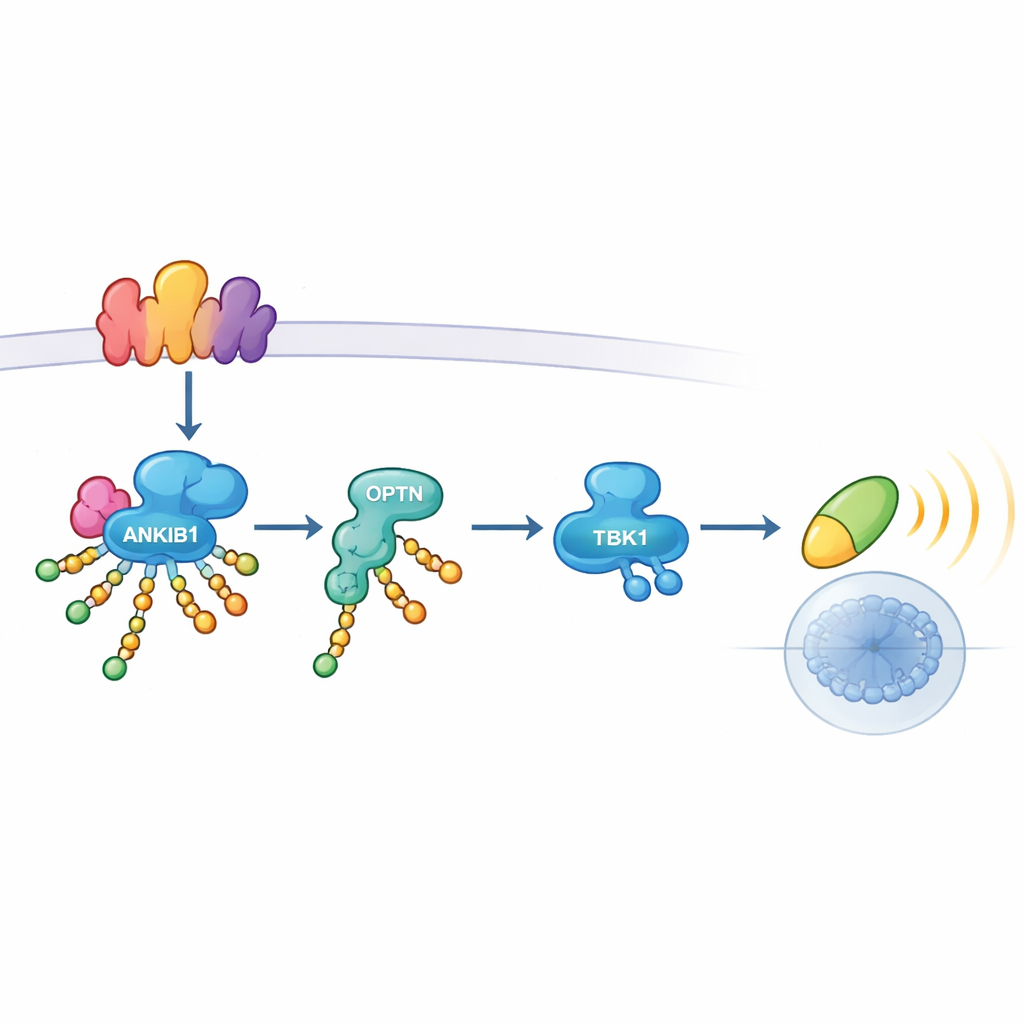
Quando Essa Via Importa — E Quando Não
A equipe então investigou se esse mecanismo é universal entre todos os sensores antivirais. Eles descobriram que ANKIB1 é vital para a indução de interferon via TLR3, o braço dependente de TRIF do TLR4, e a via cGAS–STING, todas as quais usam a OPTN como adaptador principal para o TBK1. Em contraste, outro sensor, RIG-I, que detecta RNA viral, depende de um conjunto diferente de adaptadores e não precisa de ANKIB1 ou OPTN para ativar o TBK1. Experimentos em camundongos refletiram esses achados em células. Animais sem Ankib1 produziram muito menos interferon após ativar TLR3 ou STING, foram protegidos de uma síndrome inflamatória letal dirigida por interferon, mas ficaram muito mais vulneráveis à infecção por vírus herpes simplex 1, um vírus de DNA que depende fortemente da via cGAS–STING para controle. As respostas ao vírus da influenza, detectado principalmente por RIG-I, permaneceram amplamente intactas.
Equilibrando Proteção e Dano
Em conjunto, esses resultados revelam as cadeias de ubiquitina ligadas em K11 geradas por ANKIB1 como uma moeda central em um grande ramo da sinalização antiviral inata. Ao criar locais de acoplamento para a OPTN, ANKIB1 ajuda a montar o revezamento molecular preciso que transforma o perigo sentido por TLR3, TLR4 (via TRIF) e cGAS–STING em produção robusta de interferon. Esse eixo é de dois gumes: é essencial para a defesa contra certos vírus, mas também alimenta doenças inflamatórias dirigidas por interferon quando superativado. Como a atividade catalítica e domínios específicos de ANKIB1 são necessários para essa função, eles representam alvos atraentes para futuros fármacos projetados tanto para atenuar respostas de interferon prejudiciais em condições autoimunes quanto para reforçar a imunidade antiviral quando ela é fraca.
Citação: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Palavras-chave: imunidade inata, sinalização de interferon, ubiquitinação, via cGAS–STING, infecção viral