Clear Sky Science · pt
Superando a resistência a inibidores de tirosina quinase mediada pelo nicho vascular na leucemia mieloide aguda por meio da inibição de miR-126
Por que isso importa para pacientes com câncer
A leucemia mieloide aguda (LMA) é um dos cânceres do sangue mais agressivos e, mesmo com medicamentos modernos direcionados, muitos pacientes apresentam recidiva. Este estudo responde a uma pergunta enganadoramente simples, com grandes implicações: parte do problema não é apenas as células cancerosas em si, mas o “bairro” em que elas vivem dentro da medula óssea? Ao construir um modelo computacional detalhado fundamentado em dados de laboratório, os autores investigam como pequenos vasos sanguíneos podem proteger células-tronco da leucemia contra medicamentos — e como bloquear um único pequeno RNA sinalizador pode desmontar essa proteção.
O abrigo oculto na medula óssea
A LMA surge na medula óssea, onde células blastas malignas substituem a produção normal de sangue. Dentro desse enxame esconde-se uma população menor de células-tronco da leucemia que podem autorrenovar-se e sobreviver ao tratamento, semeando a recidiva. Essas células-tronco não flutuam livremente; elas se acomodam em bolsões especializados ao redor de pequenas artérias e capilares, conhecidos coletivamente como nicho vascular. O estudo foca em pacientes cujas células leucêmicas carregam mutações FLT3-ITD, tratadas com inibidores de tirosina quinase (TKIs). Embora esses fármacos possam reduzir drasticamente a carga tumoral, muitos pacientes ainda recaem, sugerindo que algumas células estão sendo escondidas ou protegidas.
Um efeito terapêutico de duas faces
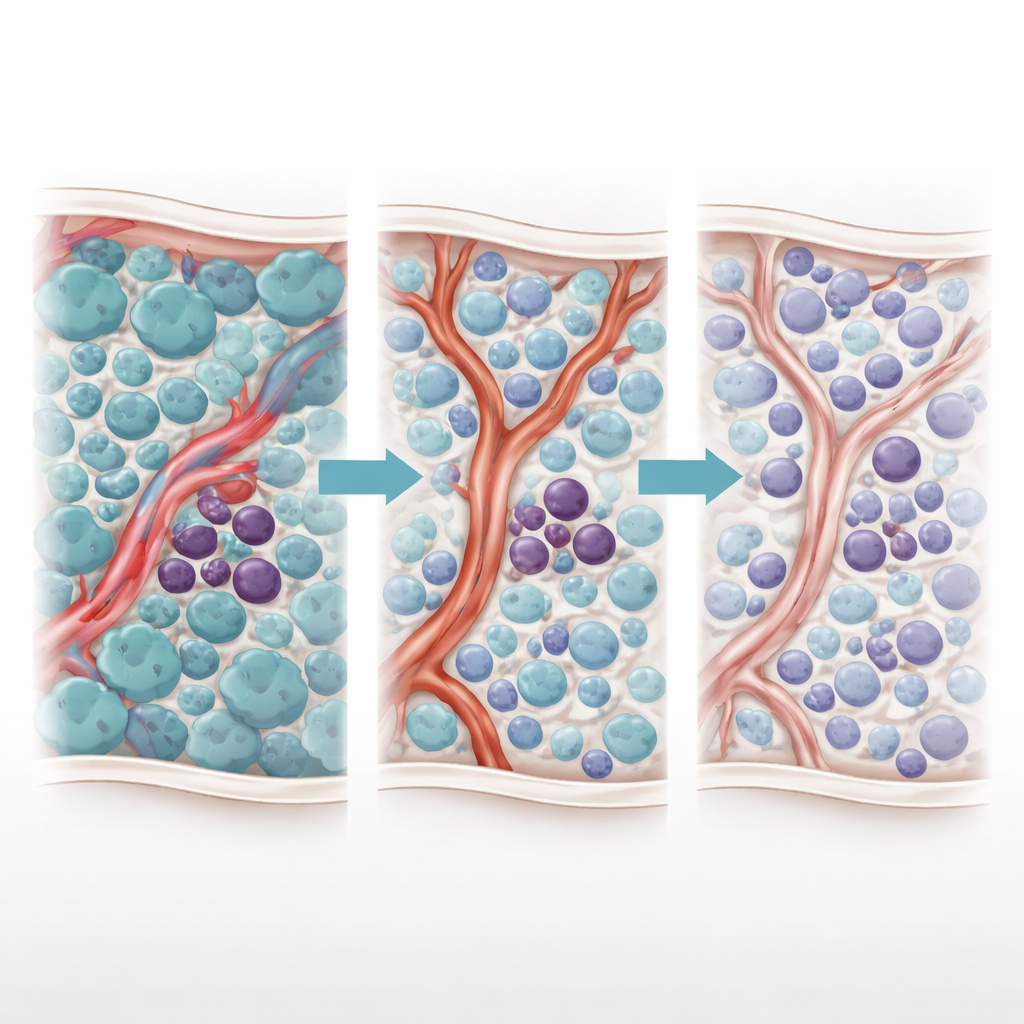
Os autores haviam descoberto anteriormente um enigmático “fenômeno de Jano” — uma resposta com duas faces à terapia com TKI. Conforme os TKIs eliminam as células blastas que se dividem rapidamente, os níveis de uma molécula inflamatória, o TNF-α, caem. Essa queda permite inesperadamente que as células vasculares vizinhas intensifiquem a produção de um pequeno RNA regulador chamado miR-126. Esse miR-126 é transferido das células endoteliais para as células-tronco da leucemia, levando-as a um estado silencioso e não-divisório que as torna altamente resistentes ao medicamento. Em outras palavras, o próprio tratamento que elimina a maioria das células cancerosas remodela a medula óssea de modo a abrigar as mais perigosas.
Construindo uma medula óssea virtual
Para dissecar essa dinâmica, a equipe criou um modelo computacional baseado em agentes da medula óssea na LMA. Cada ator-chave — células blastas, células-tronco da leucemia e células endoteliais que revestem os vasos — é representado como um “agente” individual seguindo regras biologicamente informadas. Moléculas em difusão, como TNF-α, miR-126, o TKI AC220 e um fármaco bloqueador de miR-126 chamado miRisten, se espalham pelo tecido simulado. O modelo foi calibrado com dados de imagem de camundongos que mapeiam padrões vasculares reais, incluindo áreas ricas ou pobres em vasos produtores de miR-126. Nas simulações, o tratamento padrão com TKI reproduziu de forma confiável o efeito de Jano: as blastas diminuíram, o TNF-α caiu, o miR-126 vindo dos vasos aumentou, as células-tronco recuaram para nichos protetores e a doença posteriormente rebrotou.
Desligando o escudo com timing preciso
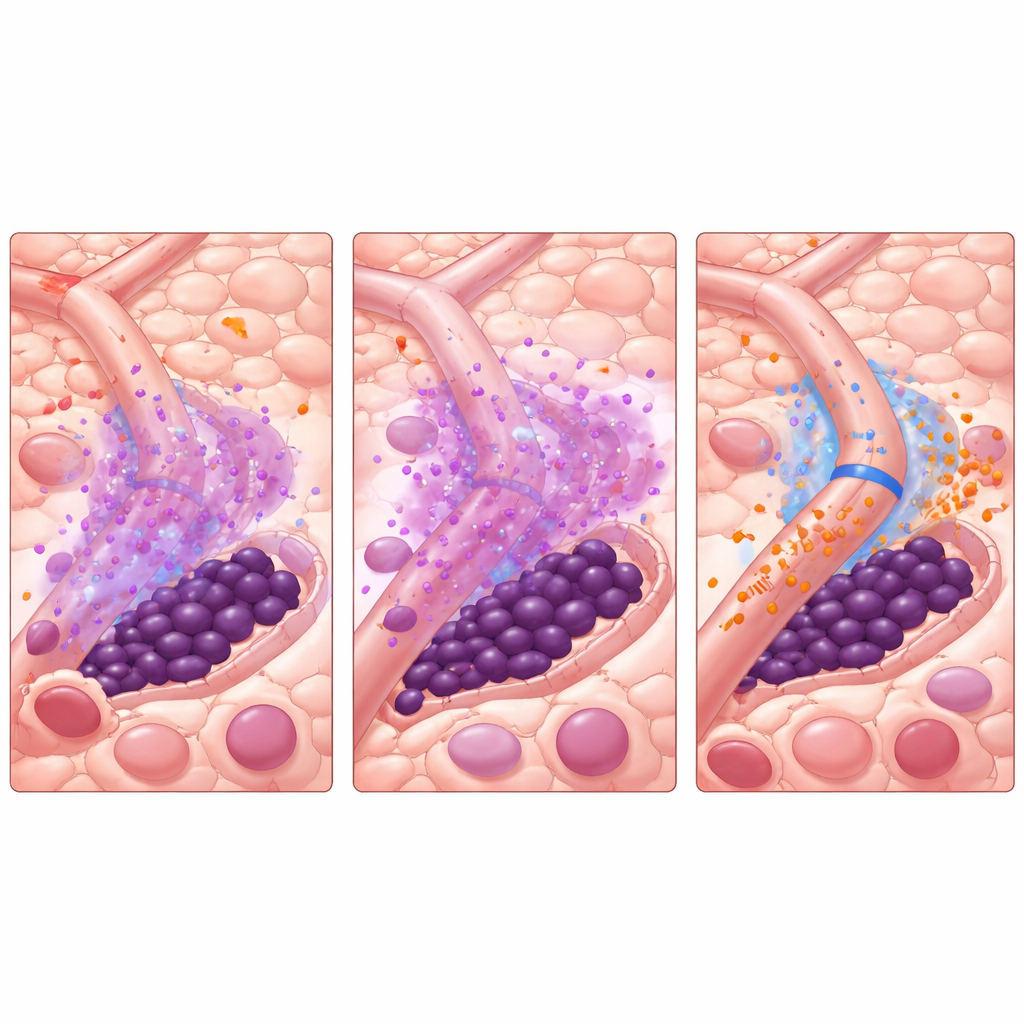
Munidos desse sistema virtual, os pesquisadores testaram formas de romper o ciclo vicioso. Simplesmente adicionar miRisten ao mesmo tempo que o TKI ajudou, mas raramente curou a doença no modelo. Uma abordagem mais estratégica foi mais potente: um curto “pré-tratamento” com miRisten isoladamente para reduzir o miR-126 vascular, seguido por TKI sozinho ou por terapia combinada contínua. Em vários arranjos vasculares simulados, mesmo poucos dias de pré-tratamento com miRisten antes de iniciar o AC220 reduziram dramaticamente ou eliminaram a recidiva, ao mesmo tempo que limitavam a exposição total a fármacos. O modelo também revelou que quão perto as células-tronco da leucemia ficam dos vasos sanguíneos afeta fortemente seu destino — células aninhadas junto aos vasos ganham a maior proteção, a menos que o miR-126 seja bloqueado.
O que isso pode significar para cuidados futuros
De forma direta, o estudo sugere que algumas células-tronco da leucemia sobrevivem não porque os TKIs sejam fracos, mas porque os pequenos vasos da medula óssea entram temporariamente em modo “protetor” durante o tratamento. Ao desligar brevemente um único sinal, o miR-126, antes de administrar o TKI, pode ser possível remover esse escudo, forçar as células-tronco a saírem do esconderijo e torná-las vulneráveis aos medicamentos existentes. Embora este trabalho se baseie em simulações de computador ancoradas em dados de laboratório — e ainda não em ensaios clínicos —, ele oferece uma estratégia concreta: programar um fármaco que mira o microambiente imediatamente antes e durante a terapia padrão. Se validada, essa abordagem poderia não apenas melhorar os resultados para pessoas com LMA mutada em FLT3, mas também inspirar táticas semelhantes em outros cânceres hematológicos e sólidos onde o “bairro” tumoral ajuda a evadir o tratamento.
Citação: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
Palavras-chave: leucemia mieloide aguda, células-tronco da leucemia, microambiente da medula óssea, resistência a inibidores de tirosina quinase, inibição de miR-126