Clear Sky Science · pt
Modelos de deep learning identificam alterações cerebrais durante a progressão da doença de Alzheimer
Por que acompanhar a mudança cerebral ao longo do tempo importa
A doença de Alzheimer vai tirando gradualmente a memória e a capacidade de raciocínio das pessoas, mas o dano no cérebro se acumula anos antes de os sintomas cotidianos ficarem evidentes. Os médicos costumam basear-se em uma única imagem cerebral ou resultado de exame para julgar se alguém tem Alzheimer, apesar de a doença se desenrolar ao longo do tempo. Este estudo coloca uma pergunta simples com grandes consequências: se seguirmos as imagens cerebrais das pessoas por vários anos e deixarmos um modelo computacional avançado aprender com essas mudanças, podemos não só detectar Alzheimer com mais precisão, como também ver quais áreas do cérebro são afetadas primeiro e com maior intensidade?
Acompanhando a história do cérebro, não apenas um instantâneo
Os pesquisadores usaram exames estruturais de ressonância magnética (RM), que mostram a anatomia cerebral em detalhe, de mais de 280 idosos, incluindo pessoas com Alzheimer e pares cognitivamente normais. Fundamentalmente, cada pessoa teve três exames realizados com cerca de um ano de intervalo, permitindo à equipe rastrear como o tecido cerebral mudou ao longo de dois anos. Em vez de tratar cada exame como uma imagem isolada, eles construíram um modelo de deep learning que leva todos os pontos temporais em conjunto. O modelo foi projetado para prestar atenção à substância cinzenta — o tecido cerebral repleto de corpos de neurônios — bem como à substância branca e ao líquor, e para aprender como os padrões nesses tecidos evoluem conforme a doença progride.
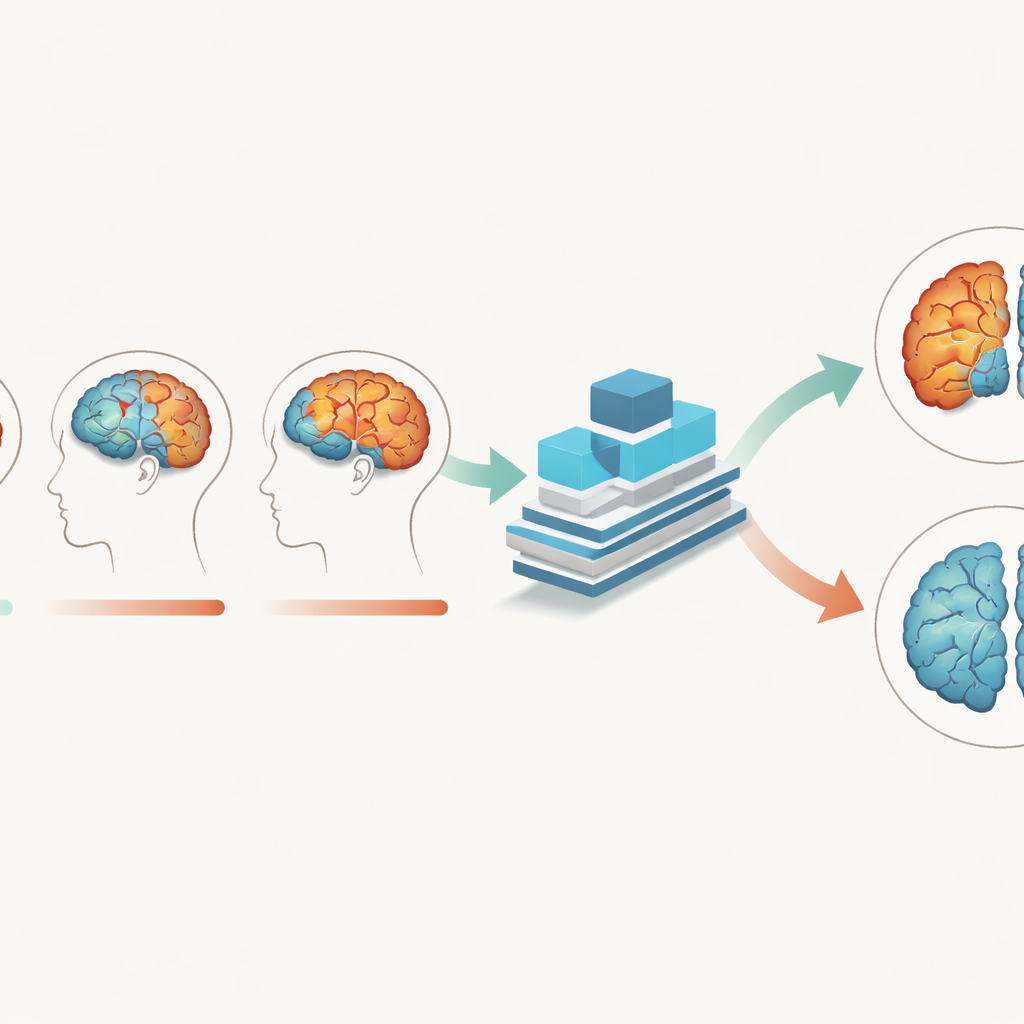
Um modelo de deep learning sintonizado aos ritmos cerebrais
Para captar essas mudanças sutis, a equipe criou uma Rede de Atenção de Fusão Multirramos (Multi-Branch Fusion Channel Attention Network), uma rede neural convolucional 3D que processa volumes de RM em vez de imagens planas. Ramos separados tratam diferentes tecidos ou pontos temporais e então fundem suas informações, enquanto um mecanismo de “atenção” ajuda o modelo a focar nas regiões tridimensionais mais informativas. Treinada principalmente com dados de substância cinzenta, a rede aprendeu a distinguir cérebros com Alzheimer de cérebros com envelhecimento normal com cerca de 93% de acurácia e especificidade perfeita em um conjunto de dados, superando vários métodos de IA existentes. Também generalizou bem para um conjunto de dados australiano independente, sugerindo que não está simplesmente memorizando particularidades de um estudo, mas captando sinais de doença mais amplos.
Vendo quais regiões cerebrais inclinam a balança
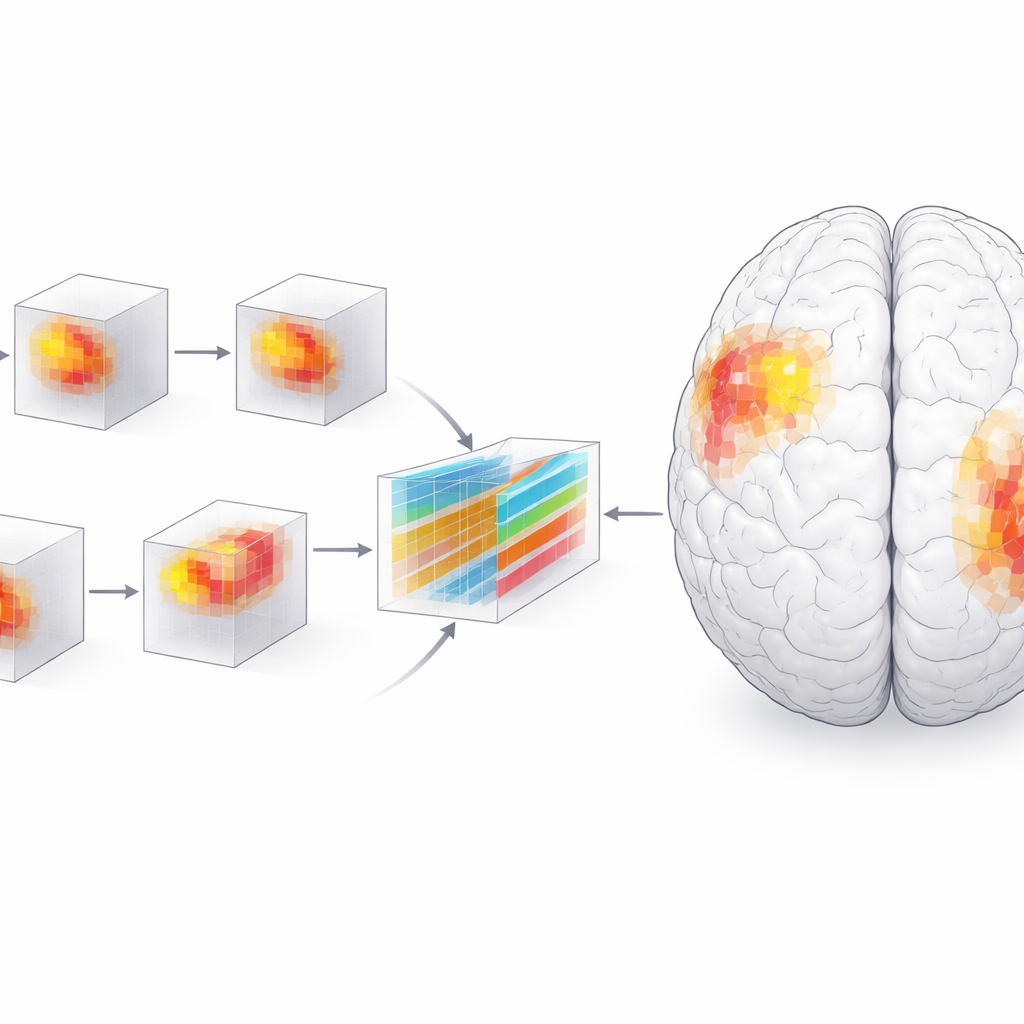
Alta acurácia por si só não é suficiente para a medicina; os clínicos precisam entender o que motiva as decisões de um modelo. Os pesquisadores, portanto, usaram uma técnica de interpretabilidade chamada SHAP, que atribui uma pontuação de importância a cada minúsculo pixel tridimensional — ou voxel — na RM. Agrupar esses voxels em regiões anatômicas revelou um quadro dinâmico da doença. No início, a amígdala, uma região envolvida em emoção e memória, destacou-se como especialmente importante para distinguir pacientes de controles saudáveis. Com o tempo, o hipocampo, o giro parahipocampal e, especialmente, as partes posteriores do lobo temporal ganharam influência, enquanto o papel relativo da amígdala diminuiu. Aos dois anos, as diferenças entre pacientes e controles estavam muito mais nítidas e mais agrupadas, particularmente no lado esquerdo do cérebro.
Padrões que correspondem a sintomas e escores clínicos
Para verificar se o foco do modelo estava alinhado com a biologia, a equipe realizou análises tradicionais de volume cerebral e testes estatísticos. Eles descobriram que a substância cinzenta nas regiões destacadas encolheu mais rapidamente em pessoas com Alzheimer do que em adultos com envelhecimento normal, e que volumes mais baixos nessas áreas acompanharam de perto piores escores em testes cognitivos padrão, como o Mini-Exame do Estado Mental (MEEM) e a Clinical Dementia Rating. O caminho do dano — das estruturas temporais internas para fora, em direção a áreas posteriores relacionadas à linguagem e associação — refletiu esquemas clássicos de estadiamento patológico da doença de Alzheimer. Surgiu também um viés do lado esquerdo, consistente com a dominância cerebral para linguagem e certas funções de memória nesse hemisfério. A morfometria baseada em voxel mostrou que as mudanças iniciais eram dispersas e pequenas, tornando-se depois maiores e mais concentradas nas regiões temporais posteriores e frontais à medida que a doença avançava.
O que isso significa para pacientes e médicos
Para não especialistas, a principal conclusão é que o Alzheimer não age como um interruptor simples ligado/desligado no cérebro; ele segue um trajeto ordenado, porém acelerado, deixando pegadas distintas ao longo do tempo. Ao ensinar um modelo de deep learning a ler não só onde o cérebro parece diferente, mas como essas diferenças crescem ao longo de vários anos, este estudo oferece uma forma de sinalizar o Alzheimer com mais precisão e em estágios mais precoces. Também identifica um conjunto pequeno de regiões cerebrais — incluindo a amígdala, o hipocampo, o giro parahipocampal e o córtex temporal posterior — cujo tamanho e estrutura em mudança estão fortemente ligados ao declínio cognitivo. Embora mais trabalho seja necessário, especialmente com métodos de imagem adicionais e conjuntos de dados maiores, essa abordagem nos aproxima do uso de exames cerebrais com resolução temporal e IA interpretável como ferramentas práticas para diagnóstico precoce, monitoramento e, em última instância, para orientar intervenções contra a doença de Alzheimer.
Citação: Sun, J., Han, JD.J. & Chen, W. Deep learning models identify brain changes during the progression of Alzheimer’s disease. npj Syst Biol Appl 12, 42 (2026). https://doi.org/10.1038/s41540-026-00666-7
Palavras-chave: Doença de Alzheimer, RM cerebral, deep learning, imagem longitudinal, neurodegeneração