Clear Sky Science · pt
Desenvolvimento de um modelo grave de síndrome de realimentação em ratos e modelagem matemática da hipofosfatemia associada
Por que voltar a comer pode ser perigoso
Quando pessoas que estiveram gravemente desnutridas finalmente recebem alimentos ou nutrição intravenosa, os médicos precisam agir com cautela. Uma entrada repentina de calorias pode desencadear a “síndrome de realimentação”, uma complicação que perturba os eletrólitos do corpo e pode prejudicar o coração, músculos e pulmões. Um ator-chave é o fósforo, um mineral necessário para a energia em cada célula. Este estudo usou ratos e modelagem por computador para descobrir por que o fósforo no sangue pode desabar tão dramaticamente durante a realimentação e como poderíamos prevenir melhor essa queda perigosa.
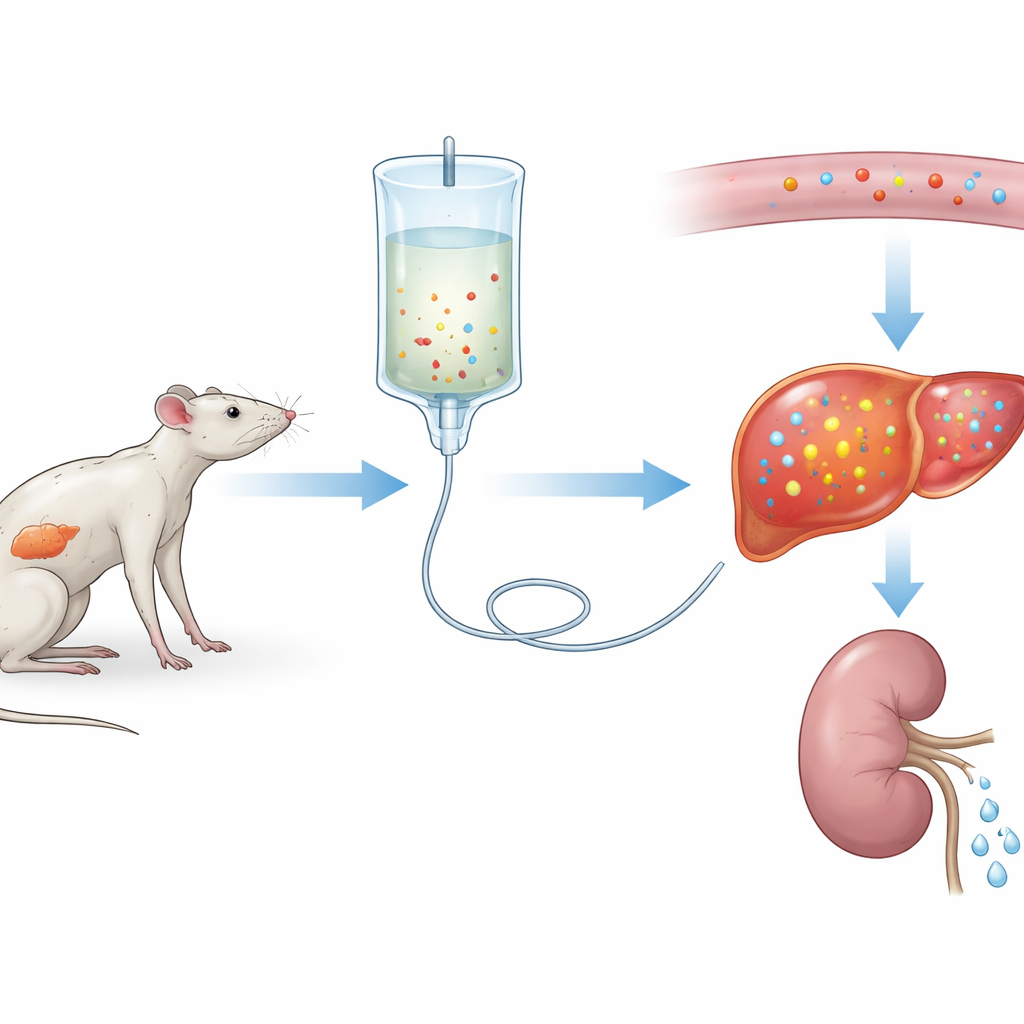
Um olhar mais atento sobre os problemas da realimentação
Os pesquisadores primeiro criaram uma versão grave da síndrome de realimentação em ratos. Por três semanas, um grupo recebeu uma dieta normal enquanto outro recebeu pouquíssima proteína, imitando a subnutrição de longa duração. Ambos os grupos então receberam a mesma nutrição intravenosa por três dias. Os ratos na dieta com baixo teor de proteína apresentaram uma queda acentuada no fósforo sanguíneo — cerca de 75% — junto com alterações em outros eletrólitos e sinais de lesão nos órgãos, especialmente no fígado e nos músculos. Essas mudanças assemelharam-se à síndrome de realimentação grave em pacientes, sugerindo que a equipe havia construído um modelo experimental fiel.
O que acontece com o fósforo durante a realimentação
Para entender como o fósforo se movimenta no corpo ao longo do tempo, os cientistas coletaram amostras repetidas de sangue e urina dos mesmos ratos. Eles descobriram que os níveis de fósforo no sangue caíram tanto em animais normais quanto naqueles privados de proteína após o início da alimentação, mas a queda foi muito mais profunda e durou mais no grupo subnutrido. Surpreendentemente, os rins reduziram a perda de fósforo na urina logo após a realimentação, de modo que o mineral não estava sendo eliminado. Em vez disso, o fósforo estava sendo puxado da corrente sanguínea para os tecidos, particularmente o fígado, cujos estoques haviam sido esgotados por semanas de dieta inadequada. Cálculos por computador confirmaram que os ratos desnutridos começaram com muito menos fósforo dentro das células e então o absorveram de forma agressiva quando os nutrientes chegaram.
A insulina não explica tudo
Como a realimentação aumenta a glicose no sangue e o hormônio insulina, os médicos há muito culpam a insulina por direcionar o fósforo para dentro das células. A equipe testou essa ideia reduzindo a liberação de insulina com o hormônio somatostatina. Como esperado, a glicemia aumentou, mas a queda no fósforo sanguíneo quase não melhorou. Ao mesmo tempo, os níveis de aminoácidos livres — os blocos de construção das proteínas — aumentaram. Em um experimento separado, os cientistas removeram aminoácidos da infusão. Nesse caso, os níveis de fósforo permaneceram muito mais estáveis, e o colapso grave foi evitado, embora os níveis de insulina fossem similares. Esses resultados apontam para um efeito combinado: tanto a insulina quanto os aminoácidos, e não apenas a insulina, estimulam as células a captar fósforo extra durante a realimentação.
Uma rede de controle oculta no fígado e no rim
Aprofundando-se, os pesquisadores examinaram proteínas hepáticas envolvidas na detecção de nutrientes, com foco numa via conhecida como mTOR, que responde à insulina e aos aminoácidos. Nos ratos com baixa proteína, a realimentação ativou fortemente essa via e aumentou os níveis de um transportador de fosfato chamado Pit2, que ajuda as células do fígado a captarem fósforo. O padrão correspondeu ao comportamento previsto pelo modelo matemático deles, que condensou essa rede em um único sinal de controle que chamaram de “simTOR”. O modelo também exigiu um fator de retroalimentação separado para explicar como os rins ajustam a perda de fósforo na urina. Medições de um hormônio derivado do osso, FGF-23, se encaixaram bem nesse papel: seus níveis despencaram quando a realimentação começou, limitando a excreção de fósforo, e então divergiram entre ratos normais e subnutridos de maneira que espelhava o sinal de retroalimentação simulado.
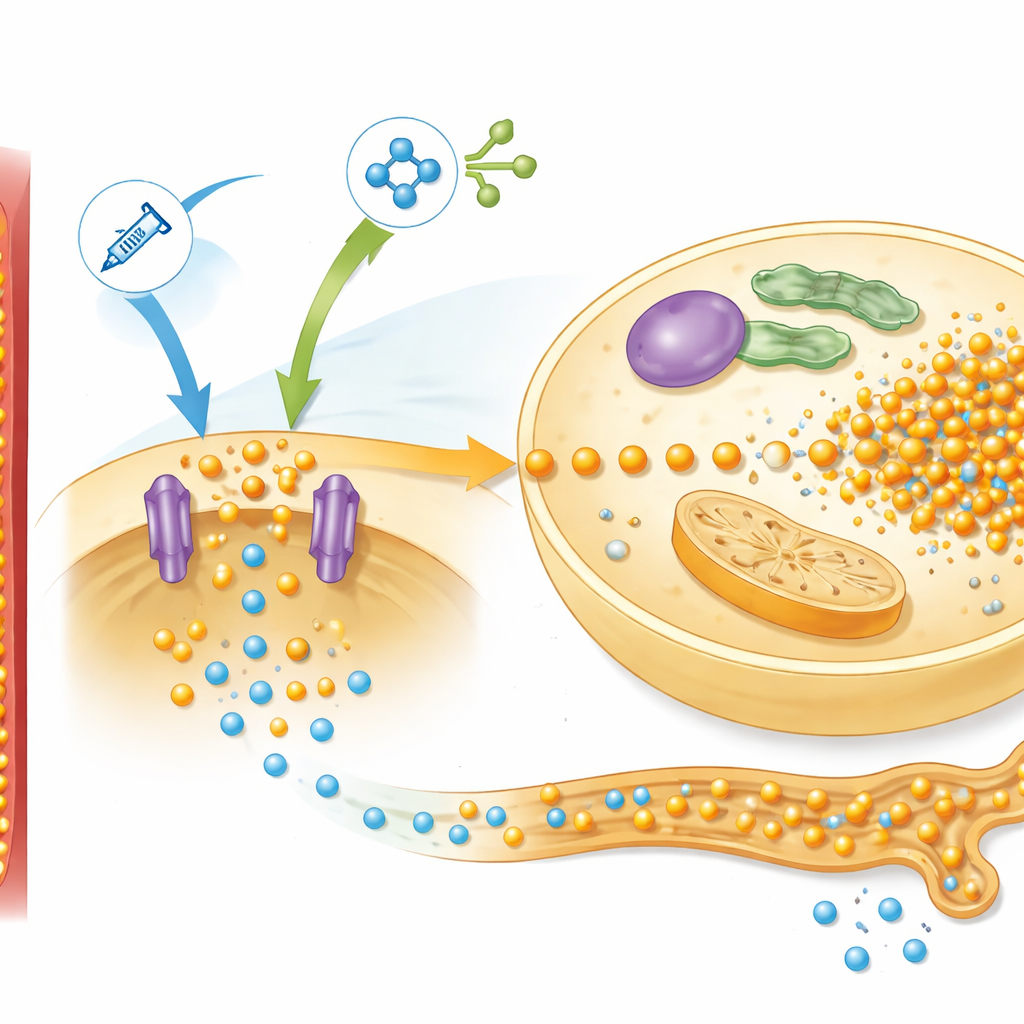
Usando matemática para testar estratégias de prevenção
Ao ajustar diferentes controles em seu modelo computacional, os autores puderam fazer perguntas “e se” que seriam difíceis ou arriscadas de testar diretamente em pacientes. A análise destacou três influências principais sobre a profundidade e a recuperação da queda de fósforo: o fósforo inicial dentro das células, a força do sistema de captação dirigido pela mTOR e a taxa de aporte de fósforo pela nutrição. As simulações sugeriram que simplesmente adicionar uma grande quantidade de fosfato no momento da realimentação seria difícil de equilibrar com segurança. No entanto, administrar fósforo extra antes da realimentação — permitindo que os órgãos reconstruam silenciosamente seus estoques internos — poderia atenuar a queda posterior nos níveis sanguíneos. Reduzir a carga de aminoácidos, especialmente aqueles que ativam fortemente mTOR e insulina, também pareceu protetor nos experimentos com animais.
O que isso significa para os pacientes
Para pessoas em risco de síndrome de realimentação — como aquelas com transtornos alimentares de longa duração ou fragilidade severa — este trabalho sugere que o perigo vem de mais do que apenas um pico de glicose no sangue. Órgãos famintos entram na realimentação com os tanques de fósforo vazios e, sob o empurrão combinado de insulina e aminoácidos, absorvem rapidamente o mineral do sangue enquanto os rins temporariamente o retêm. O resultado é uma deficiência circulante aguda e temporária que pode lesar tecidos vitais. O modelo em ratos e a estrutura matemática desenvolvidos aqui apontam para prevenções mais direcionadas: uso cauteloso e inicial de suplementos de fósforo, controle criterioso da nutrição rica em aminoácidos e atenção aos hormônios que regulam a excreção renal. Juntas, essas abordagens podem ajudar os clínicos a alimentar pacientes vulneráveis com mais segurança.
Citação: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
Palavras-chave: síndrome de realimentação, hipofosfatemia, metabolismo do fósforo, sinalização mTOR, nutrição parenteral