Clear Sky Science · pt
FBA espacial revela nichos Warburg heterogêneos em tumores renais e consumo de lactato em câncer colorretal
Por que o metabolismo tumoral no espaço importa
As células cancerosas não se comportam todas da mesma forma, mesmo dentro de um único tumor. Algumas vivem próximas a vasos sanguíneos, outras em regiões mal nutridas e profundas, e essas localizações moldam como elas obtêm e usam combustível. Este estudo apresenta uma nova forma de ler esse “mapa metabólico” oculto a partir de dados espaciais de expressão gênica de ponta. Ao fazer isso, os autores descobrem padrões surpreendentes sobre como diferentes tumores lidam com uma molécula-chave, o lactato, desafiando a visão clássica de que os cânceres apenas descartam o lactato como resíduo.
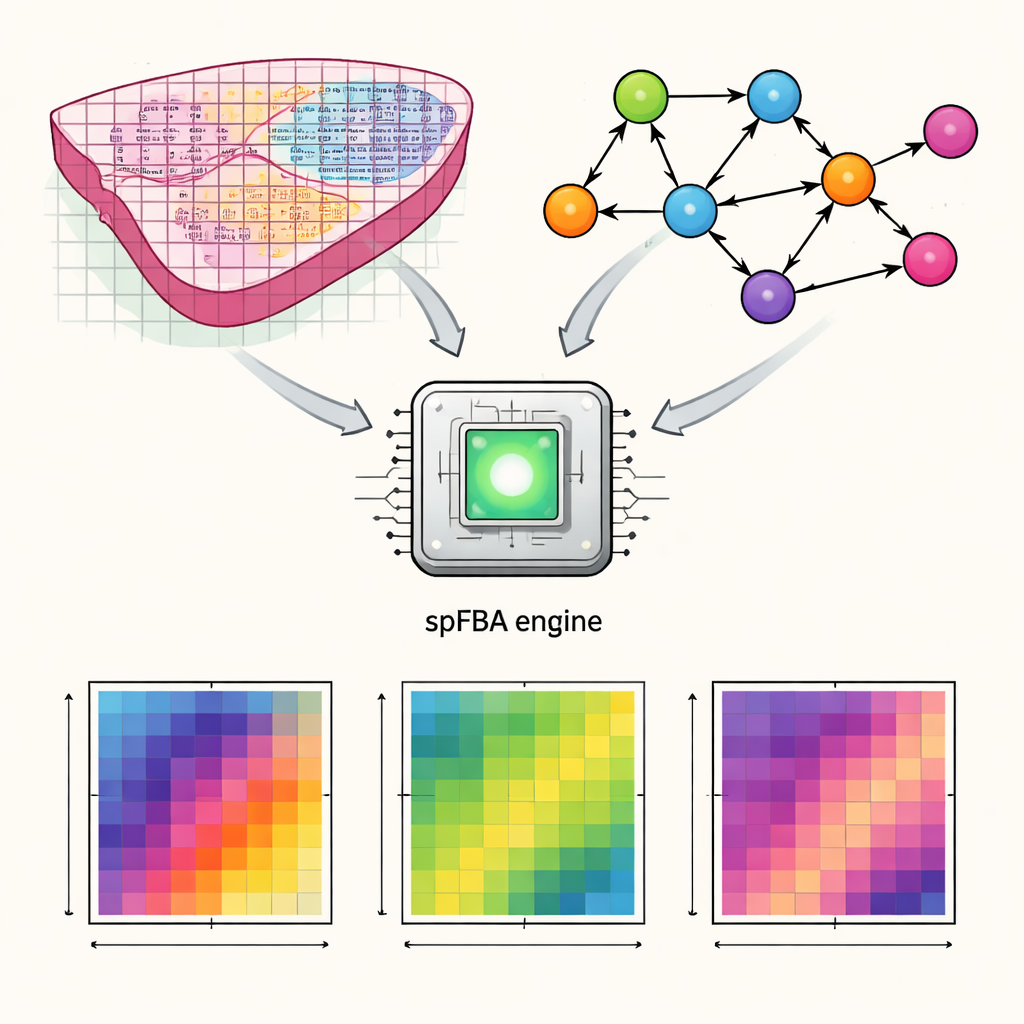
Transformando mapas gênicos em atividade metabólica
Os autores desenvolveram uma estrutura computacional chamada Análise de Balanço de Fluxo espacial, ou spFBA. Tecnologias de transcriptômica espacial medem quais genes estão ativos em milhares de pontos minúsculos ao longo de uma lâmina de tecido. O spFBA combina esses mapas de atividade gênica espacial com modelos detalhados do metabolismo humano, que descrevem como nutrientes como glicose, oxigênio e aminoácidos são transformados dentro das células. Em vez de assumir que todas as regiões de um tecido compartilham o mesmo objetivo metabólico, o spFBA trata cada ponto de forma independente, explorando quais padrões de reação são possíveis ali segundo as leis da química e do balanço de massa. A saída é um conjunto de “escores de enriquecimento de fluxo” que indicam, para cada local, quão fortemente diferentes reações metabólicas provavelmente fluem e em qual direção.
Testando o método em tumores renais
Para verificar se o spFBA produz resultados biologicamente plausíveis, a equipe recorreu primeiro ao carcinoma de células claras do rim, um câncer renal conhecido por depender fortemente da quebra do açúcar (glicólise) e da liberação de lactato, um fenômeno chamado efeito Warburg. Usando dados espaciais publicados de dez amostras de tumor renal, os autores perguntaram se os padrões metabólicos previstos correspondiam à estrutura conhecida do tecido. Eles descobriram que pontos agrupados segundo seus fluxos metabólicos inferidos se alinhavam bem com a organização histológica observada no microscópio e com agrupamentos baseados apenas na expressão gênica. Importante, o spFBA recuperou o contraste metabólico esperado entre tumor e tecido renal normal: as regiões tumorais exibiram maior uso de glicose, produção de biomassa mais intensa (um proxy para crescimento celular) e secreção robusta de lactato. Ao mesmo tempo, o uso de oxigênio permaneceu substancial, revelando que diferentes partes do mesmo tumor podem misturar fermentação e respiração dependendo do suprimento sanguíneo local.
Cânceres colorretais revelam uma história diferente sobre o lactato
Os pesquisadores então aplicaram o mesmo fluxo de trabalho a novos conjuntos de dados espaciais de alta resolução de um paciente com câncer colorretal primário e metástases hepáticas correspondentes, bem como a um conjunto de dados colorretal público e independente gerado com outra tecnologia. Aqui, os resultados foram marcadamente diferentes. Em vez de exportar lactato como resíduo, a maioria das regiões do câncer colorretal — tanto no tumor original do cólon quanto nas metástases hepáticas — foi prevista como importadora de lactato do entorno. Células estromais no tecido de suporte próximo tendiam a liberar pequenas quantidades de lactato, enquanto células tumorais agiam como fortes consumidoras. Ao rastrear padrões de fluxo ao nível das reações, os autores mostram que essas células metastáticas não simplesmente queimam lactato no ciclo energético usual dentro das mitocôndrias. Em vez disso, elas convertem o lactato em blocos de construção que alimentam vias para a síntese de lipídios e outros componentes necessários ao crescimento celular, um “pseudo–efeito Warburg reverso” em que o lactato se torna matéria-prima para biossíntese.
Nichos metabólicos e a fronteira tumor–estroma
Como o spFBA preserva a disposição espacial, ele pode identificar onde trocas metabólicas particulares ocorrem. Em tumores renais, o método revelou “bairros” metabólicos coexistentes: interfaces bem oxigenadas e ricas em sangue onde as células cancerosas tanto respiram quanto fermentam, e núcleos mais profundos e mal vascularizados que dependem mais fortemente da fermentação. Em metástases hepáticas colorretais, o spFBA destacou contrastes acentuados na fronteira entre tumor e estroma, onde o manejo de glutamato e lactato mudou de direção, sugerindo trocas intensas na frente invasiva. Em todos os conjuntos de dados, os fluxos previstos relacionados ao crescimento correlacionaram-se com medidas independentes baseadas em genes de proliferação, apoiando o realismo biológico do modelo. Crucialmente, o mesmo algoritmo previu secreção de lactato no câncer renal, mas captação de lactato no câncer colorretal, indicando que as diferenças observadas surgem dos dados, e não de um viés incorporado ao modelo.
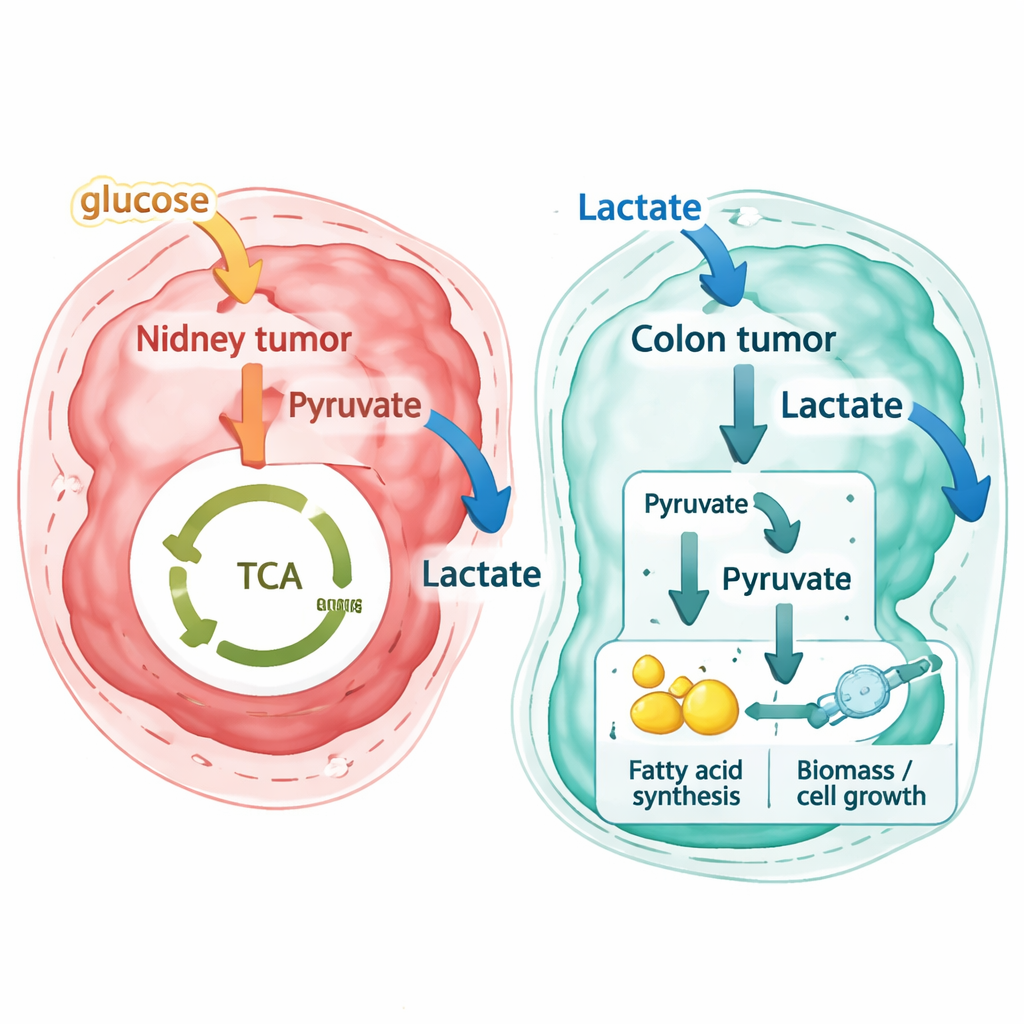
O que isso significa para entender e tratar o câncer
Para não especialistas, a mensagem-chave é que o metabolismo do câncer não é apenas anormal — ele também é fortemente local. O mesmo tumor pode abrigar múltiplos nichos metabólicos, e tumores de aparência semelhante em órgãos diferentes podem usar as mesmas moléculas de maneiras opostas. Este trabalho mostra que, ao sobrepor expressão gênica espacial a modelos metabólicos detalhados, os pesquisadores podem inferir onde os tumores provavelmente estarão carentes de nutrientes específicos, como o lactato. No câncer colorretal, a descoberta de que células tumorais consomem extensivamente lactato e o encaminham para processos relacionados ao crescimento levanta novas questões sobre como dieta, micróbios intestinais e o próprio metabolismo hepático influenciam a progressão da doença, e se bloquear o uso de lactato poderia tornar esses tumores mais vulneráveis à terapia.
Citação: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Palavras-chave: metabolismo do câncer, transcriptômica espacial, lactato, efeito Warburg, câncer colorretal