Clear Sky Science · pt
Análise de rede dinâmica revela acoplamentos de resíduos a longa distância na interface pMHC que fundamentam imunogenicidade aumentada
Como fragmentos virais minúsculos orientam nossas defesas imunológicas
Nossas células T citotóxicas patrulham o corpo em busca de sinais de infecção ou câncer. Fazem isso examinando pequenos fragmentos de proteína, chamados peptídeos, exibidos na superfície celular por moléculas conhecidas como MHC classe I. Este estudo faz uma pergunta sutil, mas importante: como uma única mudança pequena em um desses peptídeos pode fazer com que as células T respondam muito mais intensamente — ou nem respondam? A resposta envolve não apenas a estrutura estática, mas como todo o conjunto molecular se move e flexiona ao longo do tempo.
A fechadura, a chave e as peças móveis
Para entender o trabalho, ajuda imaginar o complexo peptídeo–MHC (pMHC) como uma fechadura e o receptor de célula T (TCR) como uma chave. O peptídeo se acomoda em uma ranhura na molécula de MHC e, juntos, formam a superfície que o TCR investiga. Pesquisas anteriores mostraram que tanto a sequência exata do peptídeo quanto a variante específica do MHC influenciam fortemente se uma célula T responde. Cientistas também criaram “ligantes de peptídeo alterados” que carregam pequenas modificações para ajustar respostas imunes, inclusive em imunoterapia contra o câncer. Mas, embora saibamos muito sobre as formas estáticas desses complexos, sabemos bem menos sobre como movimentos em um ponto do peptídeo podem afetar partes distantes da interface onde o TCR realmente se liga.
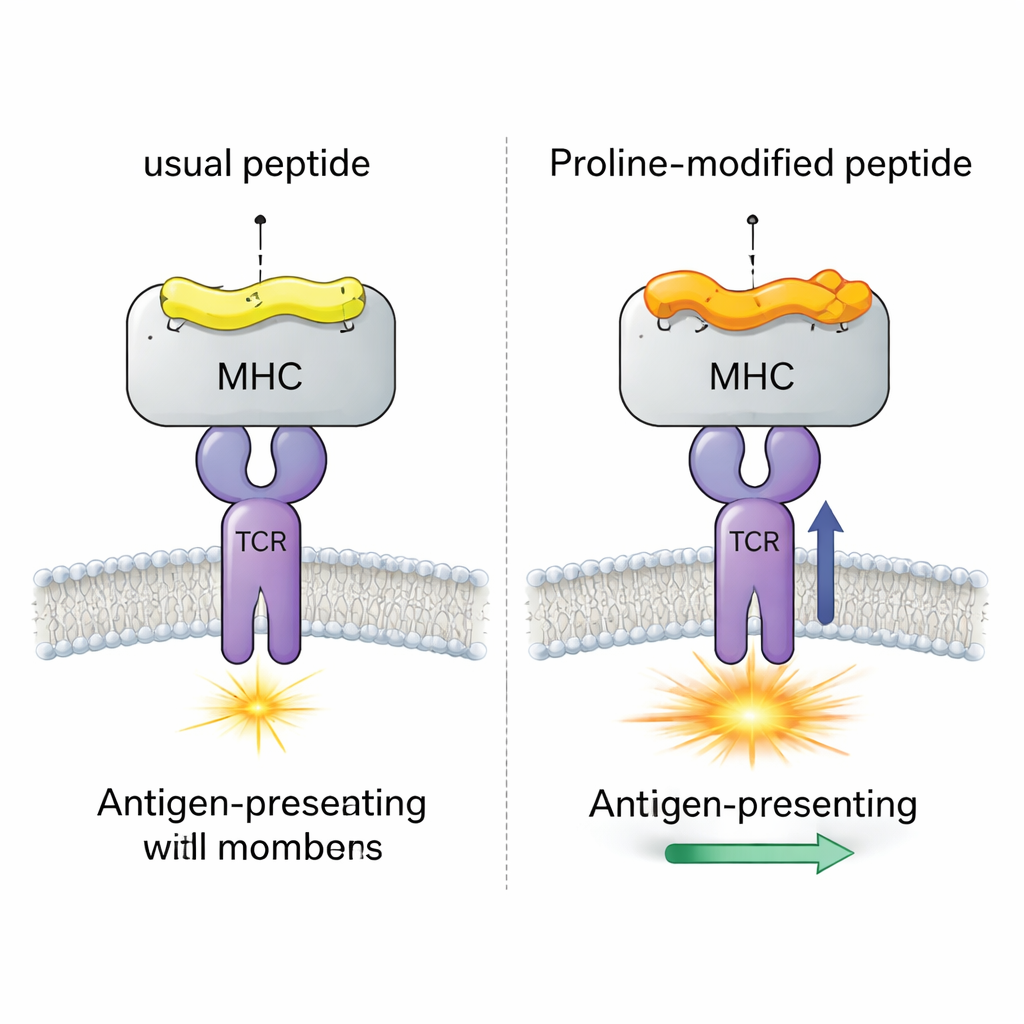
Um caso viral de teste com quatro peptídeos quase idênticos
A equipe concentrou-se em um sistema bem estudado de vírus de camundongo (LCMV) envolvendo o peptídeo gp33, que normalmente desencadeia fortes respostas de células T CD8+. Eles compararam quatro versões intimamente relacionadas desse peptídeo, todas ligadas à mesma molécula de MHC (H-2Db). Uma versão é o peptídeo viral original; outra carrega uma mutação de escape imune que as células T mal reconhecem; e duas são candidatas vacinais “alteradas por prolina”, onde um único aminoácido próximo ao início do peptídeo é trocado por prolina. Experimentos anteriores mostraram que essa troca por prolina aumenta a afinidade do complexo peptídeo–MHC e a intensidade da resposta de um TCR modelo (chamado P14), mas o mecanismo detalhado permaneceu obscuro.
Observando moléculas vibrar: simulações encontrando cristalografia
Para descobrir o que acontece, os autores combinaram estruturas cristalográficas de alta resolução com longas simulações computacionais átomo a átomo de cada complexo pMHC em movimento. Examinaram quanto cada resíduo de aminoácido flutua ao longo do tempo e como essas flutuações mudam quando a terceira posição do peptídeo é convertida em prolina. Ao correlacionar padrões de movimento por muitas simulações emparelhadas, construíram um “mapa dinâmico” de quais resíduos se movem juntos, mesmo quando estão distantes no espaço. Em seguida, transformaram esse mapa em uma rede, onde cada resíduo é um nó e as arestas representam movimentos estatisticamente ligados, e analisaram essa rede usando ferramentas de teoria dos grafos semelhantes às usadas em análise de redes sociais.
Comunicação à longa distância dentro da fechadura imunológica
A descoberta central é que alterar o terceiro resíduo do peptídeo para prolina faz mais do que simplesmente endurecer aquele ponto local. Isso muda como o movimento é transmitido ao longo de uma das hélices do MHC que contorna a fenda de ligação do peptídeo. Isso, por sua vez, afeta o comportamento de outro resíduo do peptídeo, a posição seis, que fica bem abaixo da área de contato do TCR e é crítica para o reconhecimento. Nas versões “boas” modificadas por prolina, esse resíduo explora uma gama mais ampla de conformações, incluindo as que são ótimas para a ligação ao TCR. Na variante de escape imune sem prolina, esse resíduo fica mais travado e raramente adota a orientação favorável ao TCR. A análise de rede revela que essa influência viaja através de aminoácidos específicos na ranhura do MHC, formando uma cadeia de resíduos dinamicamente acoplados que ligam o sítio da mudança por prolina à região de contato com o TCR.
Por que isso importa para vacinas e imunoterapia
Esses resultados mostram que a imunogenicidade — o quanto um peptídeo ativa células T — não é apenas sobre se as formas encaixam em um único momento, mas também sobre como o complexo respira e flexiona ao longo do tempo. Uma mudança sutil em uma posição pode reverberar por toda a rede molecular, fazendo com que resíduos de contato-chave tenham maior probabilidade de se apresentar em poses compatíveis com o TCR. O fluxo de trabalho computacional dos autores oferece uma forma de detectar sistematicamente esses acoplamentos de longa distância, o que pode ajudar a orientar o projeto de peptídeos alterados para vacinas e terapias contra o câncer. Em termos simples, eles demonstram que, escolhendo cuidadosamente onde mexer em um peptídeo, podemos empurrar toda a fechadura para um estado dinâmico mais “pronto para ser aberto” pela chave do sistema imunológico.
Citação: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Palavras-chave: reconhecimento por células T, peptídeo MHC, dinâmica de proteínas, ligantes de peptídeo alterados, imunogenicidade