Clear Sky Science · pt
Modelagem in silico da diferenciação do endoderma do intestino anterior em direção a progenitores epiteliais pulmonares
Transformando células-tronco em construtoras do pulmão
Cientistas estão aprendendo a induzir as próprias células-tronco de um paciente a se tornarem tecido pulmonar de reposição, o que um dia poderá reparar danos provocados por doenças como DPOC, fibrose ou infecções graves. Este artigo explora como pesquisadores usaram modelagem computacional para mapear e ajustar um passo crucial nessa trajetória: converter um tipo celular intermediário, chamado endoderma do intestino anterior, em progenitores epiteliais pulmonares precoces — as células iniciais que podem, eventualmente, formar as vias aéreas e os alvéolos do pulmão.
Por que as células iniciadoras pulmonares importam
Células-tronco pluripotentes induzidas humanas (iPSCs) podem ser reprogramadas a partir de tecidos adultos e então guiadas para se tornarem diferentes órgãos. Para construir tecido pulmonar, essas células passam primeiro por vários pontos de desenvolvimento. Um deles é o endoderma do intestino anterior, uma camada que normalmente dá origem a partes dos sistemas respiratório e digestivo no embrião. A partir daí, com os sinais químicos adequados, as células podem se tornar progenitores epiteliais pulmonares, que apresentam marcadores pulmonares iniciais e podem mais tarde amadurecer em células especializadas das vias aéreas ou alveolares. Como futuras terapias celulares exigirãom bilhões dessas células, os pesquisadores precisam de maneiras de aumentar confiavelmente os rendimentos e adaptar protocolos a diferentes linhagens celulares de pacientes sem depender de tentativas e erros intermináveis no laboratório.
Construindo uma versão virtual da diferenciação celular
A equipe expandiu uma estrutura matemática anterior para construir o que, segundo seu conhecimento, é o primeiro modelo em nível populacional dessa transição específica do endoderma para progenitores pulmonares. Eles consideraram duas formas de representar as células: uma versão simples que acompanha apenas o número total de células vivas, e uma versão mais detalhada que segue separadamente as células do endoderma anterior e os progenitores pulmonares. Em ambos os casos, o modelo também acompanha glicose e lactato no meio de cultura, representando nutrientes e resíduos. Usando ferramentas da biologia de sistemas, os pesquisadores construíram muitas equações candidatas sobre como as células crescem, morrem e se diferenciam, e então aplicaram testes de identificabilidade para descartar modelos cujos parâmetros nunca poderiam ser determinados, mesmo com dados perfeitos.
Projetando experimentos mais inteligentes com o modelo
Em vez de apenas ajustar o que quer que os dados disponíveis permitissem, os pesquisadores deixaram o modelo guiar como novos experimentos deveriam ser conduzidos. Eles usaram dados simulados para avaliar com que frequência precisariam medir números de células e níveis de nutrientes para estimar com precisão os parâmetros do modelo, equilibrando precisão estatística com o custo e o trabalho de amostragens frequentes. Isso os levou a um plano prático: medições diárias de glicose e lactato, e contagens celulares a cada um ou dois dias, sob quatro condições que variavam o grau de diluição das culturas no dia 10 e se o meio de crescimento era renovado diariamente. Em seguida, realizaram esses experimentos, medindo tanto a população celular total quanto, por citometria de fluxo, as frações que permaneceram como células do endoderma ou que se tornaram progenitores pulmonares.
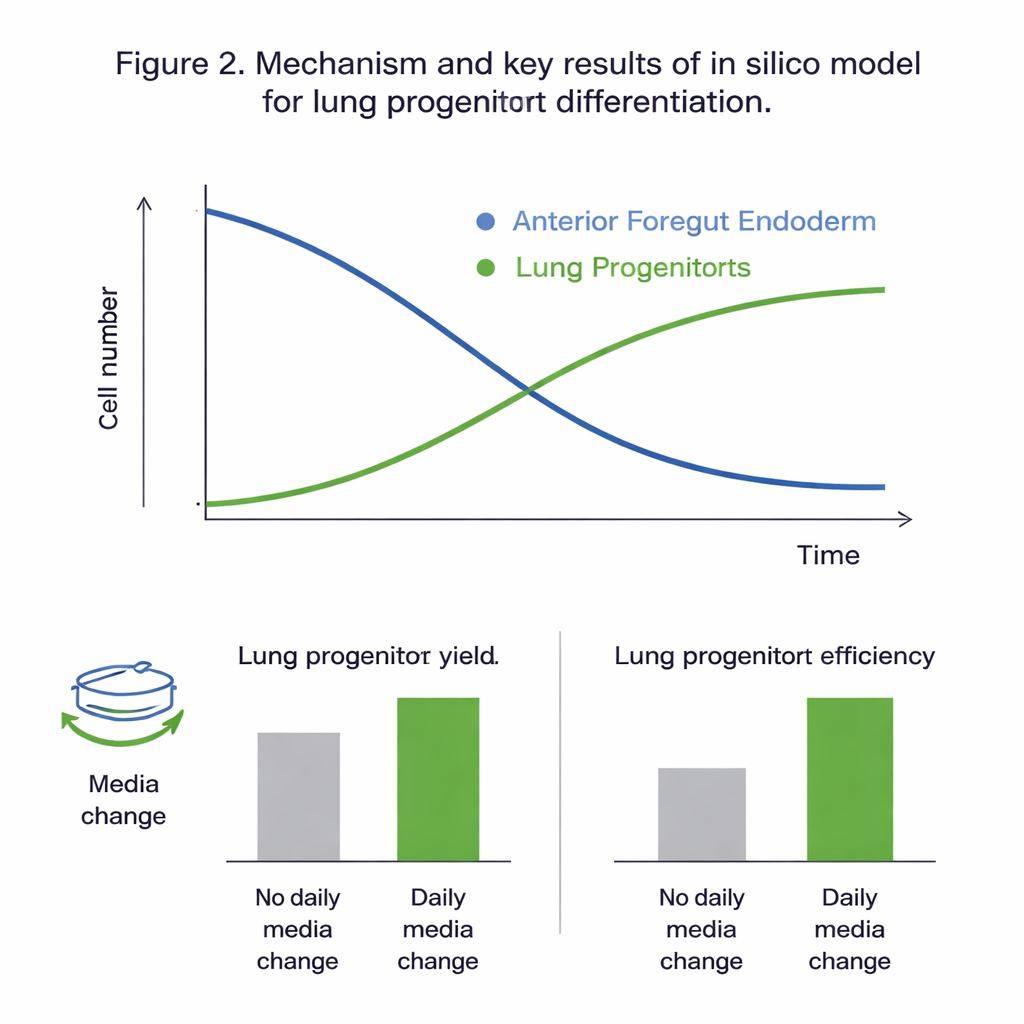
O que os experimentos virtuais revelaram
Ajustar todos os modelos candidatos aos dados experimentais mostrou que o modelo de duas populações, que acompanha separadamente células do endoderma e progenitores pulmonares, podia ser calibrado de forma confiável e capturou melhor o comportamento observado. Verificações estatísticas indicaram que, na janela temporal estudada (dias 11 a 15 do protocolo), a dinâmica foi conduzida principalmente pela proliferação e diferenciação das células do endoderma, enquanto a proliferação dos próprios progenitores pulmonares contribuiu pouco. A análise de sensibilidade global reforçou essa imagem, destacando as taxas de crescimento, morte e diferenciação das células do endoderma — e a influência da glicose — como as principais alavancas que controlam o resultado. O modelo calibrado reproduziu dados não usados na calibração com erros comparáveis à variabilidade natural dos experimentos, sugerindo que era preciso o suficiente para explorar cenários de “e se” in silico.
Otimização de trocas de meio e diluições celulares
Com um sistema virtual confiável em mãos, a equipe testou como duas escolhas práticas de protocolo afetam os resultados: quanto a cultura é diluída (razão de split) no dia 10, e se o meio de crescimento é substituído diariamente. As simulações previram que trocas diárias de meio quase dobram o número de progenitores pulmonares e o rendimento por célula inicial, principalmente evitando o esgotamento de nutrientes e o acúmulo de resíduos e moléculas sinalizadoras instáveis. Os experimentos concordaram de perto com essas previsões. O modelo também sugeriu que usar razões de split mais altas — espalhando as células mais diluídas no dia 10 — melhora o “rendimento por célula de entrada” em cerca de um quarto, embora reduza o número absoluto de células. Em ambos os casos, essas mudanças tiveram pouco efeito sobre a proporção final de progenitores pulmonares na cultura, influenciando principalmente quantas células podem ser produzidas de maneira eficiente.
O que isso significa para futuras terapias pulmonares
Para um público não especialista, a mensagem central é que os autores construíram uma espécie de simulador de voo para um passo crítico na obtenção de células pulmonares a partir de células-tronco. Ao combinar experimentos cuidadosamente projetados com modelagem matemática rigorosa, eles mostram como escolhas simples de protocolo — como a frequência de troca de meio de cultura e a densidade de semeadura — podem influenciar dramaticamente quantas células construtoras do pulmão são produzidas, sem alterar sua qualidade. Esse tipo de modelagem in silico pode ajudar a racionalizar protocolos futuros, reduzir o trabalho de tentativa e erro experimental e, em última instância, apoiar uma produção mais confiável e escalável de progenitores pulmonares para pesquisa, modelagem de doenças e, eventualmente, terapias regenerativas.
Citação: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Palavras-chave: células progenitoras pulmonares, células-tronco pluripotentes induzidas, modelagem in silico, diferenciação celular, medicina regenerativa