Clear Sky Science · pt
Associação entre alterações no número de cópias e o panorama transcriptômico imunológico no câncer
Por que nossos genes importam para a imunoterapia do câncer
A imunoterapia do câncer funciona ao ajudar o sistema imunológico a reconhecer e atacar tumores, mas apenas uma minoria dos pacientes obtém benefício duradouro. Este estudo faz uma pergunta básica com grandes consequências clínicas: como o caos genético dentro das células tumorais — em particular, grandes ganhos e perdas de DNA chamados alterações no número de cópias — molda a reação imune contra o câncer, e podemos inferir esses efeitos a partir de padrões de atividade gênica?
Uma visão panorâmica dos dados do câncer
Para enfrentar essa questão, os pesquisadores reuniram uma coleção enorme de 294.159 perfis de atividade gênica de tumores e outros tecidos. Esses perfis, obtidos a partir de vários grandes bancos de dados públicos, capturam quais genes estão ligados ou desligados em milhares de amostras que abrangem muitos tipos de câncer e condições experimentais. Em vez de analisar genes individualmente, a equipe usou um método matemático para decompor cada perfil em “componentes” subjacentes — padrões recorrentes de genes que tendem a subir e descer juntos, cada um refletindo um processo biológico como uma resposta imune ou o efeito de uma alteração no DNA.
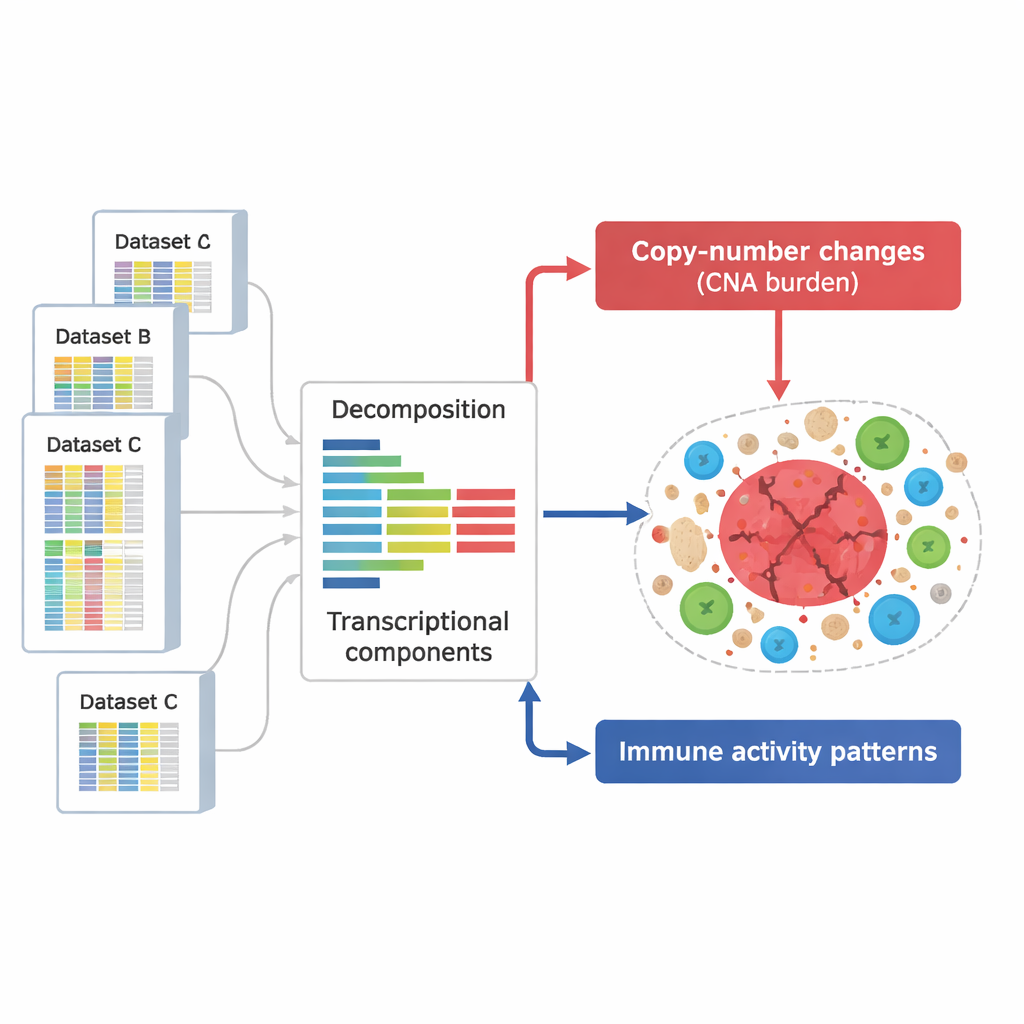
Separando sinais de dano ao DNA de sinais imunes
A partir desses componentes, os cientistas definiram dois grupos-chave. Um grupo capturou os efeitos das alterações no número de cópias — trechos de cromossomos que são repetidamente ganhos ou perdidos em células cancerosas. Esses padrões cobriram quase todo o genoma, indicando que a maioria das regiões afetadas por tais alterações deixou uma marca detectável na atividade gênica. Um segundo grupo de componentes foi enriquecido para genes envolvidos em funções imunes, como ativação de células T, atividade de células natural killer e apresentação de antígenos. No total, identificaram 657 componentes relacionados ao DNA e 283 componentes relacionados à imunidade, muitos dos quais puderam ser observados de forma reprodutível em conjuntos de dados e tecnologias independentes, sugerindo que representam características robustas e gerais da biologia tumoral.
Relacionando padrões à resposta ao tratamento
A equipe então investigou se esses padrões relacionados à imunidade poderiam ajudar a prever quem responde a inibidores de ponto de verificação imune, uma classe importante de drogas de imunoterapia do câncer. Usando dados de 13 estudos clínicos cobrindo 1.167 pacientes com sete tipos de câncer, treinaram modelos computacionais para distinguir respondedores de não-respondedores com base apenas na atividade dos componentes imunes em amostras tumorais pré-tratamento. Alguns modelos tiveram desempenho forte mesmo quando testados em grupos de pacientes completamente independentes; por exemplo, um modelo treinado em uma coorte de câncer de mama previu com precisão as respostas em uma coorte distinta de câncer de mama e apresentou desempenho útil em vários outros cânceres. Um pequeno conjunto de padrões imunes, incluindo aqueles ligados a respostas por interferon, células natural killer e ativação de células T, foi o que mais contribuiu para essas predições.
Como o caos genético remodela a imunidade tumoral
Com essa estrutura, os pesquisadores relacionaram sistematicamente a carga global de alterações no número de cópias — uma medida de quão extensivamente o DNA de um tumor é ganho ou perdido — à atividade de cada padrão imune em muitos tipos de câncer. A maioria dos padrões imunes mostrou uma relação inversa: tumores com alta carga de alterações no DNA tendiam a ter menor atividade de componentes associados a funções imunes benéficas, como apresentação de antígenos e infiltração por células imunes-chave. Contudo, uma minoria notável de padrões se movia na direção oposta. Tumores com alta carga de alterações frequentemente exibiam sinais aumentados de tipos celulares imunossupressores, incluindo células T regulatórias e certos macrófagos, bem como células inflamatórias que podem promover o crescimento tumoral em vez de sua destruição. Análises espaciais de cortes tumorais confirmaram que regiões com grandes alterações no DNA frequentemente coincidiam com baixa atividade de padrões imunes úteis e com zonas “imune-excluídas” onde as células imunes ficavam confinadas às margens do tumor.
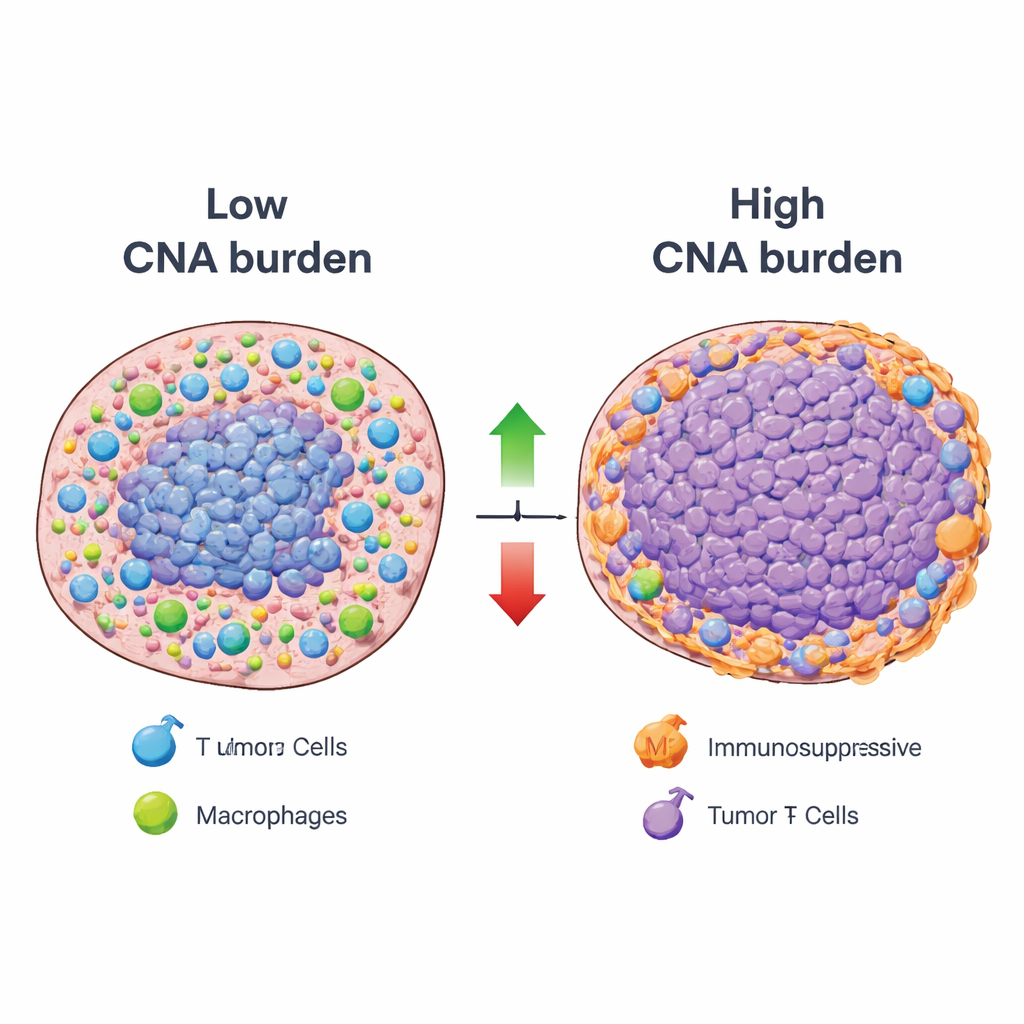
O que isso significa para o tratamento futuro do câncer
Em termos simples, o estudo mostra que tumores sobrecarregados por ganhos e perdas de DNA em larga escala tendem tanto a enfraquecer respostas imunes úteis quanto a fomentar ambientes imunes supressores ou promotores do tumor. Ainda assim, eles não são imunologicamente silenciosos; ao contrário, apresentam estados imunes específicos e recorrentes que podem ser vulneráveis a terapias direcionadas, como drogas que bloqueiam sinalizações de IL-17 ou IL-23 ou estratégias que reprogramam certos macrófagos. Ao mapear essas relações DNA–imunidade através dos cânceres e tornar o recurso publicamente disponível, o trabalho oferece um guia detalhado para por que alguns tumores geneticamente instáveis resistem às imunoterapias atuais e sugere novas estratégias de tratamento combinatório para ajudar o sistema imunológico a superar essa resistência.
Citação: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
Palavras-chave: imunoterapia do câncer, alterações no número de cópias, microambiente tumoral, inibidores de ponto de verificação imune, transcriptômica