Clear Sky Science · pt
Postbióticos alimentares de Lacticaseibacillus paracasei suprimem a formação de biofilme e a cariogenicidade de Streptococcus mutans oral
Combate às cáries com aliados à base de alimentos
A cárie dentária é um dos problemas de saúde mais comuns no mundo, impulsionada em grande parte por bactérias que se alimentam de açúcar e corroem nosso esmalte. Este estudo explora uma ideia emergente: em vez de depender apenas de enxaguantes bucais agressivos ou de “bactérias boas” vivas (probióticos), podemos proteger os dentes usando substâncias seguras e estáveis produzidas por microrganismos alimentares benéficos. Os pesquisadores mostram que postbióticos de uma bactéria alimentícia, Lacticaseibacillus paracasei, podem enfraquecer um importante agente causador de cáries e sua placa pegajosa, apontando para novos tipos de alimentos e enxaguantes para cuidados orais.
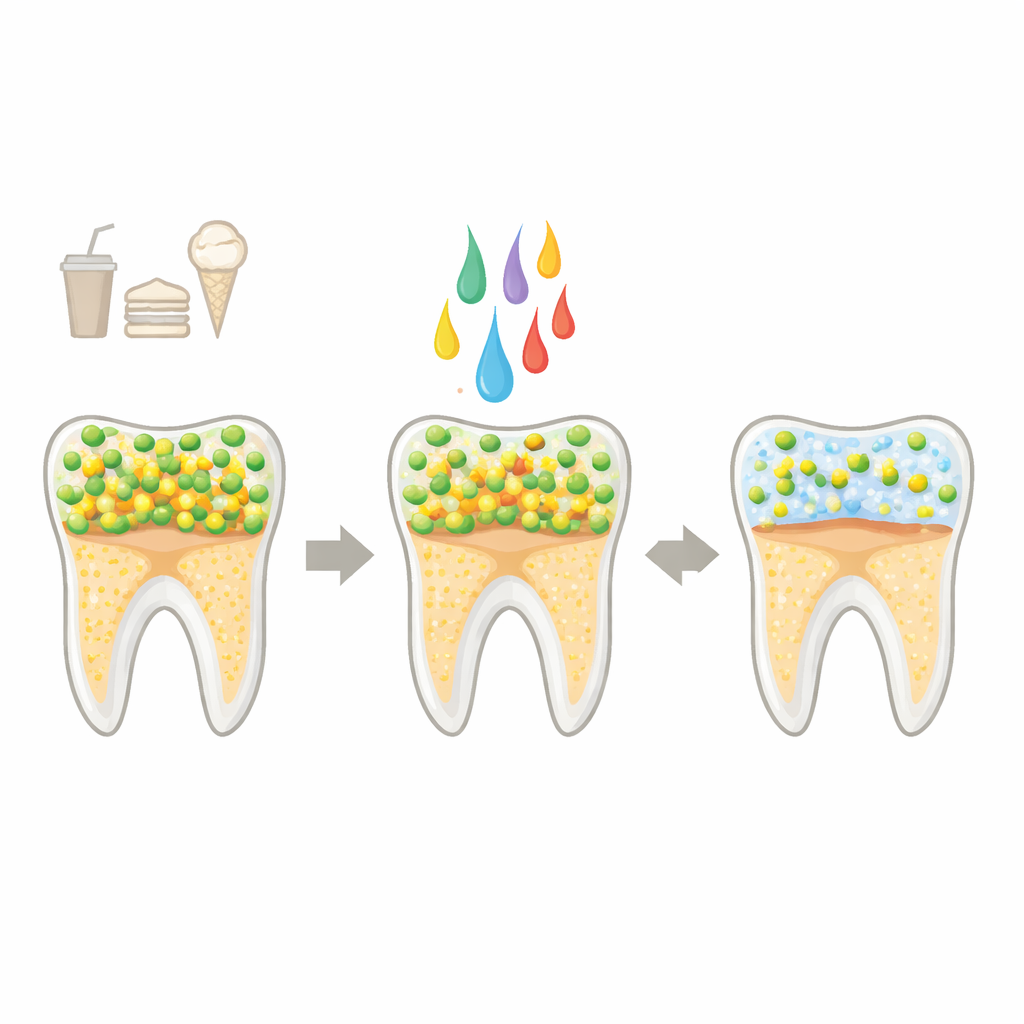
O culpado da cárie e um novo tipo de aliado
A cárie começa quando a comunidade microbiana normal da boca sai do equilíbrio. A ingestão frequente de açúcar alimenta bactérias produtoras de ácido, como Streptococcus mutans, que formam camadas espessas e semelhantes a cola (biofilmes) nos dentes. Esses biofilmes aprisionam ácidos contra o esmalte, dissolvendo minerais e eventualmente causando cáries. Escovar, usar fio dental e enxaguantes químicos ajudam, mas podem ser difíceis de aplicar perfeitamente todos os dias e podem causar efeitos colaterais. Produtos probióticos com bactérias vivas são promissores, mas levantam questões sobre estabilidade, armazenamento e segurança. Postbióticos — preparações não vivas feitas a partir de bactérias benéficas ou de seus componentes secretados — oferecem um caminho intermediário: podem ser de grau alimentício, duráveis e mais fáceis de manusear, ao mesmo tempo que direcionam microrganismos nocivos para um estado mais saudável.
Como os postbióticos enfraquecem bactérias orais nocivas
A equipe concentrou-se no sobrenadante sem células (CFS) de L. paracasei, essencialmente o caldo que resta após a remoção das bactérias. Eles testaram como esse líquido afetava S. mutans tanto em suspensão quanto em biofilmes. Em culturas de laboratório, o CFS quase interrompeu completamente a multiplicação de S. mutans. Ao microscópio eletrônico, as células tratadas pareciam murchas e danificadas, com superfícies ásperas e detritos. Medidas por citometria de fluxo confirmaram que suas membranas ficaram permeáveis, seu equilíbrio elétrico interno colapsou e muito poucas células permaneceram metabolicamente ativas. O CFS também tornou a superfície bacteriana menos repelente à água, o que é importante porque células mais hidrofóbicas aderem com mais facilidade aos dentes e entre si ao formar placa.
Decompondo a placa pegajosa e protegendo o esmalte
Quando S. mutans formou biofilmes, os postbióticos ainda tiveram um forte impacto. O CFS reduziu a massa total do biofilme, e uma forma concentrada o reduziu ainda mais. As bactérias dentro desses filmes cresceram mal, formaram cadeias mais curtas e produziram menos da cola açucarada (exopolissacarídeos) que dá estrutura à placa. Imagens tridimensionais mostraram biofilmes mais finos e irregulares, com menos células vivas e intactas e uma matriz enfraquecida. Para imitar dentes reais, os pesquisadores cultivaram S. mutans em discos de esmalte sintético revestidos com saliva humana e, em seguida, os submeteram a ciclos de “alimentação” e “enxágue” com CFS, um enxaguante padrão (clorexidina) ou uma solução controle. Os biofilmes tratados com CFS ficaram mais lisos e mais claros e — o mais importante — liberaram menos cálcio livre do esmalte, um sinal direto de menor desmineralização dental, embora o líquido ao redor permanecesse bastante ácido.
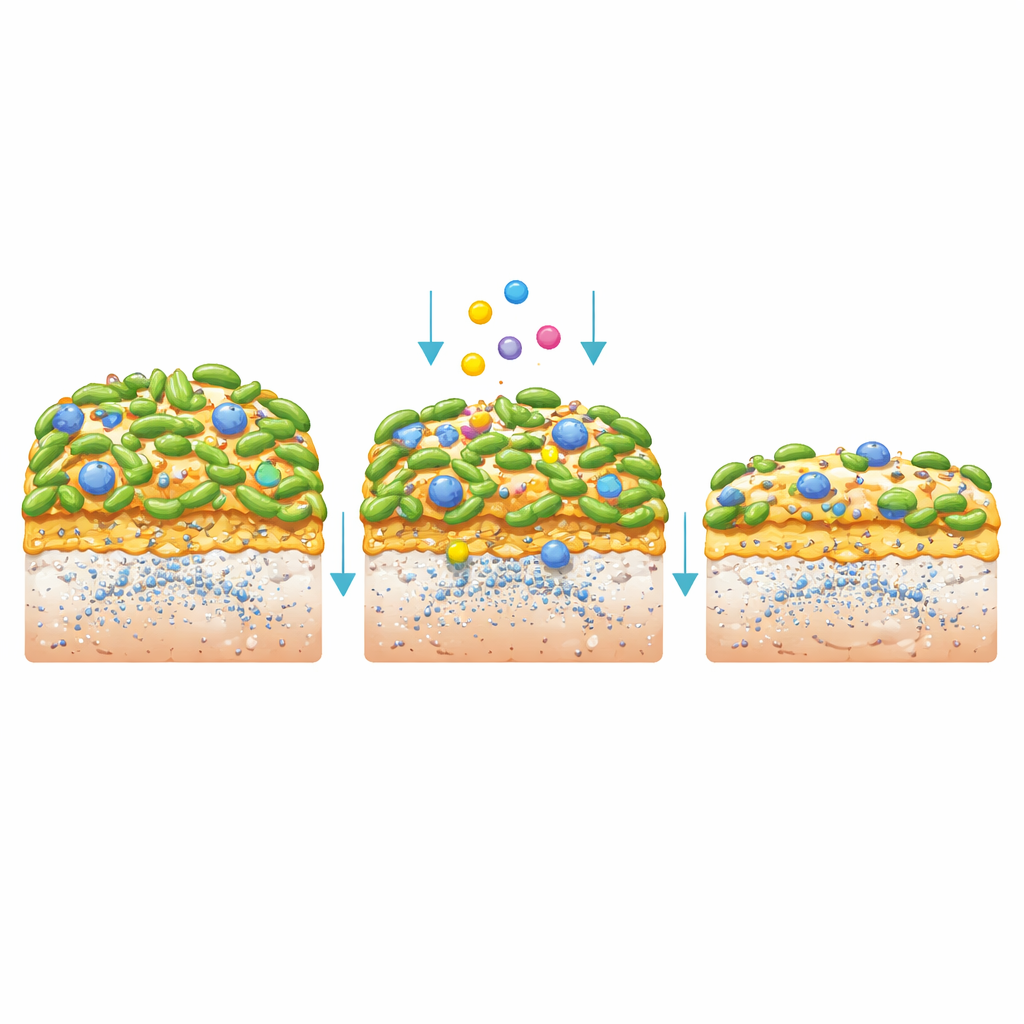
Investigando o manual molecular
Para descobrir o que no CFS estava atuando, os cientistas desativaram seletivamente componentes candidatas. Degradar proteínas, remover peróxido de hidrogênio ou adicionar açúcares extraídas do caldo pouco alterou seu efeito antibacteriano. Mas neutralizar sua acidez enfraqueceu fortemente seu poder, sugerindo que ácidos orgânicos eram os principais agentes. Esses ácidos foram mais do que simplesmente baixo pH: acidez similar criada apenas com ácido mineral não suprimiu S. mutans tão bem, indicando misturas específicas de ácidos orgânicos atuando em conjunto. A equipe então examinou quais genes bacterianos e pequenas moléculas mudaram quando S. mutans cresceu com CFS. Eles encontraram atividade reduzida em genes ligados à adesão, produção de cola, resistência ao estresse e sistemas de “conversa” bacteriana (quorum sensing) que coordenam o comportamento grupal. Certos metabólitos, como creatina e fosfoenolpiruvato, mudaram de maneiras compatíveis com menor produção de ácido e virulência reduzida, ajudando a explicar por que menos mineral do esmalte foi perdido.
O que isso pode significar para cuidados orais do dia a dia
Em termos simples, este trabalho mostra que postbióticos seguros e de grau alimentício de L. paracasei podem abrir brechas na armadura de uma bactéria chave causadora de cáries, afinando sua placa, enfraquecendo suas defesas e reduzindo o dano ácido a superfícies semelhantes ao esmalte. Como esses postbióticos são estáveis ao calor, ao armazenamento e a uma gama de condições, eles poderiam ser incorporados em pastilhas, enxaguantes ou alimentos funcionais como um auxílio suave e duradouro, aliado à escovação e ao uso do fio dental. Embora não substituam uma boa higiene oral ou visitas regulares ao dentista, apontam para um futuro em que ingredientes inteligentes derivados de alimentos remodelam discretamente a comunidade microscópica da boca para manter os dentes mais fortes por mais tempo.
Citação: Luo, SC., Hu, PF., Wei, SM. et al. Food-grade Lacticaseibacillus paracasei postbiotics suppress oral Streptococcus mutans biofilm formation and cariogenicity. npj Sci Food 10, 89 (2026). https://doi.org/10.1038/s41538-026-00742-6
Palavras-chave: cárie dentária, microbioma oral, postbióticos, Streptococcus mutans, alimentos funcionais