Clear Sky Science · pt
Licopeno mitiga a ferroptose hepática induzida pela toxina T-2 ao alvejar o eixo Nrf2/mitofagia em camundongos
Por que uma toxina de molde em grãos do dia a dia importa
Muitos alimentos básicos, incluindo trigo e milho, podem ser contaminados por uma toxina produzida por fungos chamada toxina T-2. Esse contaminante invisível sobrevive ao cozimento e ao processamento, e a exposição prolongada pode danificar silenciosamente órgãos vitais, especialmente o fígado. O estudo resumido aqui investiga duas questões urgentes: como exatamente a toxina T-2 prejudica o fígado e um composto natural presente nos alimentos — o licopeno, o pigmento vermelho de tomates e outras frutas — pode ajudar a proteger contra esse dano?
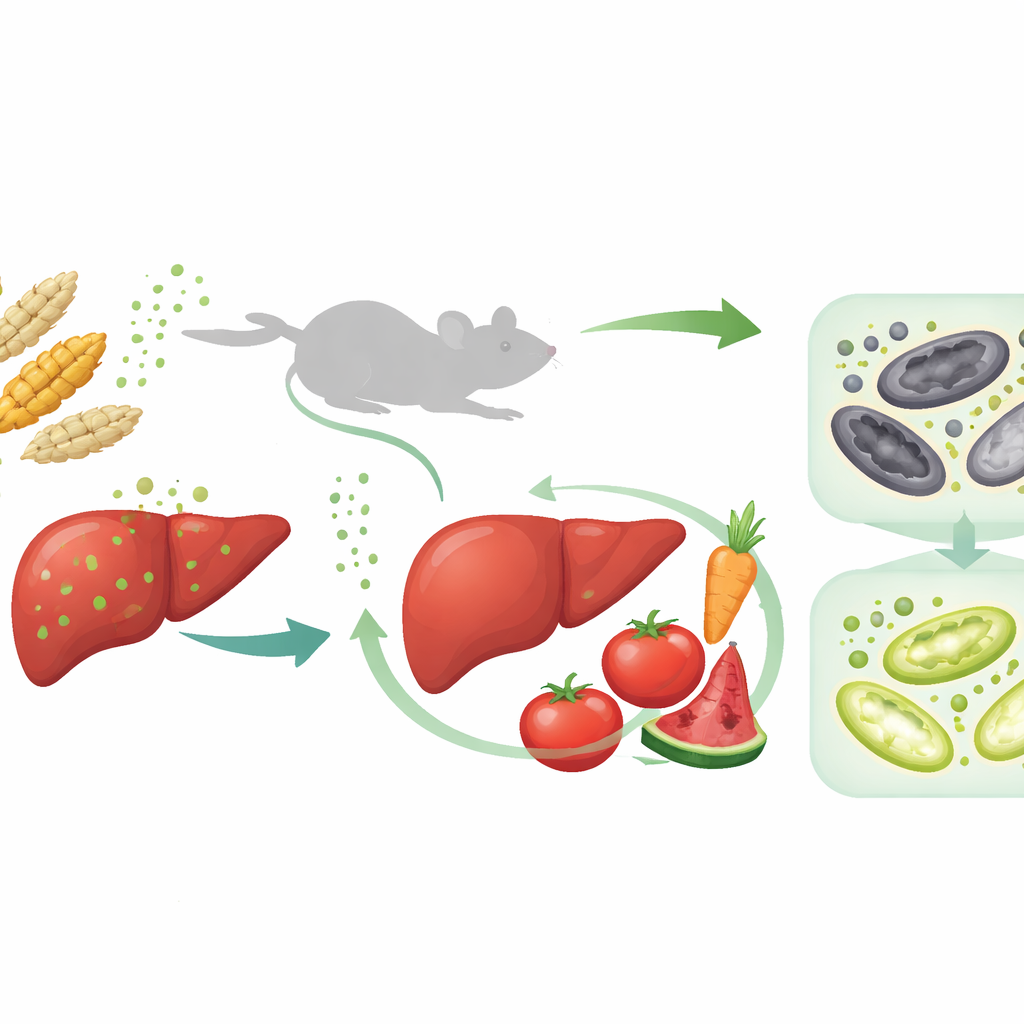
Como a toxina prejudica o fígado
Os pesquisadores primeiro alimentaram camundongos com doses graduais de toxina T-2 por quatro semanas para imitar a exposição dietária contínua. À medida que os níveis da toxina aumentaram, os animais ganharam menos peso, seus fígados ficaram aumentados e amarelados, e exames de sangue mostraram níveis crescentes de enzimas hepáticas indicativas de lesão. Ao microscópio, o tecido hepático parecia inchado e desorganizado, com vacúolos dentro das células e sinais de morte celular. Uma pesquisa ampla de proteínas das amostras de fígado revelou que muitas das vias mais alteradas estavam relacionadas ao manejo do ferro, ao metabolismo de lipídios e a uma forma específica de morte celular chamada ferroptose, que é dirigida pelo ferro e pela oxidação desenfreada de gorduras.
Sobrecarga de ferro e uma morte celular semelhante à ferrugem
Aprofundando-se, a equipe mediu marcadores clássicos de ferroptose. Nos fígados expostos à toxina, o conteúdo de ferro aumentou, enquanto moléculas que indicam dano lipídico cresceram e a atividade de uma enzima protetora chave, a GPx-4, caiu. Proteínas que normalmente armazenam ferro com segurança dentro das células aumentaram, mas o principal “exportador” de ferro nas células hepáticas diminuiu, sugerindo que o ferro estava ficando preso internamente. Quando os cientistas administraram a alguns camundongos um fármaco que bloqueia especificamente a ferroptose, a estrutura e a função hepáticas melhoraram: o inchaço foi reduzido, as pontuações de lesão caíram e os sinais químicos de dano oxidativo aliviaram. Isso vinculou firmemente a toxicidade hepática da toxina T-2 a uma forma de morte celular semelhante à ferrugem, dirigida pelo ferro.
Mitocôndrias, limpeza celular e um interruptor de defesa
A equipe então voltou sua atenção para as mitocôndrias, as usinas de energia dentro das células, que são tanto fonte quanto alvo do estresse oxidativo. Em camundongos tratados com a toxina, a produção de energia mitocondrial caiu enquanto o vazamento de citocromo c e as espécies reativas de oxigênio aumentaram, e a microscopia eletrônica mostrou mitocôndrias encolhidas e estruturalmente danificadas. Ao mesmo tempo, o sistema de controle de qualidade da célula — a mitofagia, um processo seletivo de “limpeza” que remove mitocôndrias defeituosas — foi ativado por uma via envolvendo as proteínas PINK1 e Parkin. Quando os pesquisadores usaram camundongos sem Parkin, incapazes portanto de montar a mitofagia normalmente, a toxina T-2 provocou acúmulo de ferro ainda maior, sinais de ferroptose mais intensos e dano hepático mais grave. Isso mostrou que a mitofagia atua como um freio protetor, limitando a lesão induzida pela toxina.
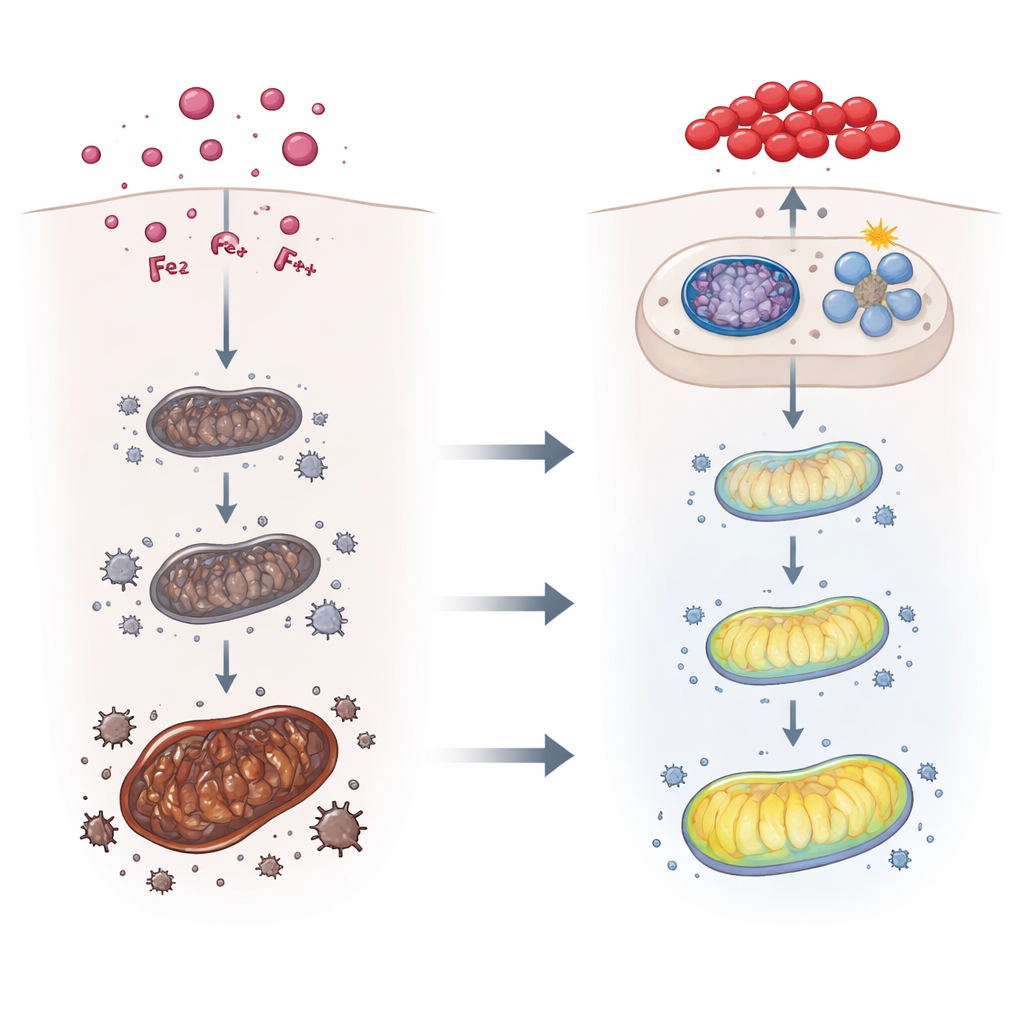
Uma via de proteção embutida e o papel do licopeno
Como o equilíbrio do ferro, o estresse oxidativo e a mitofagia pareciam interligados, os autores buscaram um controlador a montante e focaram no Nrf2, um interruptor mestre que ativa genes antioxidantes e de detoxificação. A própria toxina T-2 ativou parcialmente o Nrf2, mas quando camundongos receberam um composto conhecido por ativar o Nrf2, a exportação de ferro hepático melhorou, os marcadores de ferroptose diminuíram e a mitofagia aumentou, tudo contribuindo para amaciar o impacto da toxina. A equipe então investigou se o licopeno poderia atuar como um potenciador natural do Nrf2. Modelagem computadorizada sugeriu que o licopeno pode se ligar fisicamente tanto ao Nrf2 quanto à sua proteína repressora Keap1 de maneiras que favoreceriam a ativação do Nrf2. Em camundongos vivos, o tratamento com licopeno antes e durante a exposição à toxina melhorou o peso corporal, restaurou a aparência do fígado e os exames de sangue, reduziu o acúmulo de ferro e o dano oxidativo, e ativou ainda mais o Nrf2 e a via de mitofagia PINK1–Parkin.
O que isso significa para segurança alimentar e dieta
Em termos simples, o estudo mostra que a toxina T-2 prejudica o fígado ao aprisionar ferro em excesso dentro das células, destruir mitocôndrias e desencadear ferroptose. O organismo responde ativando Nrf2 e mitofagia para eliminar mitocôndrias danificadas e reequilibrar o ferro, mas essa defesa pode ser sobrecarregada. O licopeno parece fortalecer esse escudo interno, ajudando o fígado a exportar ferro, limpar mitocôndrias defeituosas e resistir à morte celular ferroptótica. Embora mais pesquisas sejam necessárias antes de traduzir essas descobertas para humanos, a pesquisa sugere que certos compostos vegetais, como o licopeno, poderiam um dia fazer parte de estratégias para reduzir o impacto à saúde de toxinas alimentares inevitáveis.
Citação: Yang, X., Song, W., Lu, Z. et al. Lycopene mitigates T-2 toxin-induced hepatic ferroptosis by targeting the Nrf2/mitophagy axis in mice. npj Sci Food 10, 94 (2026). https://doi.org/10.1038/s41538-026-00736-4
Palavras-chave: toxina T-2, licopeno, lesão hepática, ferroptose, mitofagia