Clear Sky Science · pt
Metabolômica auxiliada por aprendizado de máquina decodifica a remodelação adaptativa de biofilmes de Bacillus em resposta ao estresse da pasteurização
Por que quem bebe leite deveria se importar
O leite pasteurizado é pensado para ser seguro e ter longa duração, ainda que algumas bactérias resistentes possam sobreviver ao tratamento térmico e silenciosamente formar comunidades mucosas — chamadas biofilmes — dentro dos equipamentos de processamento. Este estudo faz uma pergunta inquietante com consequências práticas: a pasteurização às vezes pode tornar esses biofilmes piores e, se sim, quais mudanças químicas internas às bactérias são responsáveis?
Micróbios persistentes em laticínios modernos
O leite é rico em nutrientes e sustenta uma indústria próspera de produtos lácteos refrigerados e de baixa temperatura. Mas também é um ambiente para Bacillus, um grupo de bactérias que formam esporos resistentes e aderem a superfícies metálicas. Esses micróbios constroem biofilmes — camadas protetoras de células e material tipo cola — que resistem à limpeza, reduzem a transferência de calor e aumentam o risco de deterioração ou até de doenças transmitidas por alimentos. Os autores coletaram 14 cepas de Bacillus de leite cru em fazendas chinesas e testaram sua capacidade de formar biofilmes antes e depois de uma etapa simulada de pasteurização a 75 °C por 15 segundos. Surpreendentemente, enquanto muitas cepas formaram biofilmes mais fracos após o aquecimento, várias na verdade ficaram mais fortes e pegajosas.
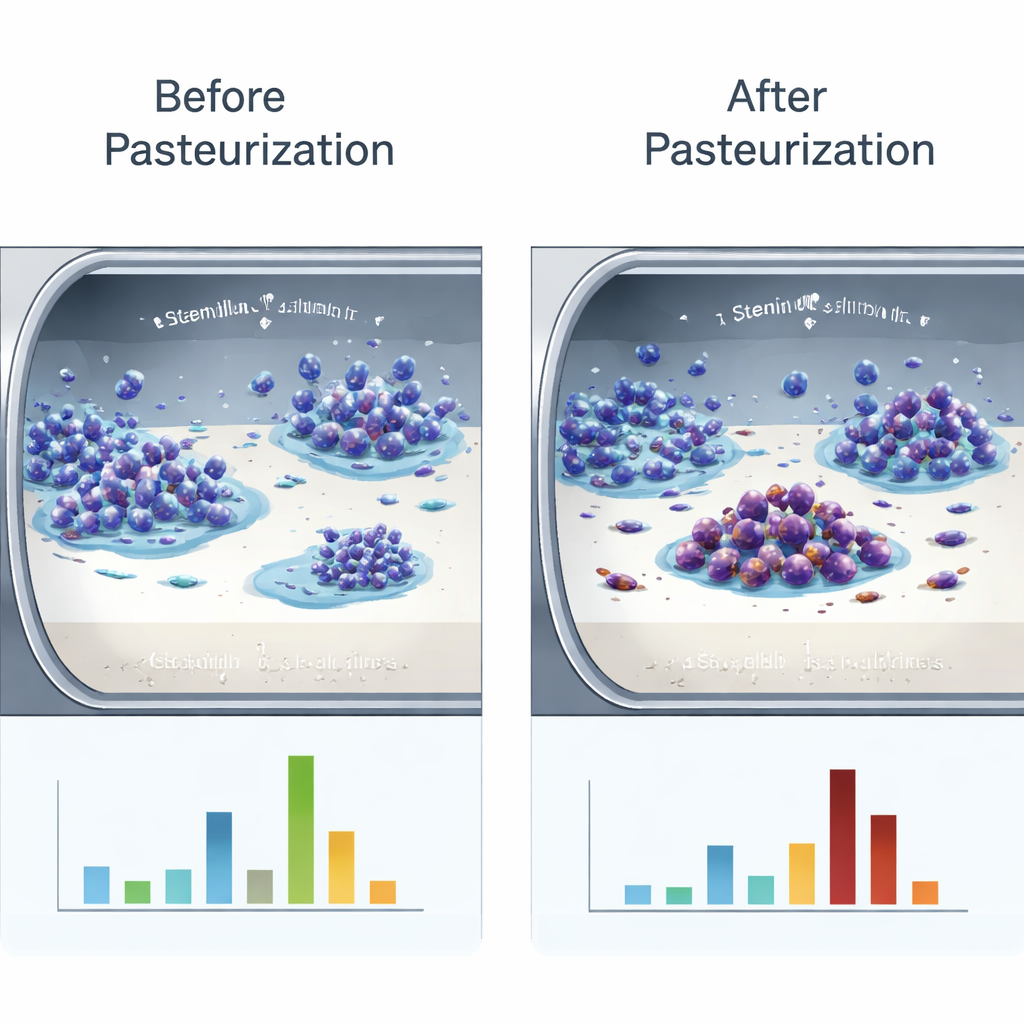
Calor que ajuda alguns biofilmes, prejudica outros
Para imitar equipamentos reais de laticínios, os pesquisadores cultivaram cepas selecionadas em coupons de aço inoxidável 304 banhados em leite estéril. Em seguida, tingiram e mediram a sujeira total — bactérias mais resíduos do leite — deixada no metal. Duas cepas, uma de Bacillus cereus (BC01) e outra de Bacillus subtilis (BS01), passaram de fraca para fortemente adesivas após a pasteurização, enquanto parentes próximos (BC02 e BS02) mostraram a tendência oposta. Imagens em microscópio eletrônico revelaram como a arquitetura do biofilme mudou: nas cepas reforçadas pelo calor, a malha fibrosa fina habitual de substâncias poliméricas extracelulares fundiu‑se em agregados espessos e em blocos que aprisionaram mais células e proteínas do leite, formando um revestimento mais resistente e extenso. Nas cepas enfraquecidas pelo calor, a matriz tornou‑se esparsa e fragmentada.
Quando a aderência superficia quebra as regras
A sabedoria convencional sustenta que quanto mais repelente de água (hidrofóbico) um esporo é, melhor ele adere e mais facilmente um biofilme se forma. A equipe testou a hidrofobicidade dos esporos usando um sistema óleo‑água e encontrou o oposto do que os livros dizem. Após a pasteurização, as cepas que ganharam força no biofilme mostraram na verdade menor hidrofobicidade de esporos, enquanto aquelas que perderam capacidade de biofilme se tornaram mais hidrofóbicas. Mesmo dentro dos biofilmes, os esporos de formadores fortes eram menos hidrofóbicos do que seus equivalentes livres. Essa contradição apontou para um motor mais profundo: mudanças induzidas pelo calor no metabolismo e na atividade gênica que podem sobrepujar propriedades físicas simples como a aderência superficial.
Reconfiguração química sob estresse térmico
Usando metabolômica não direcionada — um levantamento amplo de pequenas moléculas dentro das células — combinado com análise por aprendizado de máquina, os autores mapearam como o calor remodelou a química do biofilme de cada cepa. As quatro cepas mostraram grandes mudanças em centenas de metabólitos, especialmente em sistemas de transporte e vias de aminoácidos, mas os detalhes diferiram acentuadamente. Em BC01, o aquecimento pareceu ativar uma enzima chamada glutaminase, esvaziando a reserva do nutriente do leite L‑glutamina e do aminoácido histidina. Essa mudança forneceu blocos de construção para a matriz do biofilme e removeu freios naturais à formação de biofilmes. Os níveis de xantosina, um composto que normalmente afasta as bactérias dos biofilmes, também caíram, provavelmente favorecendo um estilo de vida aderido e estável. Em BS01, o calor reduziu a arginina e vários D‑aminoácidos, dopamina e ácido aracidônico — moléculas conhecidas por outros estudos por desestabilizar biofilmes ou bloquear sua formação. Quantidades menores desses inibidores, junto com o metabolismo energético alterado, ajudaram a inclinar o equilíbrio para biofilmes mais robustos. Em contraste, BC02 e BS02 sofreram carências de precursores polissacarídicos essenciais e componentes do ciclo de energia, e em BS02, metabólitos anti‑biofilme como D‑triptofano e D‑arabinose aumentaram, minando coletivamente o crescimento do biofilme.
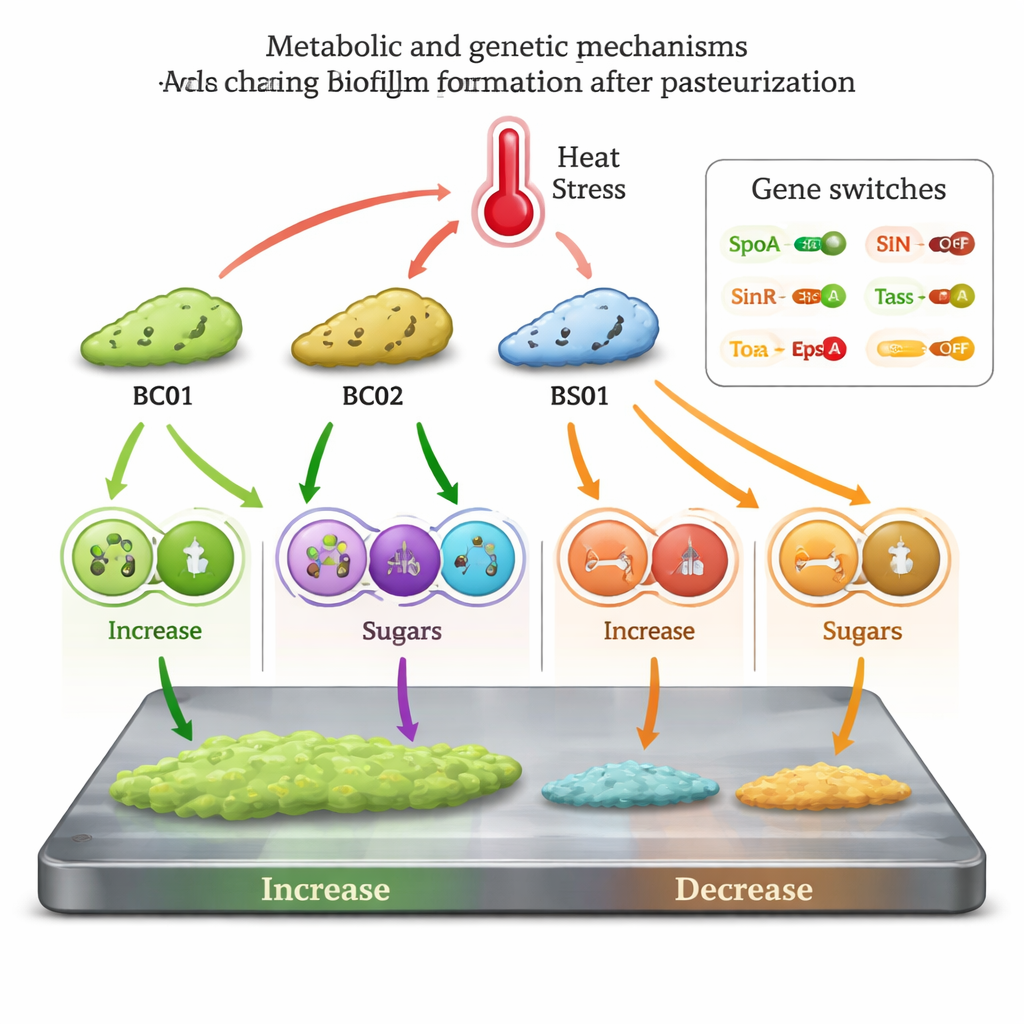
Genes que viram o interruptor do biofilme
Para ligar a química ao comportamento, a equipe mediu genes-chave relacionados ao biofilme. Nas cepas fortalecidas pelo calor BC01 e BS01, reguladores mestres que promovem a formação de biofilme (Spo0A, TasA e EpsA) foram ativados, enquanto SinR, um gene que normalmente mantém os genes do biofilme sob controle, foi rebaixado. O padrão oposto apareceu em BC02 e BS02. Em conjunto, os dados metabólicos e as leituras gênicas sustentam um modelo no qual a pasteurização atua como um sinal de estresse que algumas linhagens de Bacillus exploram: elas reprogramam seu metabolismo, reduzem certos metabólitos naturais anti‑biofilme e acionam interruptores genéticos para produzir mais matriz e revestimentos mais espessos, mesmo quando sua atividade global diminui.
O que isso significa para um leite mais seguro
Para os consumidores, a mensagem não é que o leite pasteurizado seja inseguro, mas que os micróbios que sobrevivem ao tratamento térmico podem ser mais adaptáveis do que se espera. Em vez de apenas endurecer esporos, a pasteurização pode empurrar algumas cepas de Bacillus para um modo de “refúgio” em que constroem biofilmes mais fortes dentro de tubos e tanques. Ao identificar metabólitos e vias gênicas específicas que impulsionam essa mudança, o estudo sugere novas formas de contra‑ataque: em vez de depender apenas de temperaturas mais altas ou tempo maior de aquecimento, os processadores poderiam, no futuro, adicionar bloqueadores metabólicos benignos ou ajustar regimes de limpeza que desestabilizem o sistema químico de suporte desses biofilmes. Em essência, entender como o calor remodela a química bacteriana abre caminho para estratégias mais inteligentes de manter os produtos lácteos nutritivos e realmente limpos.
Citação: Liang, L., Wang, P., Zhao, X. et al. Metabolomics aided by machine learning decodes adaptive remodeling of Bacillus biofilms in response to pasteurization stress. npj Sci Food 10, 62 (2026). https://doi.org/10.1038/s41538-026-00712-y
Palavras-chave: leite pasteurizado, biofilmes de Bacillus, segurança alimentar, processamento de laticínios, metabolismo bacteriano