Clear Sky Science · pt
Inibição de CDK8 resgata a cicatrização óssea prejudicada por isquemia
Por que o fluxo sanguíneo importa quando os ossos se quebram
A maioria dos ossos quebrados eventualmente se recompõe, mas para milhões de pessoas a cada ano esse processo emperra. O fluxo sanguíneo insuficiente ao redor de uma fratura — conhecido como isquemia — aumenta drasticamente o risco de que a fratura cicatrize lentamente, de forma deficiente ou não cicatrize. Este estudo investiga por que isso acontece no nível celular e testa uma pílula experimental que parece orientar o organismo para longe da reparação semelhante a cicatriz e de volta à verdadeira regeneração óssea.
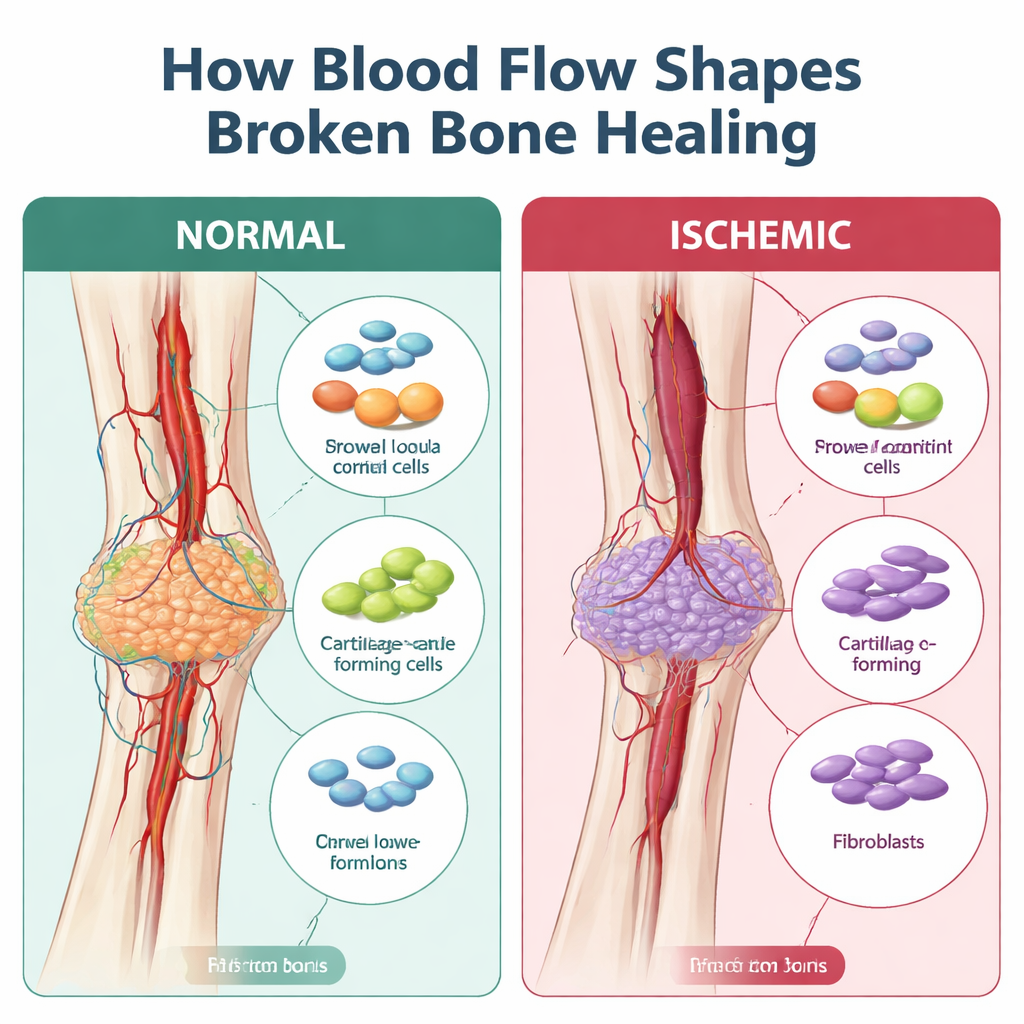
Quando a cura vira cicatriz em vez de reconstrução
O osso normalmente cicatriza formando uma ponte macia de cartilagem que é gradualmente substituída por osso duro. Essa ponte, chamada calo, depende de um suprimento de células de suporte semelhantes a células-tronco, células imunes e vasos sanguíneos que coordenam a reparação. Em fraturas isquêmicas, trabalhos anteriores mostraram que o calo tende a ser menor, mais fraco e preenchido por tecido fibroso, mais parecido com uma cicatriz do que com um remendo robusto de osso novo. O que faltava era um mapa detalhado de quais células falham, e quando, durante esse desvio da cicatrização adequada.
Células únicas revelam um desvio para a fibrose
Os pesquisadores usaram um modelo de camundongo em que uma artéria da perna é danificada cirurgicamente no momento da fratura, imitando de perto a perda de fluxo sanguíneo vista em lesões graves ou em pessoas com doença vascular ou fumantes. Em seguida aplicaram seqüenciamento de RNA de célula única, uma técnica que lê os genes ativos em milhares de células individuais, aos calos de fratura quatro e sete dias após a lesão. Em fraturas bem perfundidas, o calo inicial estava repleto de células imunes que logo deram lugar à expansão de células estromais — as células de suporte que se tornam cartilagem e osso. Em condições isquêmicas, porém, havia muito menos células formadoras de cartilagem e osso e muitas mais fibroblastos, as células que depositam tecido fibroso. Análises computacionais de “trajetória” mostraram que, em vez de maturarem suavemente de progenitores iniciais em cartilagem, as células estromais em ossos isquêmicos frequentemente desviavam por um estado semelhante ao de fibroblastos, correspondendo ao calo mais parecido com cicatriz observado ao microscópio.
Um freio molecular nas células formadoras de osso
Aprofundando-se na atividade gênica dessas células, a equipe encontrou um forte sinal de estresse celular nos calos isquêmicos, incluindo níveis elevados de proteínas de choque térmico. Entre as mudanças mais marcantes houve um aumento da atividade de um gene chamado Cdk8, que codifica uma enzima reguladora presente em um importante complexo de transcrição e que pode desacelerar ou redirecionar como as células respondem a sinais. Já se sabia que Cdk8 pode bloquear a diferenciação celular em outros contextos. Aqui, estava especialmente elevado em progenitores estromais iniciais em osso isquêmico. Células estromais mesenquimais humanas cultivadas em condições de baixo oxigênio — mimetizando o fluxo sanguíneo deficiente — também aumentaram a expressão de CDK8, ligando diretamente a falta de oxigênio a esse potencial “freio” sobre a formação de cartilagem e osso.
Desligando o CDK8 para resgatar a reparação
Os pesquisadores então perguntaram se bloquear o CDK8 poderia liberar as células estromais para retomar a cicatrização adequada. Em cultura celular, tratar progenitores de camundongo e humanos com inibidores seletivos de CDK8 aumentou genes-chave da cartilagem e elevou a produção de matriz cartilaginosa, além de melhorar a mineralização quando as mesmas células foram induzidas a se tornar osso. A equipe então testou um inibidor oral de CDK8/19 chamado SNX631-6 em camundongos com fraturas isquêmicas. Quando administrado durante a janela inicial de formação de cartilagem, a droga aumentou a quantidade de cartilagem no calo. Quando o tratamento foi estendido para a transição posterior de cartilagem para osso, os calos mostraram mais osso total, maior conteúdo mineral e tamanho geral maior em exames de micro–TC e em cortes de tecido, indicando uma reparação estrutural mais robusta.
De um insight de laboratório a possíveis novas terapias
Em conjunto, os resultados sugerem que a isquemia direciona as células de cura para um destino estressado e fibrótico em parte por aumentar o CDK8, que restringe sua capacidade de se tornar cartilagem e osso. Bloquear essa enzima parece liberar esse freio, permitindo que mais cartilagem se forme cedo e que mais osso seja depositado depois, mesmo quando o suprimento sanguíneo está comprometido. Como inibidores de CDK8 já estão sendo testados em pacientes com câncer, eles podem um dia ser reaproveitados para ajudar pessoas com alto risco de má cicatrização de fraturas — como idosos, fumantes ou aqueles com doença vascular — a regenerar osso forte em vez de tecido cicatricial frágil.
Citação: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Palavras-chave: cicatrização de fratura óssea, isquemia, inibidor de CDK8, células estromais mesenquimais, fibrose