Clear Sky Science · pt
O mapa sensorial olfativo é perturbado em um modelo transgênico de camundongo superexpressando α-sinucleína humana selvagem da doença de Parkinson
Por que a perda do olfato importa na doença de Parkinson
Muita gente associa a doença de Parkinson a um distúrbio do movimento, mas, para a maioria dos pacientes, a primeira função a falhar é o olfato. Essa perda pode aparecer décadas antes de tremor ou rigidez, tornando-se um sinal de alerta precoce poderoso. O estudo descrito aqui pergunta algo básico, ainda não respondido: o que exatamente dá errado na circuitaria cerebral do olfato quando surgem as alterações relacionadas ao Parkinson? Ao investigar essa questão em um modelo de camundongo cuidadosamente projetado, os pesquisadores revelam como uma proteína-chave do Parkinson perturba o “mapa do olfato” interno do cérebro e apontam para uma nova fonte de pistas precoces da doença, de fácil acesso.
O mapa olfativo do cérebro
Nossos narizes contêm milhões de células olfativas especializadas que respondem a moléculas de odor específicas. Essas células enviam fibras longas e finas para a frente do cérebro, onde convergem em pequenos núcleos chamados glomérulos dentro do bulbo olfativo. Cada tipo de odor ativa um padrão específico de glomérulos, formando um mapa sensorial preciso que permite ao cérebro distinguir café de canela ou fumaça de perfume. Em camundongos saudáveis, as células que expressam um receptor de odor (chamado M72) e outro (chamado P2) projetam de forma confiável para apenas dois glomérulos bem definidos por bulbo, criando um mapa altamente ordenado e reprodutível.
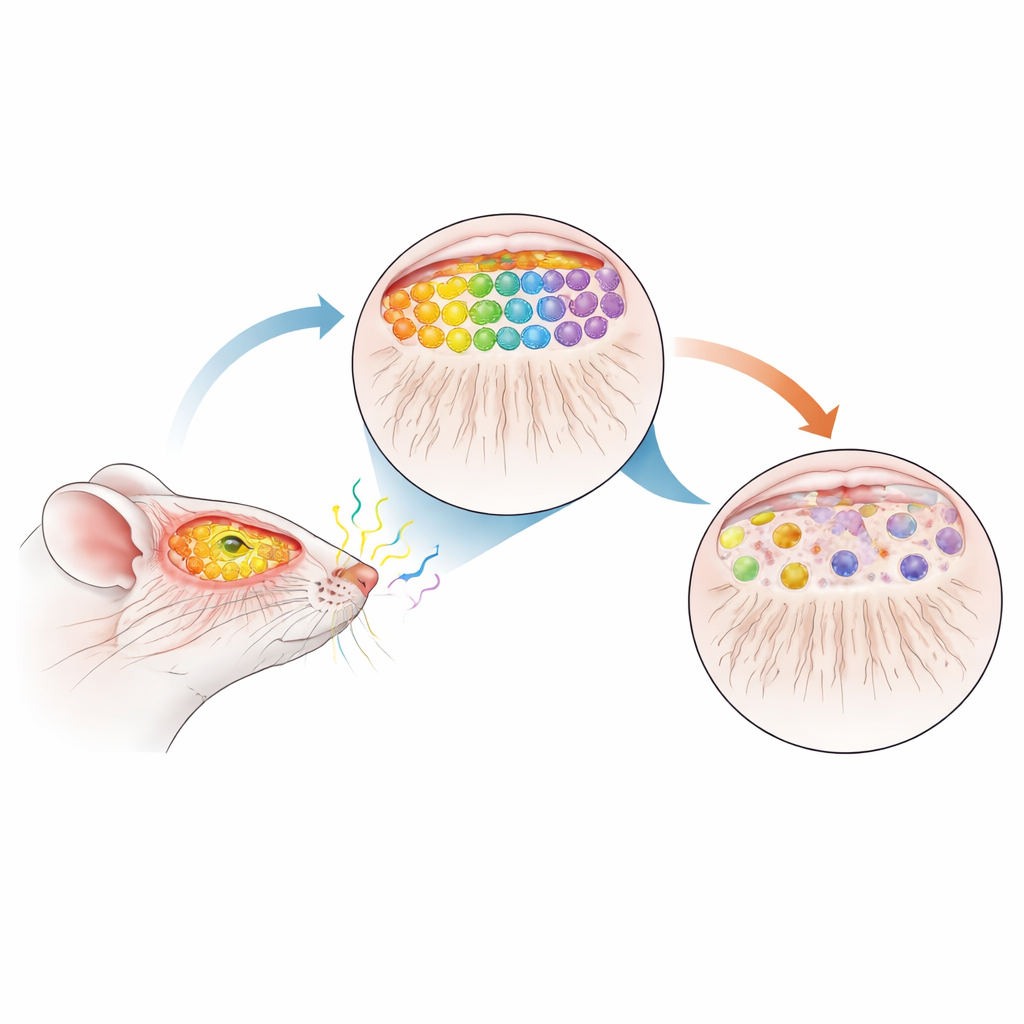
Um substituto murino para o Parkinson precoce
Para ver como a doença de Parkinson pode perturbar esse mapa, a equipe usou camundongos que superproduzem α-sinucleína humana normal, a mesma proteína que forma agregados nos cérebros de pessoas com Parkinson. Em seguida, cruzaram esses animais com camundongos marcados para M72 e P2 para que pudessem rastrear visualmente células olfativas selecionadas e suas conexões. Importante: o excesso de α-sinucleína é ativado apenas após o nascimento e se acumula gradualmente com a idade, mimetizando o curso lento e progressivo da doença humana. Aos 12 meses de idade — aproximadamente meia-idade para um camundongo e comparável a um estágio prodrômico, ou pré-diagnóstico, em humanos — os pesquisadores examinaram em detalhe os sistemas olfativos dos animais.
Quando o mapa do olfato se desfaz
Ao corar os neurônios marcados e seguir seus trajetos, os cientistas encontraram uma ruptura marcante do mapa olfativo em camundongos que superexpressam α-sinucleína. O número de neurônios M72 e P2 no nariz caiu drasticamente — cerca de três quartos a menos para M72 e quase metade para P2 — enquanto suas fibras para o bulbo foram muito reduzidas. Em vez de convergirem limpidamente em dois glomérulos robustos, as fibras remanescentes frequentemente formaram múltiplos glomérulos menores de tamanhos e posições variadas. Esses núcleos “extras” não apareciam em locais consistentes de um camundongo para outro, sinalizando perda da precisão topográfica normal. Um marcador amplo dos terminais das células olfativas, VGLUT2, também foi reduzido em cerca de 44% no bulbo, indicando que essa degeneração se estendia bem além dos dois tipos de receptor marcados.
Ligando circuitos quebrados à perda do olfato
O dano estrutural se traduziu em problemas olfativos mensuráveis. Camundongos mais velhos com α-sinucleína demoraram mais para localizar comida escondida, mostraram pior capacidade de distinguir um odor de outro e deixaram de preferir áreas marcadas com seu próprio cheiro — testes comportamentais que, juntos, revelam hiposmia e discriminação olfativa prejudicada. Eles também precisaram de concentrações de odor muito maiores para responder, evidenciando sensibilidade reduzida. Esses déficits não apareceram em camundongos mais jovens, nos quais os neurônios marcados e seus mapas ainda pareciam em grande parte normais, ligando o momento da perda funcional à degradação tardia do mapa sensorial, em vez de ao desenvolvimento inicial. Notavelmente, embora a proteína problemática fosse abundante no bulbo olfativo, ela não foi detectada no epitélio sensorial do nariz, apontando para alterações dentro da circuitaria do bulbo — particularmente nas células mitrais que retransmitem a informação olfativa adiante — como os prováveis motores da perturbação do mapa.
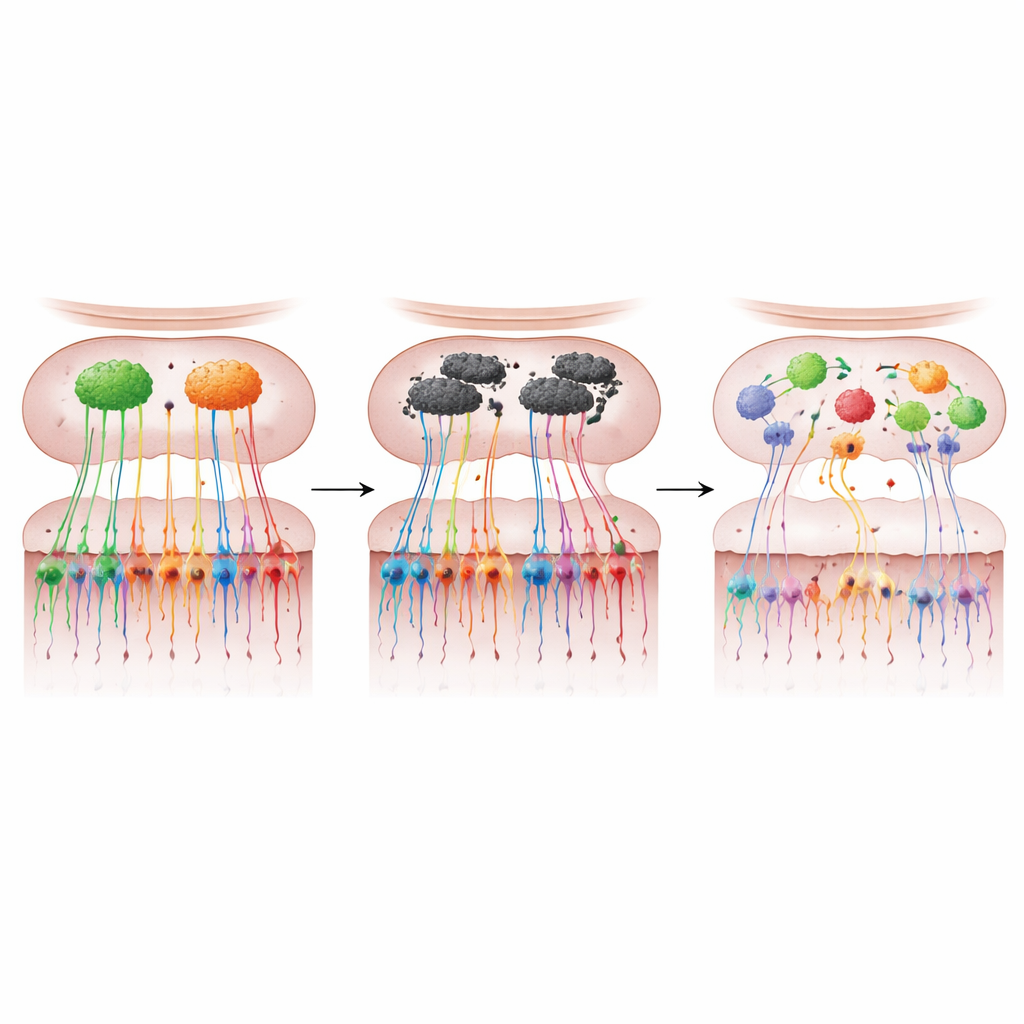
Células olfativas como janelas para a doença precoce
Em conjunto, o trabalho sustenta uma mensagem clara para não-especialistas: neste modelo murino semelhante ao Parkinson, a superprodução de α-sinucleína no bulbo olfativo leva tanto à perda quanto ao mal-encaminhamento das células olfativas, deformando o mapa de odores do cérebro e causando problemas olfativos precoces. Como as células sensoriais do nariz são relacionadas ao cérebro do ponto de vista do desenvolvimento, mas podem ser amostradas com swabs ou biópsias minimamente invasivas, os autores argumentam que mudanças semelhantes em pessoas poderiam fornecer um biomarcador precoce poderoso da doença de Parkinson. Mapear as impressões digitais moleculares dessas células, sugerem, pode não apenas ajudar a identificar indivíduos em risco anos antes do aparecimento dos sintomas motores, mas também oferecer nova visão sobre como a doença começa e se espalha — e como ela pode ser retardada ou prevenida.
Citação: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
Palavras-chave: Doença de Parkinson, disfunção olfativa, alfa-sinucleína, mapa sensorial, biomarcadores