Clear Sky Science · pt
Mutação LRRK2R1627P amplifica inflamação crônica induzida por fatores ambientais e agregação de α-sinucleína no intestino de ratos
Por que o intestino importa em uma doença cerebral
A doença de Parkinson é mais conhecida por tremores e problemas de movimento, mas evidências crescentes sugerem que suas raízes podem começar longe do cérebro, no intestino. Este estudo explora como uma mudança genética específica associada ao Parkinson em populações asiáticas pode, juntamente com o envelhecimento e a exposição a toxinas, danificar gradualmente o intestino de ratos. Ao observar o que acontece no intestino ao longo da vida dos animais, os pesquisadores traçam como defesas imunes cotidianas podem deslizar para uma inflamação crônica, criando o cenário para o acúmulo de proteínas relacionadas à doença que podem, eventualmente, ameaçar o cérebro.
Um gene de risco no trato digestivo
Os cientistas se concentraram em uma variante de um gene chamado LRRK2, há muito associada à doença de Parkinson e a certas condições inflamatórias intestinais. Eles produziram ratos portadores da mutação análoga, denominada LRRK2R1627P, e os compararam com ratos normais ao longo da vida. Embora a quantidade de mensageiro do gene LRRK2 no intestino não tenha mudado, a proteína LRRK2 total e um de seus marcadores de atividade-chave foram reduzidos, indicando que a mutação enfraquece a função normal dessa proteína no intestino. Essa alteração molecular sutil não causou danos dramáticos precoces, mas alterou discretamente a forma como as células intestinais se renovam e se organizam à medida que os animais envelhecem.
Intestino envelhecendo sob tensão lenta e persistente
Com o passar dos meses, ratos com a mutação desenvolveram sinais claros de estrutura intestinal perturbada. Seus intestinos delgados encurtaram, e as delicadas vilosidades e as criptas que absorvem nutrientes ficaram menores. Certas células especializadas do epitélio que produzem muco protetor e substâncias antimicrobianas—células caliciformes e células de Paneth—foram reduzidas, enquanto proteínas que ajudam as células vizinhas a formar junções apertadas e resistentes a vazamentos também caíram. Ao microscópio, essas junções tornaram-se mais curtas ou mais largas, sugerindo uma barreira enfraquecida. Importante: a arquitetura geral não colapsou; em vez disso, o intestino apresentou um padrão mais insidioso de renovação e proteção reduzidas, o que pode torná-lo mais vulnerável a irritações e infecções. 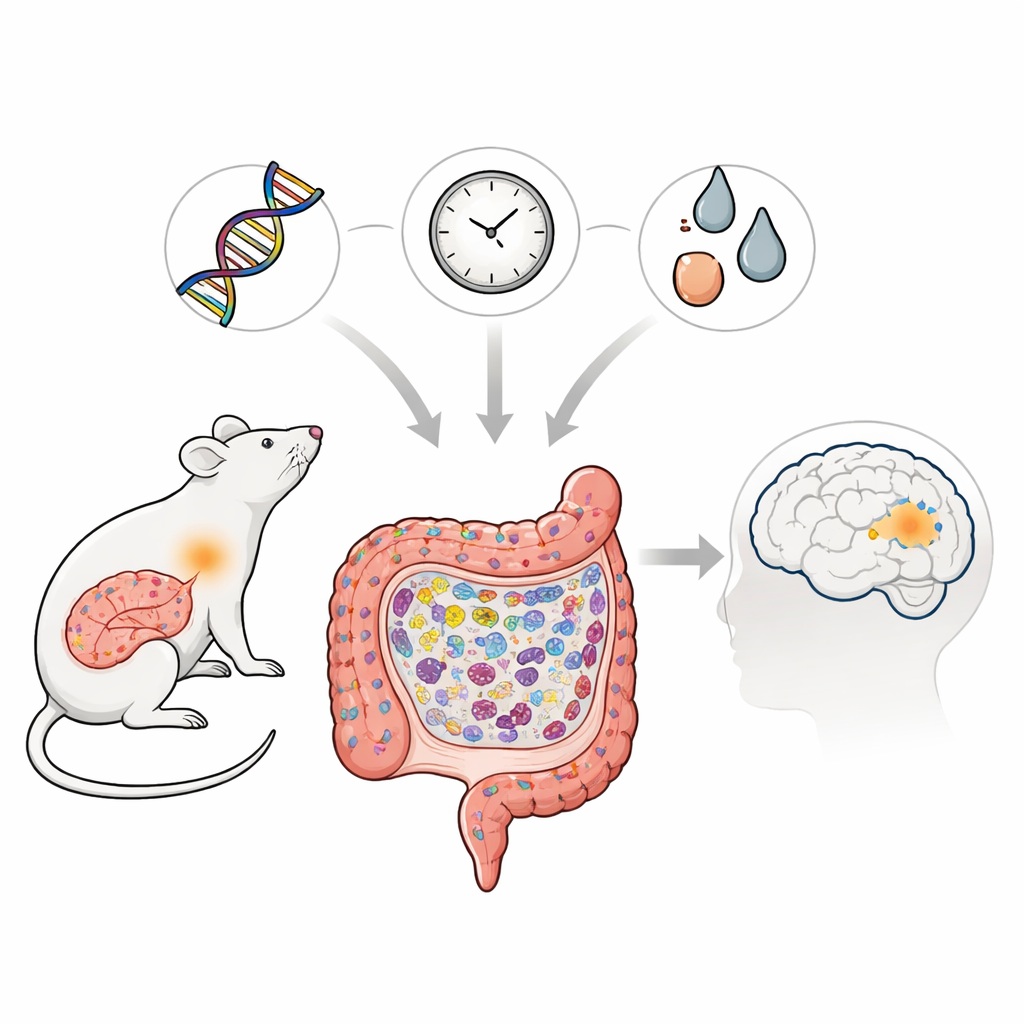
Sistema imunológico em alerta máximo
Para entender por que o intestino se desequilibrava, a equipe examinou a atividade gênica e as células imunes na parede intestinal. Eles descobriram que vias ligadas a um sensor chamado TLR4 e seu parceiro NF-κB estavam hiperativas em ratos mutantes mais velhos. Esses sensores normalmente ajudam o corpo a detectar micróbios nocivos, mas aqui impulsionaram o acúmulo de células imunes do tipo “lutar-antes” conhecidas como macrófagos M1. Essas células liberaram moléculas inflamatórias, transformando o intestino em um ambiente cronicamente irritado. De forma notável, a proteína relacionada ao Parkinson, α-sinucleína, em sua forma fosforilada associada à doença, começou a se acumular não nos neurônios intestinais, mas dentro desses macrófagos ativados no intestino delgado, especialmente em animais mais velhos.
Extra sensibilidade a agressões ambientais
A mutação genética sozinha não contou toda a história. Quando ratos jovens foram brevemente expostos a toxinas bacterianas (LPS), que estimulam o TLR4, os animais com a mutação LRRK2 desenvolveram inflamação intestinal muito mais severa do que seus pares normais. O revestimento intestinal perdeu mais células, as proteínas de barreira caíram ainda mais, e macrófagos pró-inflamatórios aumentaram em número, novamente acumulando α-sinucleína anormal. Isso sugere que pessoas portadoras de mutações similares podem ser especialmente sensíveis a agressões ambientais que perturbam o intestino, como certas infecções ou toxinas, ampliando seu risco a longo prazo.
Diminuindo o sinal de alarme
Como o TLR4 estava no centro dessa tempestade inflamatória, a equipe testou um fármaco, TAK-242, que especificamente atenua a sinalização do TLR4. Administrado por vários meses a ratos de meia-idade, o inibidor restaurou em grande parte o comprimento do intestino delgado, o tamanho de vilosidades e criptas, as células produtoras de muco e as proteínas de barreira. Reduziu macrófagos hiperativos, abaixou moléculas inflamatórias e cortou drasticamente o acúmulo de α-sinucleína anormal no intestino. Ao mesmo tempo, corrigiu uma comunidade microbiana perturbada: a diversidade aumentou, um supercrescimento de Lactobacillus diminuiu, e vários grupos bacterianos benéficos se recuperaram, enquanto as funções microbianas previstas se deslocaram para longe de padrões associados à doença. 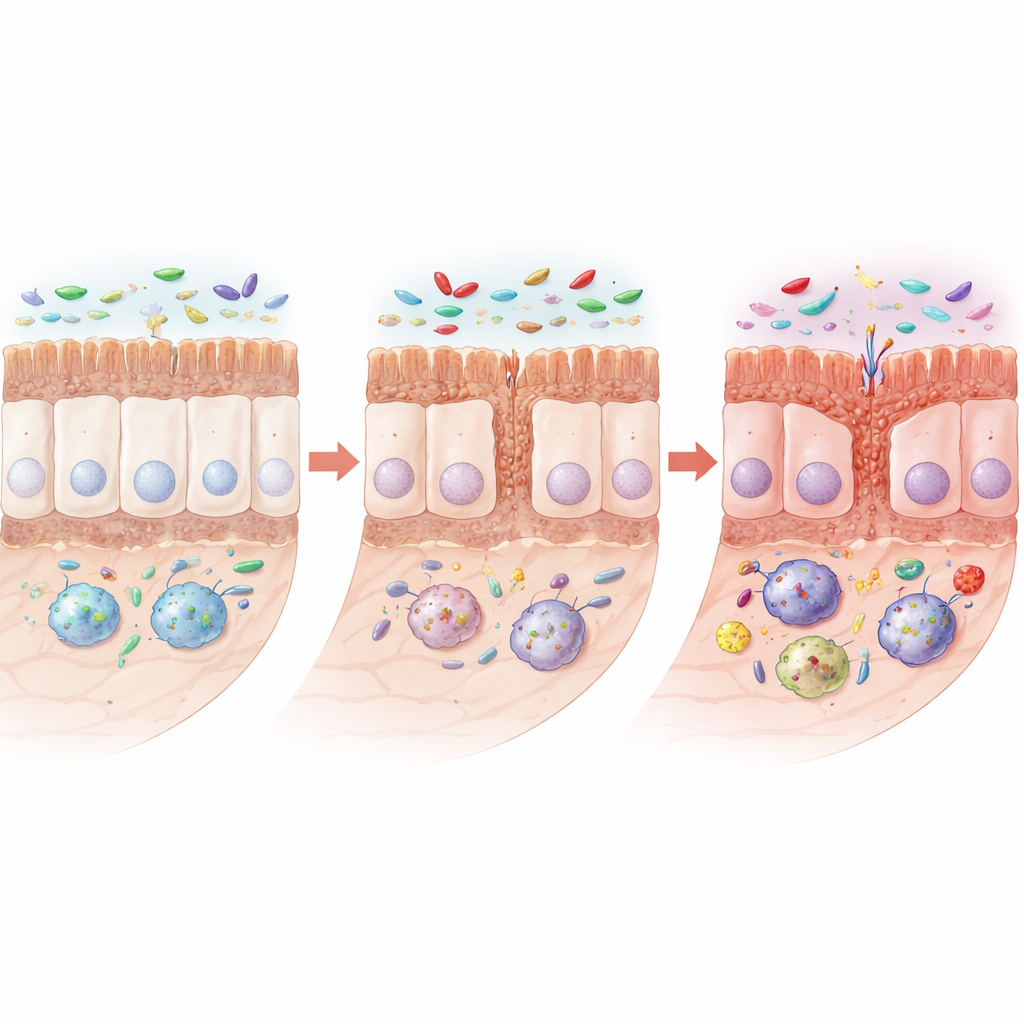
O que isso significa para o risco de Parkinson
Para um não especialista, a mensagem é que um “gene do Parkinson” pode, silenciosamente, remodelar as defesas imunes do intestino ao longo do tempo, especialmente na presença de envelhecimento e estresse ambiental. Nestes ratos, o resultado é uma inflamação crônica de baixo grau que enfraquece a barreira intestinal, perturba os micro-organismos residentes e faz com que proteínas associadas ao Parkinson se acumulem em células imunes—ainda não Parkinson em sua forma clínica plena, mas um contexto biológico que poderia favorecer doença cerebral posterior. Ao mostrar que bloquear uma única via imune intestinal pode reverter muitas dessas alterações, o estudo destaca o intestino como um alvo prático precoce: proteger a saúde intestinal e controlar a inflamação no intestino pode ajudar a retardar ou prevenir o Parkinson em pessoas com risco genético.
Citação: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Palavras-chave: Doença de Parkinson, inflamação intestinal, mutação LRRK2, microbioma, imunidade inata