Clear Sky Science · pt
Fenotipagem neurocomportamental profunda revela impressões neurais dos déficits locomotores na doença de Parkinson
Por que os problemas ao caminhar na doença de Parkinson importam
Para muitas pessoas com doença de Parkinson, um dos sintomas mais assustadores é quando os pés parecem colados ao chão ou a caminhada diminui a ponto de quase parar. Essas falhas de movimento, que vão da lentidão sutil ao completo "congelamento" da marcha, aumentam muito o risco de quedas e perda de independência, e ainda assim medicamentos e estimulação cerebral frequentemente não os previnem. Este estudo teve como objetivo descobrir os padrões cerebrais ocultos que acompanham esses problemas de locomoção, com a meta de longo prazo de projetar terapias mais inteligentes e sob demanda.
Observando o movimento em detalhes finos
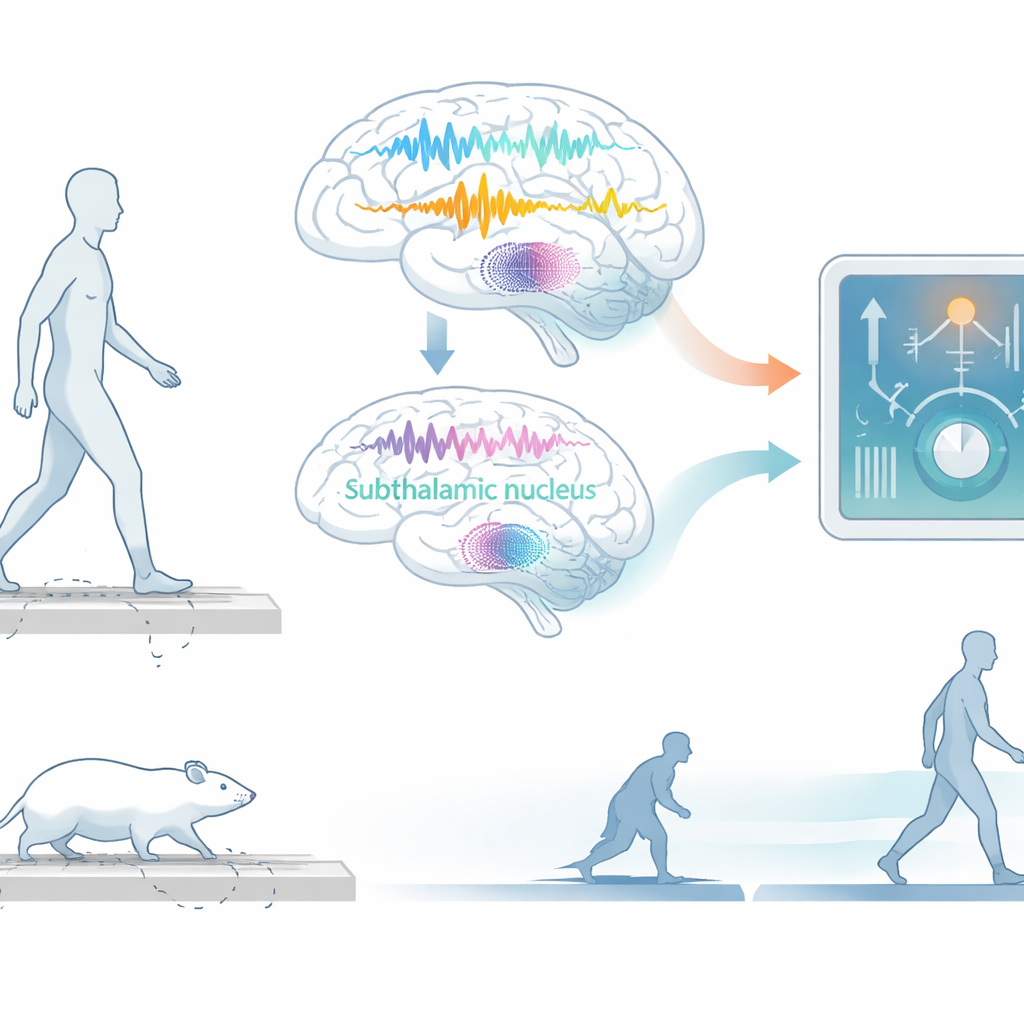
Os pesquisadores começaram com um modelo de rato bem estabelecido da doença de Parkinson. Treinaram os ratos para caminhar de um lado a outro por uma pista, rastreando cada pequeno movimento das patas traseiras em três dimensões e registrando a atividade elétrica das áreas cerebrais relacionadas ao movimento. Cada momento de comportamento foi classificado em um de três estados: caminhada normal, pequenos movimentos intencionais no lugar ou acinesia—uma paralisação quase completa do movimento que se assemelha aos episódios de congelamento observados em pacientes. Isso criou um rico conjunto de dados “neurocomportamentais” que alinhou ritmos cerebrais ao que o corpo fazia instante a instante.
Encontrando padrões nas ondas cerebrais
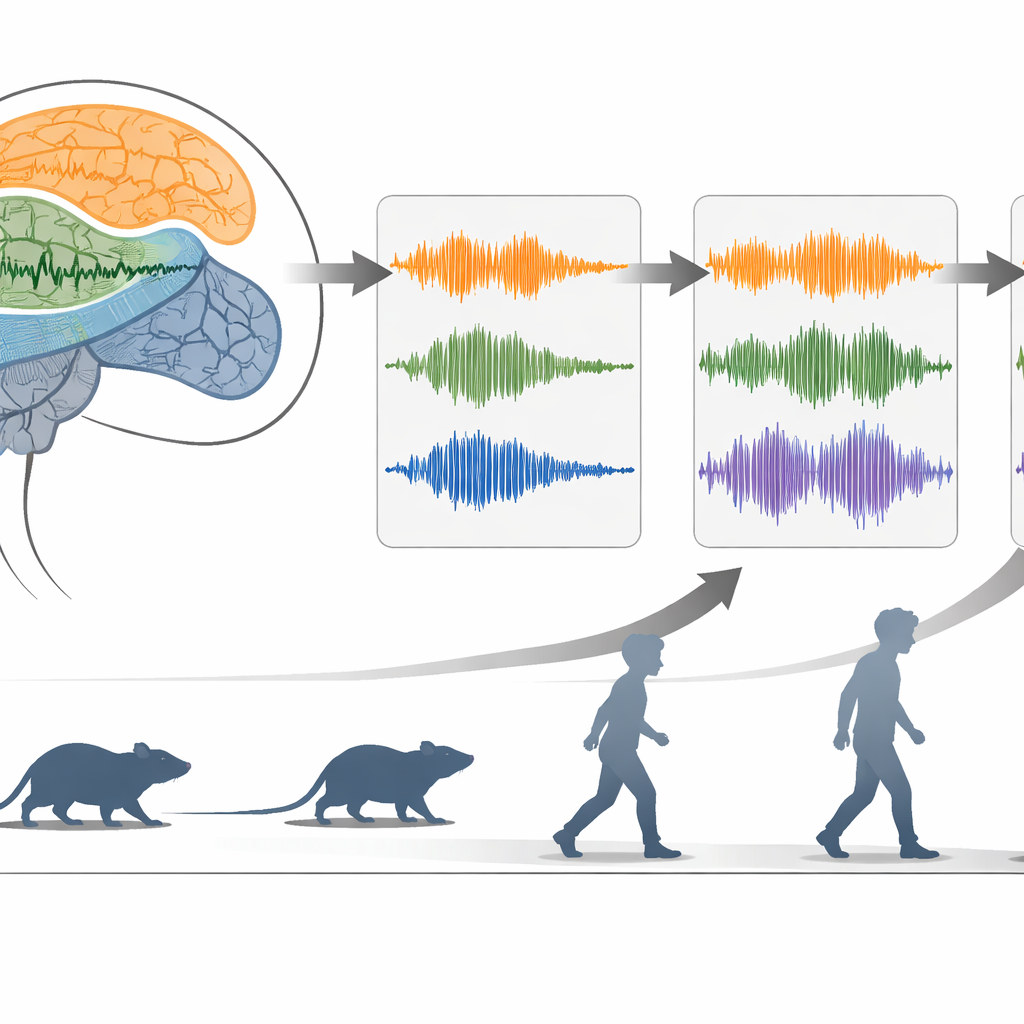
Para dar sentido a esses dados de alta dimensionalidade, a equipe aplicou tanto estatística clássica quanto ferramentas modernas de deep learning. Primeiro confirmaram assinaturas já conhecidas: ratos com dano similar ao da doença de Parkinson passaram mais tempo em acinesia do que animais saudáveis, e seus sinais cerebrais mostraram atividade mais forte em uma faixa de frequência relacionada a ritmos beta anormais e gamma baixo. Mas quando os cientistas perguntaram quais características melhor distinguiam os três estados de movimento, novos protagonistas surgiram. Medidas chamadas complexidade de Hjorth e mobilidade de Hjorth—resumos no domínio do tempo sobre o quão irregular e quão rápido o sinal varia—mostraram‑se marcadores poderosos. No hemisfério afetado, maior complexidade e menor mobilidade estiveram fortemente ligadas ao início da acinesia, enquanto outras características, como potência em gamma de alta frequência, acompanharam o movimento ativo.
Focalizando o momento em que o movimento cessa
Usando redes neurais que aprendem “mapas” compactos dos dados, os pesquisadores puderam posicionar cada janela de tempo breve em um espaço de baixa dimensionalidade onde caminhada, movimento estacionário e acinesia ocupavam regiões distintas. Dentro desse espaço, as medidas de Hjorth e a banda beta–gamma baixa anormal influenciaram fortemente onde os episódios acinéticos se situavam. Quando a equipe focou nos segundos ao redor do início de um episódio acinético, observaram uma sequência consistente: complexidade e potência tipo‑beta aumentaram pouco antes e no momento da parada, enquanto mobilidade e potência em gamma diminuíram. Crucialmente, essas medidas podem ser calculadas rapidamente sem análises de frequência pesadas, tornando‑as candidatas atraentes para monitoramento em tempo real.
De ratos a pessoas com congelamento da marcha
O grupo então investigou se impressões neurais semelhantes aparecem em humanos. Analisaram captura de movimento detalhada e registros de eletrodos implantados em uma estrutura profunda do cérebro, o núcleo subtalâmico, em duas pessoas com Parkinson que apresentavam congelamento da marcha. Em um dos participantes, o mesmo padrão observado em ratos surgiu durante os episódios de congelamento: aumento da complexidade de Hjorth e da potência beta, junto com redução da mobilidade de Hjorth. Embora o comportamento da banda gamma tenha diferido um pouco entre as espécies, o sinal central de que o movimento estava deslizando para um estado patológico parecia surpreendentemente similar no córtex dos ratos e no núcleo subtalâmico desse paciente, sugerindo um mecanismo subjacente compartilhado pela rede motora.
O que isso pode significar para terapias futuras
Ao fundir rastreamento de movimento detalhado com análise avançada de ondas cerebrais, este trabalho identifica “impressões” simples e computacionalmente leves de quando a caminhada na doença de Parkinson está prestes a entrar em colapso. Para o público em geral, isso significa que médicos e engenheiros em breve poderão construir estimuladores cerebrais que detectem essas impressões em tempo real e respondam apenas quando necessário, afastando o sistema de um episódio de congelamento antes que ele se estabeleça totalmente. Embora sejam necessários estudos maiores em humanos, a abordagem abre um caminho promissor rumo a tratamentos personalizados e em circuito fechado para problemas incapacitantes da marcha na doença de Parkinson.
Citação: Garulli, E.L., Merk, T., El Hasbani, G. et al. Deep neurobehavioral phenotyping uncovers neural fingerprints of locomotor deficits in Parkinson’s disease. npj Parkinsons Dis. 12, 65 (2026). https://doi.org/10.1038/s41531-026-01280-4
Palavras-chave: Doença de Parkinson, congelamento da marcha, ritmos cerebrais, estimulação cerebral profunda, fenotipagem neurocomportamental