Clear Sky Science · pt
Avaliação sistemática de reguladores da morfologia mitocondrial para a melhora da α-sinucleinopatia neuronal
Por que as pequenas usinas importam nas doenças cerebrais
Mitocôndrias, as “usinas” da célula, são cruciais para manter os neurônios vivos e suas conexões funcionando. Em doenças cerebrais como a doença de Parkinson, essas estruturas frequentemente parecem danificadas ou fragmentadas, mas tem sido difícil saber quais alterações são prejudiciais e quais “chaves” podemos acionar com segurança para protegê‑las. Este estudo testa de forma sistemática reguladores-chave da “forma” mitocondrial em um modelo de laboratório de acúmulo proteico relacionado ao Parkinson, usando uma ferramenta de inteligência artificial para medir as formas mitocondriais em diferentes partes dos neurônios. O trabalho aponta para um regulador em particular, chamado Fis1, como um alvo promissor para manter mitocôndrias — e sinapses — saudáveis sem causar novos efeitos colaterais.
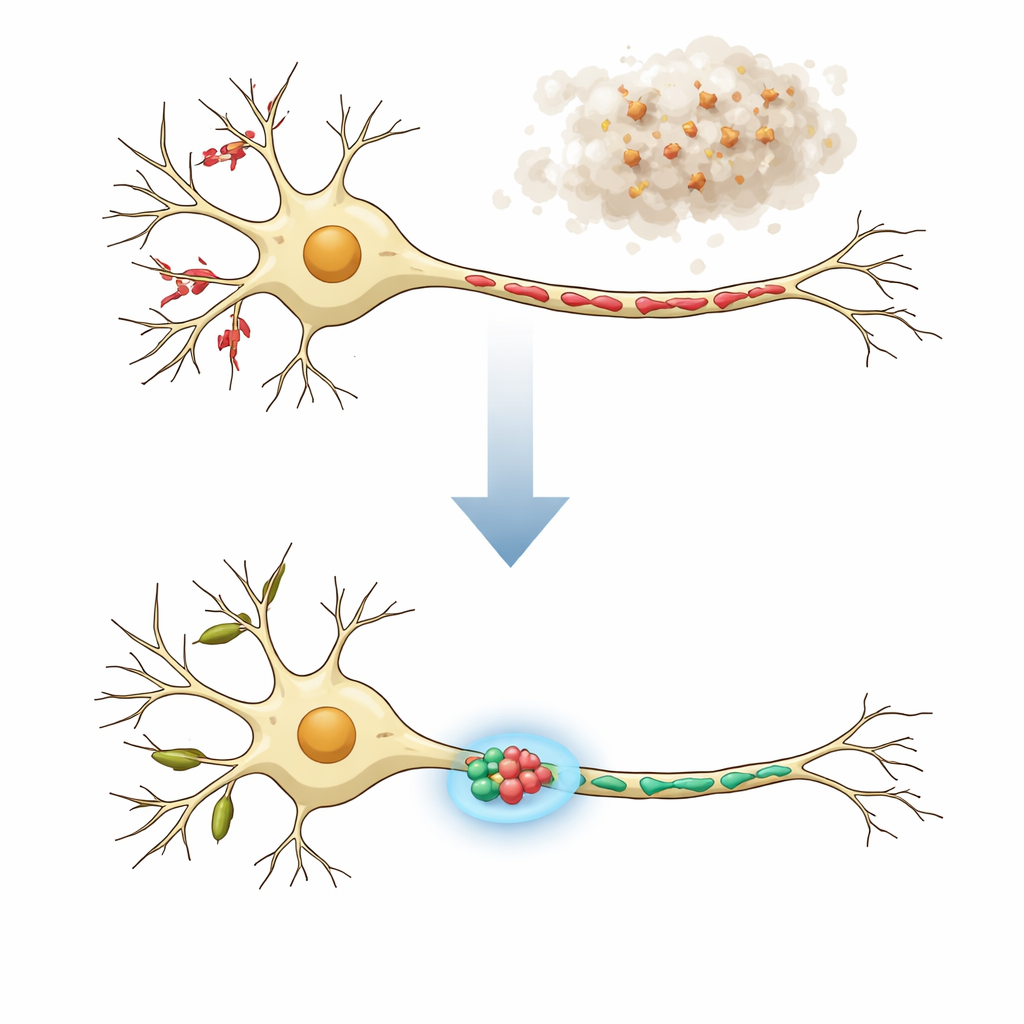
Os dois bairros de uma célula cerebral
Os neurônios não são uniformes: seus ramos em forma de árvore (dendritos) e seus longos cabos (axônios) têm funções diferentes e abrigam mitocôndrias com formatos muito distintos. Em neurônios saudáveis, os dendritos tendem a conter mitocôndrias longas e tubulares que ajudam a sustentar a produção local de proteínas e a comunicação flexível em locais receptores chamados espinhas dendríticas. Os axônios, que enviam sinais, carregam muitos mitocôndrias curtos que fornecem energia e ajudam a controlar os níveis de cálcio nos terminais pré‑sinápticos. Em doenças neurodegenerativas, tanto a função quanto a estrutura dessas mitocôndrias podem ser perturbadas, manifestando‑se como fragmentos, formas inchadas ou cordões com aspecto de contas. Os autores supuseram que tratamentos verdadeiramente eficazes precisam restaurar as mitocôndrias em dendritos e axônios de volta aos seus formatos normais, específicos por compartimento.
Construindo um teste de estresse semelhante ao do Parkinson
Para imitar uma característica-chave da doença de Parkinson e transtornos relacionados, os pesquisadores expuseram neurônios corticais de camundongo em cultura a fibrilas pré‑formadas de alfa‑sinucleína, uma proteína que pode se agregar em acúmulos prejudiciais. Em poucos dias, essas fibrilas semearam o acúmulo anômalo de alfa‑sinucleína nas células e levaram a uma fragmentação mitocondrial pronunciada tanto em dendritos quanto em axônios. Usando o MitoVis, um sistema de análise de imagens por deep learning, a equipe conseguiu separar automaticamente dendritos de axônios em imagens de microscopia e medir o comprimento, a área e a forma de centenas de mitocôndrias por imagem cerca de dez vezes mais rápido do que o traçado manual. Essa abordagem de alto rendimento confirmou que a condição semelhante à doença encurtou as mitocôndrias e as tornou mais arredondadas, em consonância com relatos de modelos animais e tecido de pacientes.
Testando os interruptores da forma mitocondrial
A equipe então perguntou se modular proteínas específicas de fusão e fissão poderia prevenir esse dano. Aumentar duas proteínas de fusão (Mfn1 e Mfn2) ou reduzir uma proteína de fissão (Mff) protegeu as mitocôndrias dendríticas do encurtamento induzido pela alfa‑sinucleína e também preservou as espinhas dendríticas. Contudo, essas mesmas manipulações tornaram as mitocôndrias axonais excessivamente longas, o que trabalhos anteriores associaram a problemas na liberação de sinais e no ramificação axonal. Em contraste, reduzir outra proteína de fissão, Fis1, restaurou o comprimento mitocondrial tanto em dendritos quanto em axônios a valores próximos do normal sem causar super‑alongamento. Importante, nesse sistema a redução de Fis1 não matou neurônios e, como as outras intervenções, preservou a densidade de espinhas dendríticas que de outra forma diminuiria sob estresse por alfa‑sinucleína.
Manter o cálcio em equilíbrio
Como as mitocôndrias nos axônios ajudam a amortecer o cálcio durante a atividade elétrica, os pesquisadores testaram se mudar sua forma alterava esse equilíbrio delicado. Eles usaram um sensor de cálcio fluorescente direcionado às mitocôndrias em botões pré‑sinápticos e estimularam os axônios com rajadas breves de potenciais de ação. Na condição com alfa‑sinucleína, o manejo do cálcio em mitocôndrias axonais levemente encurtadas parecia semelhante ao normal. Mas quando as mitocôndrias axonais foram tornadas excessivamente longas por superexpressão de Mfn1 ou redução de Mff, elas captaram mais cálcio do que o habitual após a estimulação. Essa captação aumentada poderia perturbar a função pré‑sináptica. Em contraste, a redução de Fis1, que normalizou mas não excedeu o comprimento mitocondrial, preservou as respostas mitocondriais ao cálcio que correspondiam de perto aos controles saudáveis, sugerindo menos compensações ocultas.
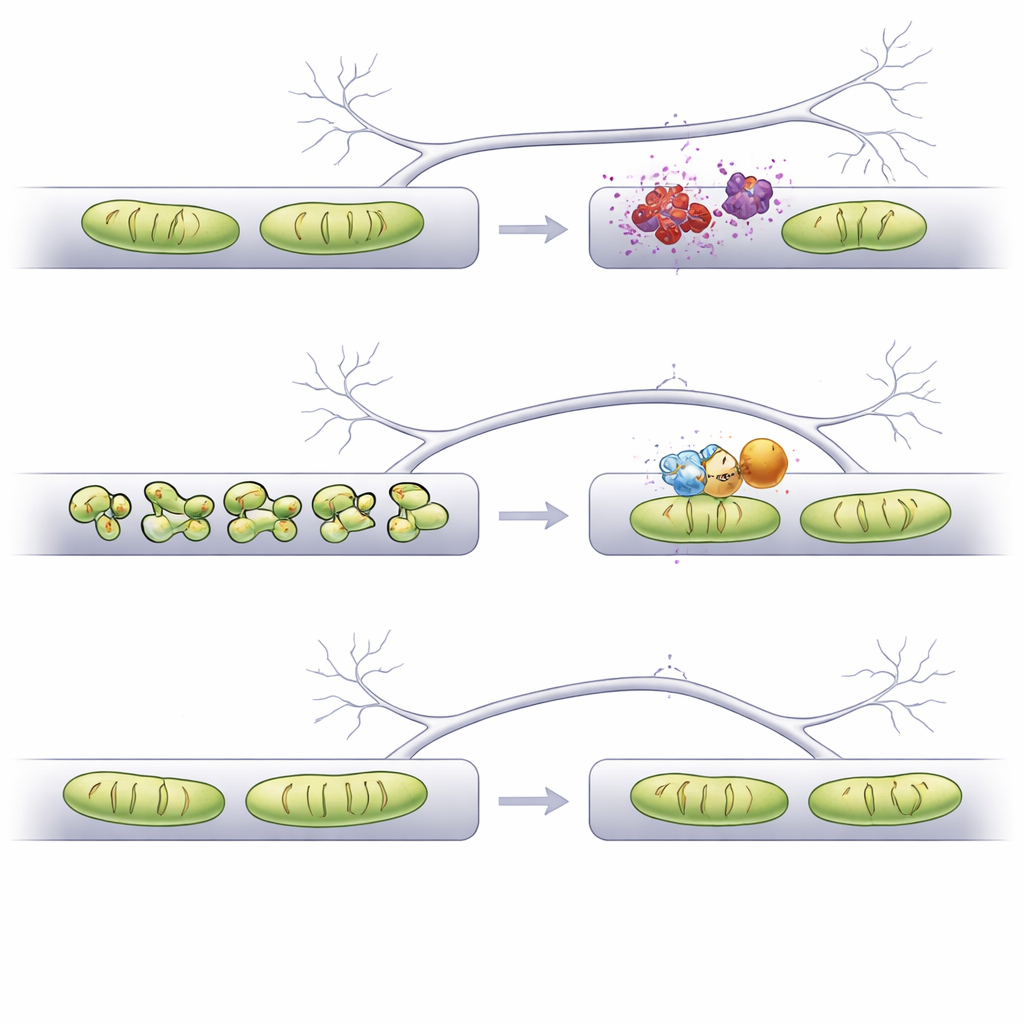
O que isso pode significar para tratamentos futuros
Em conjunto, o estudo mostra que simplesmente alongar mitocôndrias não é suficiente — restaurar sua forma ao tamanho certo no compartimento certo é a chave. Usando um fluxo de trabalho de imagem assistido por IA, os autores identificam Fis1 como um alvo especialmente atraente: sua downregulation mantém as mitocôndrias estruturalmente estáveis em dendritos e axônios, previne a perda de espinhas dendríticas e evita manuseio anômalo de cálcio em terminais pré‑sinápticos. Essas descobertas sustentam a ideia de que ajustar cuidadosamente a forma mitocondrial, potencialmente com drogas ou moléculas antisenso direcionadas a Fis1, poderia ajudar a proteger sinapses vulneráveis na α‑sinucleinopatia relacionada ao Parkinson e possivelmente em outras doenças cerebrais em que as mitocôndrias se alteram.
Citação: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
Palavras-chave: Doença de Parkinson, mitocôndrias, alfa-sinucleína, disfunção sináptica, neurodegeneração