Clear Sky Science · pt
Utilidade clínica dos potenciais evocados para programação da estimulação cerebral profunda no núcleo subtalâmico na doença de Parkinson
Por que essa história do marcapasso cerebral importa
Para muitas pessoas com doença de Parkinson, os medicamentos acabam deixando de funcionar de forma estável. Elas podem oscilar entre rigidez e movimentos incontroláveis, e o ajuste fino do tratamento vira um ciclo frustrante de visitas ao consultório. Este artigo de revisão examina como os médicos podem usar os próprios ecos elétricos do cérebro — chamados potenciais evocados — para programar a estimulação cerebral profunda (DBS) de maneira mais rápida e objetiva. Em essência, questiona se é possível transformar a programação da DBS de tentativa e erro em um marcapasso cerebral mais orientado por dados e personalizado.
Do método tentativa e erro ao ajuste guiado
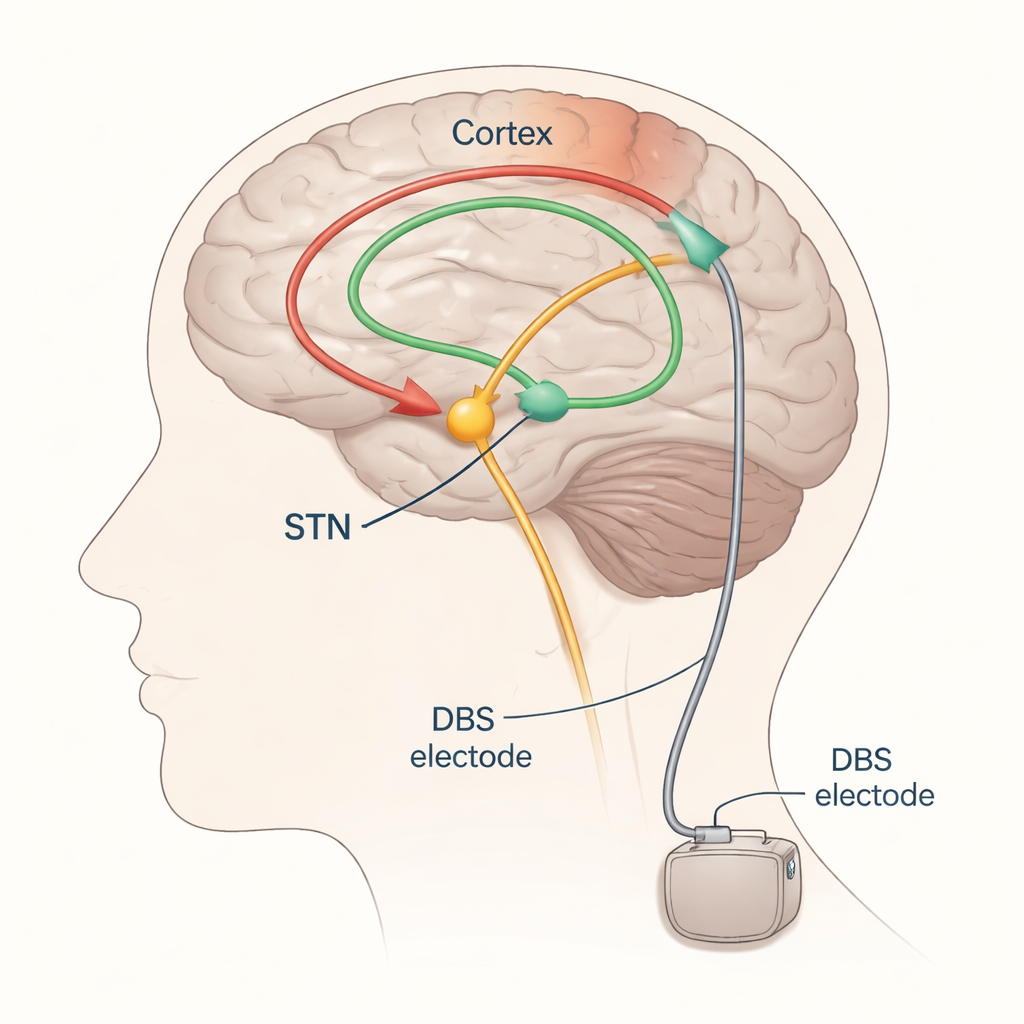
A DBS para Parkinson geralmente tem como alvo uma pequena estrutura profunda do cérebro chamada núcleo subtalâmico (NST). Eletrodos são implantados ali e conectados a um gerador de pulsos sob a pele no peito. Quando bem ajustada, a DBS do NST pode aliviar tremor, bradicinesia e rigidez, mas se o campo elétrico se espalhar demais pode estimular acidentalmente vias próximas que controlam músculos ou sensibilidade, causando efeitos colaterais como contrações musculares ou formigamento. Hoje, os neurologistas normalmente ajustam a DBS alterando lentamente as configurações e observando os movimentos e efeitos colaterais do paciente — uma abordagem que consome tempo, depende de como o paciente está naquele dia e frequentemente exige várias consultas de acompanhamento.
Ouvindo os ecos elétricos do cérebro
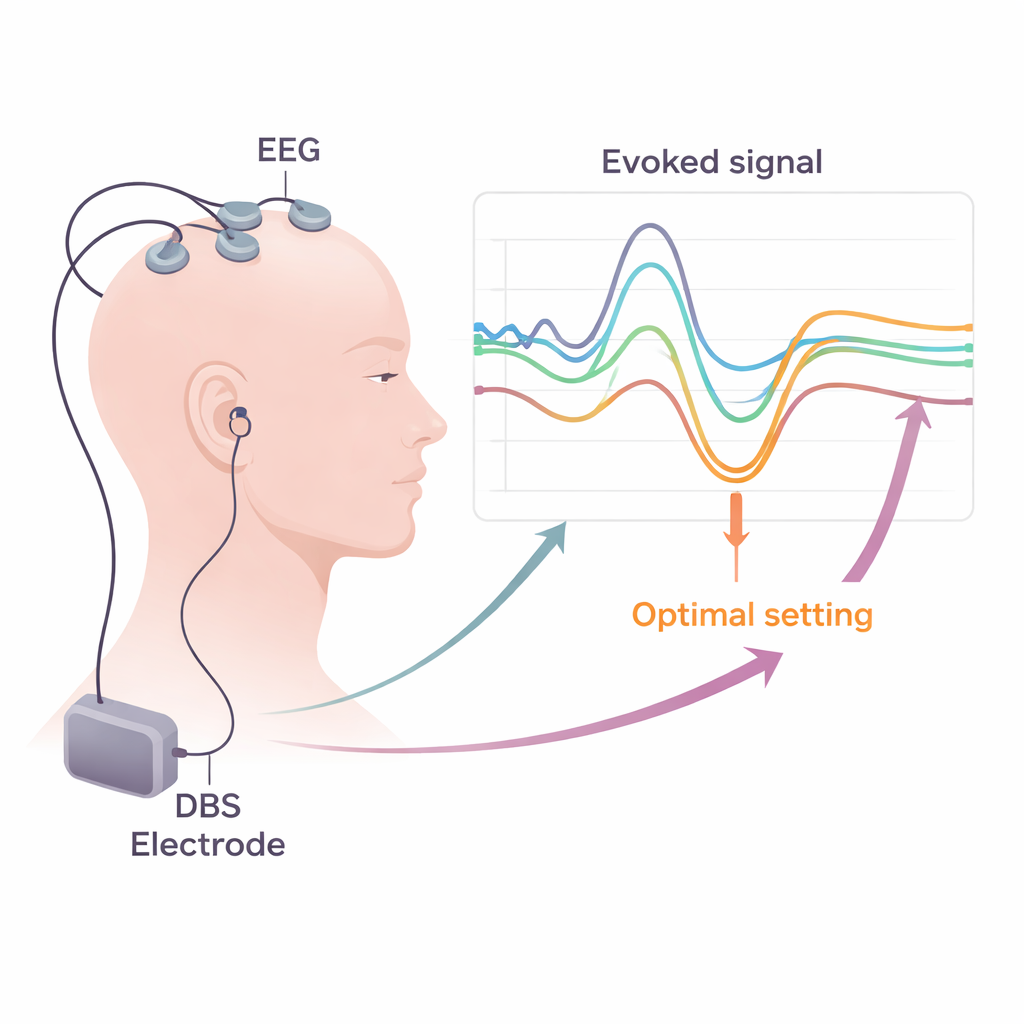
Os autores focam nos potenciais evocados — pequenas respostas elétricas sincronizadas no cérebro ou nos músculos após um estímulo — como possíveis indicativos de configurações de DBS boas ou ruins. Quando o NST é estimulado, ondas de atividade viajam por vias nervosas e podem ser detectadas no couro cabeludo com EEG, na atividade muscular com EMG, ou ocasionalmente com fitas de registro colocadas diretamente sobre a superfície cerebral. Estimulando repetidamente em baixas frequências e fazendo a média das respostas, os pesquisadores podem visualizar ondas distintas que aparecem em diferentes latências (milissegundos) após cada pulso. Ondas precoces, chegando por volta de dois milésimos de segundo, refletem principalmente a ativação de vias motoras rápidas próximas ao eletrodo. Ondas um pouco mais tardias, em torno de três milissegundos (frequentemente chamadas de componente “P3”), são consideradas provenientes de uma ligação direta entre o córtex frontal e o NST conhecida como via hiper-direta. Ondas ainda mais tardias provavelmente percorrem circuitos mais longos e em loop que incluem o tálamo e outros núcleos profundos.
Encontrando o ponto ideal e evitando problemas
Em vários estudos, surge um quadro consistente: contatos no eletrodo de DBS que produzem um P3 forte e de curta latência tendem a estar na parte do NST mais útil e se associam a melhor melhora dos sintomas motores parkinsonianos e a uma “janela terapêutica” mais ampla antes do aparecimento de efeitos colaterais. Em contraste, ondas muito precoces vinculadas a vias motoras e certas respostas em 8–10 milissegundos frequentemente indicam que a estimulação está se espalhando para estruturas vizinhas, aumentando o risco de contrações musculares ou outros efeitos indesejados. Medidas separadas de potenciais evocados motores (respostas EMG em músculos da face e dos membros) e potenciais evocados somatossensoriais (padrões de EEG relacionados a vias táteis) podem revelar ativação sutil da cápsula interna ou do lemnisco medial — feixes de fibras que conduzem comandos motores e informações sensoriais. Detectar essas alterações cedo permite aos clínicos desviar a corrente de áreas arriscadas escolhendo contatos diferentes ou ajustando a forma e a polaridade do pulso.
Tornando as ferramentas de laboratório práticas na clínica
Converter esses insights em cuidado rotineiro exige soluções práticas. A revisão explica como sistemas hospitalares padrão de EEG e EMG já podem registrar a maioria dos sinais necessários, desde que usem taxas de amostragem altas e métodos cuidadosos para remover o “ruído” elétrico dos pulsos de DBS. Os autores discutem estratégias para reduzir artefatos, como re-referência inteligente, subtração por template e algoritmos avançados de computador que separam a atividade cerebral verdadeira dos resíduos de estimulação. Eles defendem que sessões de teste curtas e estruturadas — combinando breves períodos de DBS em baixa frequência, registros no couro cabeludo e monitoramento muscular em repouso e em contração leve — poderiam ser integradas à habitual semana de programação pós-cirúrgica. Mapas de potenciais evocados de cada contato poderiam então ser combinados com imagens e outros biomarcadores para orientar quais contatos e configurações usar a longo prazo.
O que isso significa para pessoas com Parkinson
O artigo conclui que os potenciais evocados são candidatos promissores para tornar a programação da DBS mais precisa, eficiente e previsível. Em particular, a onda P3 de curta latência parece ser um marcador forte de que a estimulação está atingindo o circuito certo para aliviar os sintomas motores do Parkinson, enquanto respostas evocados motoras e sensoriais podem alertar quando a corrente está vazando para vias que causam efeitos colaterais. Embora sejam necessários mais estudos para padronizar técnicas e comprovar benefícios na prática clínica cotidiana, essa abordagem aponta para um futuro em que médicos podem “ouvir” o cérebro durante a programação, localizar rapidamente o ponto ideal de cada paciente e reduzir o ônus da tentativa e erro para pessoas que vivem com a doença de Parkinson.
Citação: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Palavras-chave: Doença de Parkinson, estimulação cerebral profunda, potenciais evocados, mapeamento cerebral, neurofisiologia