Clear Sky Science · pt
Decodificando o impacto dos estados visuais nos sinais de feedback da estimulação cerebral profunda adaptativa em transtornos do movimento
Por que fechar os olhos importa para implantes cerebrais
Para pessoas que convivem com doença de Parkinson ou distonia, a estimulação cerebral profunda (DBS) pode funcionar como um marcapasso para circuitos cerebrais que disparam de forma inadequada. Sistemas mais recentes, chamados “adaptativos”, prometem ajustar automaticamente a estimulação em tempo real ao “ouvir” os sinais do cérebro. Este estudo mostra que algo tão simples e habitual quanto fechar os olhos pode alterar fortemente esses sinais, o que significa que futuros implantes cerebrais precisam primeiro reconhecer o estado da pessoa antes de decidir como estimular.
Marcapassos cerebrais que aprendem e se adaptam
A DBS tradicional fornece pulsos elétricos constantes a áreas profundas do cérebro ao longo do dia. Embora isso possa aliviar sintomas como tremor e rigidez, também pode desperdiçar bateria e ocasionalmente causar efeitos colaterais, porque a estimulação não muda quando a condição do paciente muda. A DBS adaptativa busca resolver isso aumentando ou diminuindo a corrente com base em “potenciais de campo local”, pequenas tensões rítmicas registradas pelos mesmos eletrodos que entregam a terapia. Esses ritmos são mais fortes em estruturas chamadas núcleo subtalâmico (STN) e globo pálido interno (GPi), pontos-chave na rede de movimento. 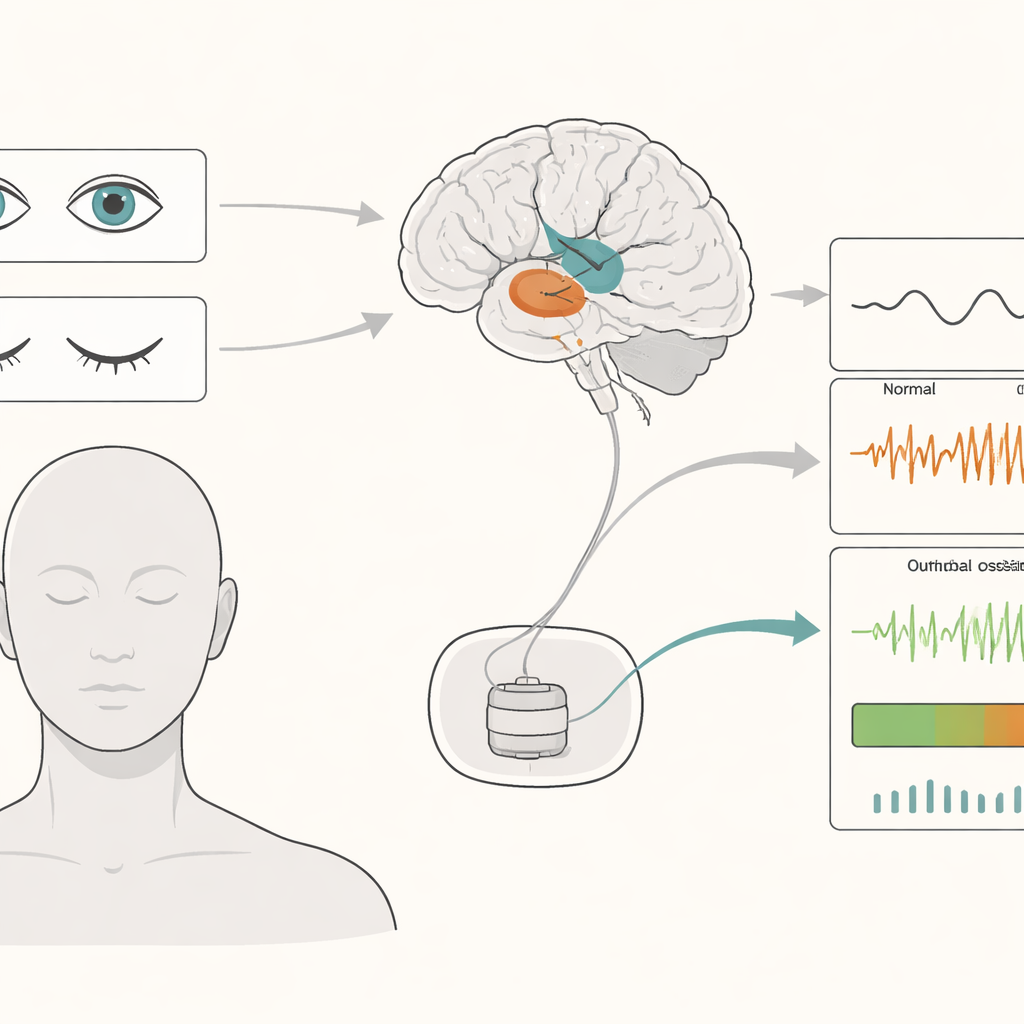
Quando a visão descansa, os ritmos cerebrais profundos mudam
Os pesquisadores acompanharam 36 pacientes — 18 com doença de Parkinson e 18 com distonia — nos dias após a cirurgia de DBS. Eles registraram a atividade cerebral a partir de eletrodos no STN ou GPi e do couro cabeludo enquanto os pacientes descansavam com olhos abertos, olhos fechados ou dormindo. Fechar os olhos aumentou consistentemente ritmos lentos no cérebro profundo, especialmente nas faixas teta e alfa, que são exatamente os sinais que muitos sistemas de DBS adaptativa monitoram. Esse aumento foi mais pronunciado no STN, que está fortemente conectado à superfície externa “pensante” do cérebro, e menos acentuado no GPi. O sono apresentou um padrão diferente, com ondas muito lentas particularmente fortes.
Distúrbios diferentes, impressões digitais de sinal diferentes
A doença de Parkinson e a distonia já têm “impressões” rítmicas distintas, e o estudo mostrou que o fechamento dos olhos alterou essas impressões de maneiras ligeiramente diferentes. Em ambos os transtornos, a potência em baixas frequências e em alfa caiu quando os pacientes reabriram os olhos. Mas na doença de Parkinson apareceu uma queda extra na potência teta que não surgiu na distonia. Como resultado, com os olhos abertos, pessoas com distonia mantiveram mais atividade teta do que aquelas com Parkinson. Isso ressalta que o mesmo sinal profundo pode refletir tanto a doença quanto mudanças ordinárias no nível de alerta, tornando arriscado tratar qualquer ritmo isolado como um marcador simples de ligar/desligar dos sintomas.
Redes cerebrais conversam mais quando os olhos estão fechados
Além da força dos próprios ritmos, a equipe também examinou o quão sincronizados estavam as estruturas profundas e o córtex. Usando um método que foca em comunicação genuína em vez de ruído compartilhado simples, descobriram que fechar os olhos aumentou a atividade coordenada em baixas frequências e em alfa entre o STN e regiões centrais do couro cabeludo sobre o córtex sensório-motor. O GPi também mostrou um acoplamento alfa mais forte ao córtex com olhos fechados, embora de forma mais modesta e sem diferenças regionais claras. Essas descobertas sugerem que descansar com os olhos fechados altera não apenas a atividade local, mas os padrões mais amplos de comunicação da rede de movimento.
Ensinando máquinas a reconhecer estados internos
Como implantes futuros provavelmente usarão algoritmos para ler sinais cerebrais, os pesquisadores testaram se modelos simples de aprendizado de máquina poderiam distinguir olhos abertos de olhos fechados apenas com base nesses ritmos. Ao alimentar classificadores com várias bandas de frequência, eles identificaram o estado dos olhos com cerca de 88 por cento de acerto usando sinais do STN e 77 por cento usando sinais do GPi, tanto na doença de Parkinson quanto na distonia. Modelos não lineares, capazes de capturar padrões mais complexos, tiveram desempenho ainda melhor, e a melhor decodificação veio de regiões sensório-motoras mais diretamente ligadas ao movimento. 
Rumo a uma estimulação cerebral mais inteligente e ciente do contexto
Em termos simples, o estudo mostra que mudanças ordinárias e saudáveis no nível de vigília ou no engajamento visual de uma pessoa podem alterar fortemente as ondas cerebrais nas quais os sistemas de DBS adaptativa confiam. Se um implante simplesmente reagir sempre que um ritmo cruzar um limiar fixo, pode interpretar mal mudanças normais de estado como agravamento da doença e superestimular ou subestimular. Os autores defendem que a próxima geração de DBS deveria primeiro detectar o contexto da pessoa — como olhos abertos versus fechados, sono versus vigília — e então interpretar os sinais da doença de forma diferente dependendo desse estado. Esses marcapassos cerebrais “conscientes do estado” poderiam fornecer ajuda mais precisa, evitar estimulação desnecessária e apoiar melhor pessoas com transtornos do movimento em sua vida diária.
Citação: Zhu, GY., Merk, T., Butenko, K. et al. Decoding the impact of visual states on adaptive deep brain stimulation feedback signals in movement disorders. npj Parkinsons Dis. 12, 61 (2026). https://doi.org/10.1038/s41531-026-01273-3
Palavras-chave: estimulação cerebral profunda adaptativa, doença de Parkinson, distrofia, oscilações cerebrais, interfaces cérebro-computador