Clear Sky Science · pt
Inibição da corrosão por perfuração em aço inoxidável por NaNO3: insights mecanísticos sobre dissolução de sulfeto, despassivação e dissolução ativa
Por que pequenas manchas de ferrugem importam
De pontes e arranha‑céus a carros e plantas químicas, o aço inoxidável é escolhido porque geralmente resiste à ferrugem. Ainda assim, em condições específicas, ele pode desenvolver repentinamente pequenos e profundos buracos chamados porosidades, que podem evoluir para trincas perigosas. Este estudo faz uma pergunta prática para a indústria: um produto químico comum e relativamente seguro — o nitrato de sódio — pode impedir que essas porosidades comecem, e em caso afirmativo, como? A resposta pode ajudar a manter infraestruturas críticas mais seguras por mais tempo, usando aditivos que são acessíveis e menos prejudiciais ao meio ambiente. 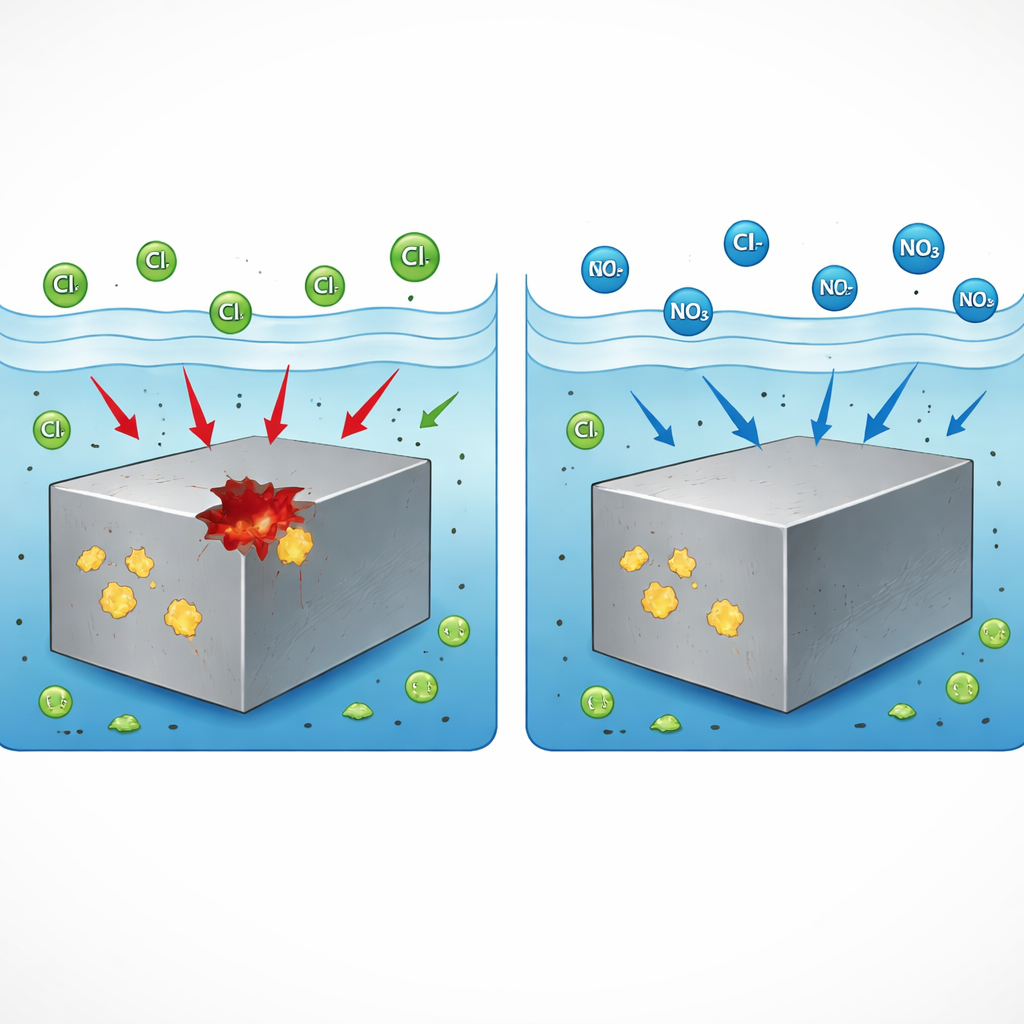
Pontos fracos ocultos dentro do aço inoxidável
Mesmo os melhores aços inoxidáveis não são perfeitamente homogêneos. Espalhadas no interior estão partículas microscópicas ricas em enxofre, conhecidas como inclusões de sulfeto. Dois tipos importantes são baseados em manganês (MnS) e cálcio (CaS). Essas inclusões comportam‑se como pontos fracos incorporados onde as porosidades preferencialmente se iniciam quando água contendo cloreto, como spray salino ou água de resfriamento, entra em contato com o metal. Trabalhos anteriores mostraram que a formação de porosidade segue um roteiro consistente: a partícula de sulfeto começa a dissolver, o filme protetor no aço adjacente se rompe e então o metal circundante começa a dissolver rapidamente, escavando um poro. O presente estudo compara dois aços inoxidáveis comerciais Tipo 304 — um dominado por inclusões ricas em MnS e outro por inclusões baseadas em CaS — para entender se o nitrato pode interromper esse roteiro em um ou ambos os tipos de ponto fraco.
Testando aditivos comuns em água salgada
Os pesquisadores imergiram os aços em uma solução salina simples e forçaram lentamente o metal a condições mais corrosivas enquanto observavam quando porosidades estáveis se formavam. Compararam três aditivos em concentrações realistas: amônio, nitrito e nitrato, todos na forma de sais de sódio ou amônio. Somente o nitrato teve um efeito marcante. Em ambos os aços, ricos em MnS e ricos em CaS, a adição de uma quantidade modesta de nitrato de sódio impediu completamente a formação de porosidades estáveis na faixa testada, enquanto os outros dois aditivos não apresentaram melhoria. A microscopia confirmou que, sem nitrato, as porosidades realmente começavam nas inclusões de sulfeto, enquanto com nitrato essas inclusões não mais desencadeavam buracos danosos. Isso mostrou que o nitrato é um inibidor de porosidade amplamente eficaz para diferentes tipos de sulfeto, não apenas um caso especial. 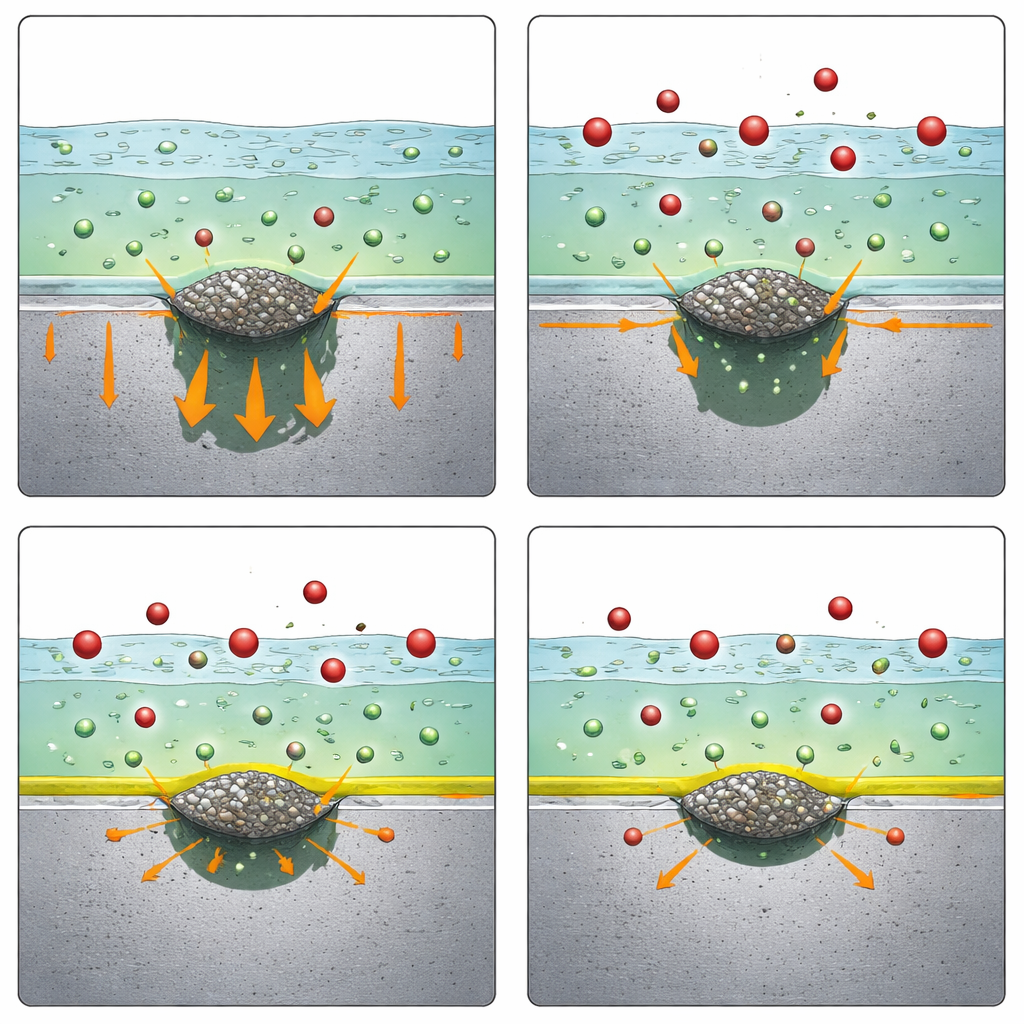
Observando de perto o que o nitrato muda — e o que não muda
Para identificar como o nitrato atua, a equipe examinou de perto os estágios iniciais de formação de porosidade ao redor de partículas únicas de MnS usando microeletrodos e imagens de alta resolução. Observaram que o nitrato não impedia as partículas de MnS de se dissolverem, nem alterava as pequenas trincheiras que se formam na interface entre a inclusão e o aço circundante. O nitrato também não alterou o nível de acidez no qual o filme protetor do aço falha em solução cloretada. Tudo isso indicou que os primeiros passos da iniciação de porosidade — enfraquecimento e ruptura ao redor da inclusão — ainda ocorrem de maneira bastante semelhante na presença de nitrato.
Retardando a fase final de perda metálica
A diferença crucial surgiu quando os pesquisadores recriaram o ambiente severo dentro de um poro já formado: condições muito ácidas e ricas em cloreto. Usando soluções ácidas fortes que imitam a química no interior dos poros, eles constataram que o aço normalmente apresenta duas explosões distintas de dissolução metálica rápida conforme a voltagem é aumentada. A adição de nitrato reduziu consistentemente a primeira explosão de dissolução, tanto em ácido puro quanto em ácido que também continha espécies de enxofre semelhantes às liberadas pela dissolução de MnS. Observações de superfície mostraram ataque uniforme, porém a uma taxa claramente menor. Testes adicionais, variando acidez e níveis de cloreto, sugeriram que o efeito do nitrato não pode ser explicado simplesmente por diluição da acidez, deslocamento do cloreto ou estabilização de crostas salinas. Em vez disso, os resultados apontaram para o nitrato ajudando o cromo presente na liga a formar uma camada superficial estabilizadora, que por sua vez retarda a fase inicial, mais crítica, da perda ativa de metal.
O que isso significa para aços no mundo real
Em termos simples, o nitrato não impede as primeiras mordidas químicas em pequenas partículas de sulfeto dentro do aço inoxidável, mas retarda a fase final e descontrolada em que uma imperfeição inofensiva se transforma em um poro perigoso. Ao amortecer esse surto de perda metálica em microambientes ácidos e salgados, o nitrato de sódio mantém o aço mais próximo de um estado passivo e autoprotectivo, mesmo quando inclusões de sulfeto e íons cloreto estão presentes. Como o nitrato é relativamente barato, menos tóxico do que muitas alternativas e já é usado em sistemas de água industriais, entender esse mecanismo fortalece o argumento para seu uso cuidadoso como aditivo de controle de corrosão para estender a vida útil de estruturas e equipamentos em aço inoxidável.
Citação: Amatsuka, S., Nishimoto, M. & Muto, I. Pitting-corrosion inhibition in stainless steel by NaNO3: mechanistic insights on sulfide dissolution, depassivation, and active dissolution. npj Mater Degrad 10, 40 (2026). https://doi.org/10.1038/s41529-026-00753-4
Palavras-chave: corrosão de aço inoxidável, inibição de perfuração, nitrato de sódio, inclusões de sulfeto, soluções cloretadas