Clear Sky Science · pt
Efeito dos processos eletroquímicos de tratamento de água na corrosão do aço carbono em sistema de abastecimento urbano
Por que as tubulações da sua água encanada importam
Os sistemas de tratamento eletroquímico de água estão se tornando mais comuns nas cidades porque removem poluentes com eficiência, amaciam a água e eliminam microrganismos. Mas as mesmas reações elétricas que limpam a água também podem corroer silenciosamente os tubos que a conduzem até nossas casas. Este estudo examina como esse tratamento afeta o aço carbono, um material de tubulação comum, e explica por que a corrosão pode acelerar dramaticamente quando eletricidade e a química cotidiana da água encanada interagem.
Limpar a água com eletricidade
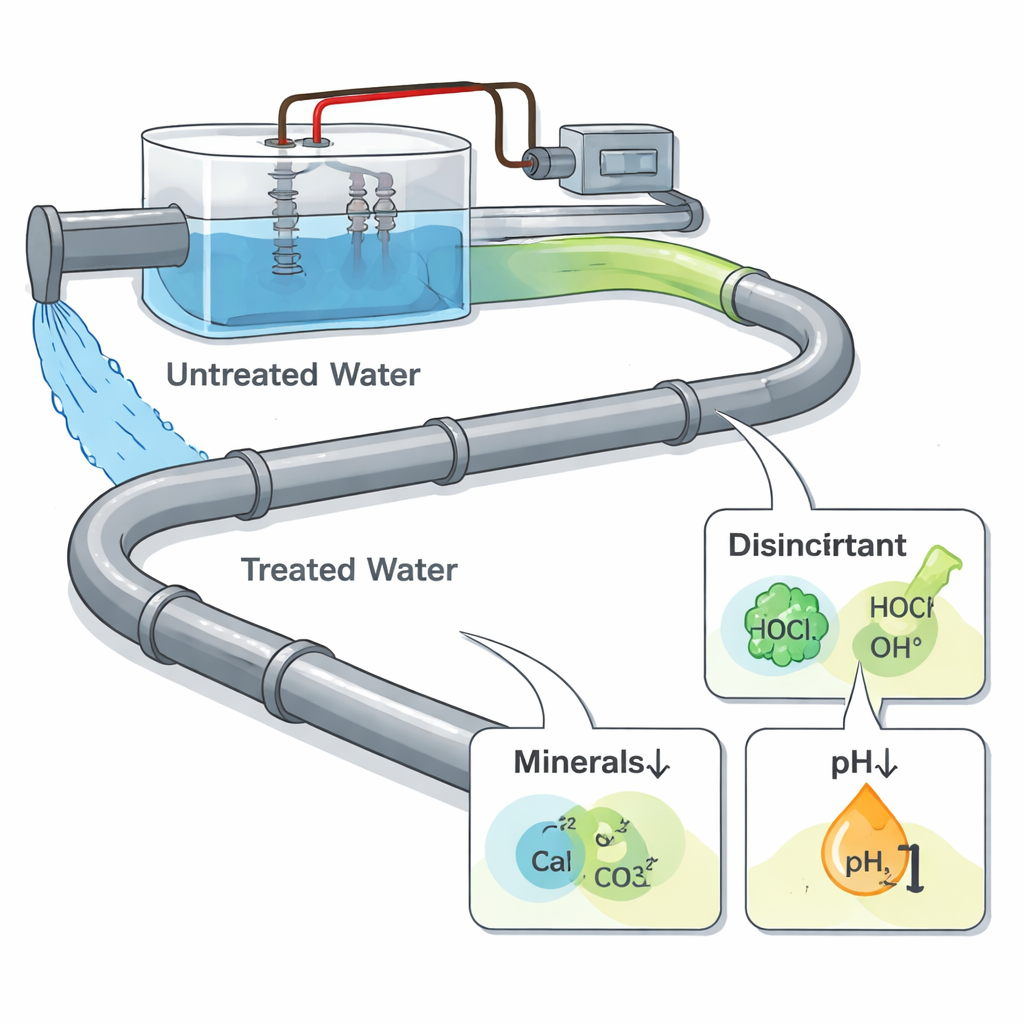
O tratamento eletroquímico faz passar uma corrente elétrica pela água usando placas metálicas chamadas eletrodos. Isso pode remover íons indesejados, degradar poluentes orgânicos e gerar desinfetantes, tornando o processo atraente para sistemas urbanos e industriais. Ao contrário do tratamento tradicional, porém, as tubulações em si não são eletricamente conectadas ao sistema—elas apenas recebem a água tratada que sai da unidade. Isso significa que qualquer corrosão adicional não é causada pela eletricidade atingindo diretamente o tubo, mas por mudanças na química da água: novos agentes oxidantes para desinfecção, variações na acidez e movimentação de íons minerais que normalmente ajudam a formar camadas protetoras no interior das tubulações.
Perda de metal mais rápida e danos ocultos mais profundos
Os pesquisadores conduziram um experimento de 90 dias com água de cidade real, expondo amostras de aço carbono a diferentes tensões, de 0 a 9 volts, e acompanharam perda de massa, danos na superfície e comportamento eletroquímico. Constatou-se que mesmo nos primeiros três dias a eletrólise aumentou a corrosão, e tensões maiores sempre significaram mais dano. A 9 volts, a taxa de corrosão geral aumentou mais de 25 vezes em comparação com a água que não passou pelo processo elétrico. Usando varreduras 3D da superfície, também mostraram que pequenos pits no metal se tornaram muito mais profundos à medida que a tensão aumentava. Na maior tensão, os pits mais profundos chegaram a ser quase cinco vezes mais profundos do que na água não tratada, reduzindo drasticamente a vida útil esperada do aço mesmo quando a perda média de metal não parecia extrema.
Por que as camadas protetoras falham
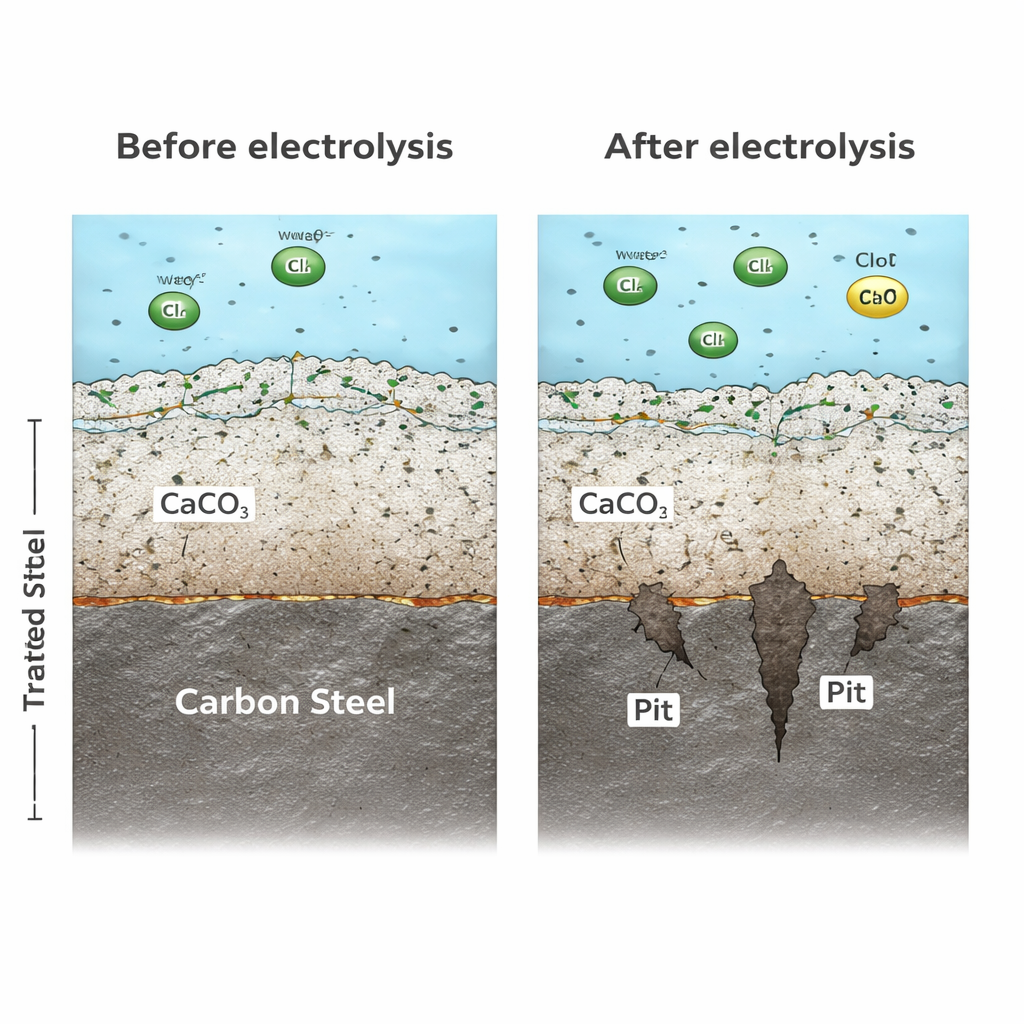
No interior de muitas tubulações, minerais presentes na água constroem naturalmente uma camada fina e densa que ajuda a proteger o metal. Na água não tratada, o carbonato de cálcio desempenha esse papel protetor. Na água tratada eletroquimicamente, porém, essa proteção mineral praticamente desaparece. Como o cátodo na unidade de tratamento atrai íons de cálcio e carbonato e os incentiva a formar depósitos ali, menos desses íons permanecem para construir uma barreira sólida nas paredes das tubulações. Testes de microscopia e difração revelaram que, em vez de uma barreira compacta e rica em minerais, o aço na água tratada desenvolveu uma camada de ferrugem solta e porosa com pequenos cristais instáveis. Esse revestimento fraco permitiu que espécies corrosivas e elétrons se movessem com facilidade, de modo que a corrosão permaneceu rápida em vez de desacelerar com o tempo.
Um ataque químico mais forte na água
Para identificar o que estava impulsionando o ataque extra, a equipe separou os diferentes fatores. Quando fizeram eletrólise em uma solução de sulfato sem cloreto, os subprodutos da divisão da água—como oxigênio, hidrogênio e radicais de curta duração—mal alteraram o comportamento de corrosão do aço. Mas quando o cloreto, o mesmo íon encontrado em sais comuns e em muitas águas abastecidas, estava presente, a história mudou. A eletrólise converteu parte do cloreto em hipoclorito, um desinfetante mais reativo. Testes eletroquímicos mostraram que, à medida que a corrente aumentava, o aço se tornava muito mais suscetível à corrosão em soluções com cloreto. Simulações computacionais confirmaram isso: o hipoclorito reduziu a barreira de energia para que átomos de ferro deixassem a superfície metálica, fazendo a corrosão progredir mais facilmente do que com cloreto sozinho. Ao mesmo tempo, a rápida formação de produtos de ferrugem consumiu íons hidróxido, empurrando a água para pH mais baixo, ou condições mais ácidas, o que favoreceu ainda mais a corrosão.
O que isso significa para os sistemas de água
Para não especialistas, a conclusão é que limpar e desinfetar a água com eletricidade não é automaticamente algo suave para os tubos que a transportam. Em sistemas onde a água contém cloreto, o tratamento eletroquímico pode transformar parte desse cloreto em um desinfetante mais forte e corrosivo enquanto remove ingredientes minerais necessários para formar proteção natural. O resultado é um afinamento mais rápido do metal e pits mais profundos que podem encurtar a vida útil das tubulações e aumentar o risco de vazamentos ou contaminação. Os autores sugerem que projetistas e operadores desses sistemas tratem a corrosão como uma preocupação central de projeto—limitando a tensão, reduzindo o cloreto antes do tratamento, escolhendo eletrodos que formem menos subprodutos agressivos e monitorando pitting e a química da água a longo prazo—para garantir que água mais limpa não venha ao custo de infraestrutura que falha.
Citação: Zhao, S., Jing, Y., He, X. et al. Effect of electrochemical water treatment processes on carbon steel corrosion in urban water supply system. npj Mater Degrad 10, 23 (2026). https://doi.org/10.1038/s41529-026-00736-5
Palavras-chave: tratamento eletroquímico de água, corrosão do aço carbono, tubulações de água urbanas, cloreto e hipoclorito, durabilidade da infraestrutura hídrica