Clear Sky Science · pt
Variantes em MTNAP1 causam um distúrbio neurodegenerativo ao comprometerem a estabilidade mitocondrial
Por que esta história importa para a saúde do cérebro
Muitas famílias vivem a dor de ver uma criança perder habilidades de desenvolvimento aos poucos sem um diagnóstico claro. Este estudo revela uma nova causa genética para essa condição, traçando o caminho desde um único gene defeituoso até “estações geradoras de energia” danificadas dentro das células cerebrais e, por fim, ao encolhimento do tecido cerebral. Entender essa cadeia de eventos não só traz respostas para as famílias afetadas, como também aprimora nossa visão geral sobre quão frágeis são os sistemas energéticos do cérebro.
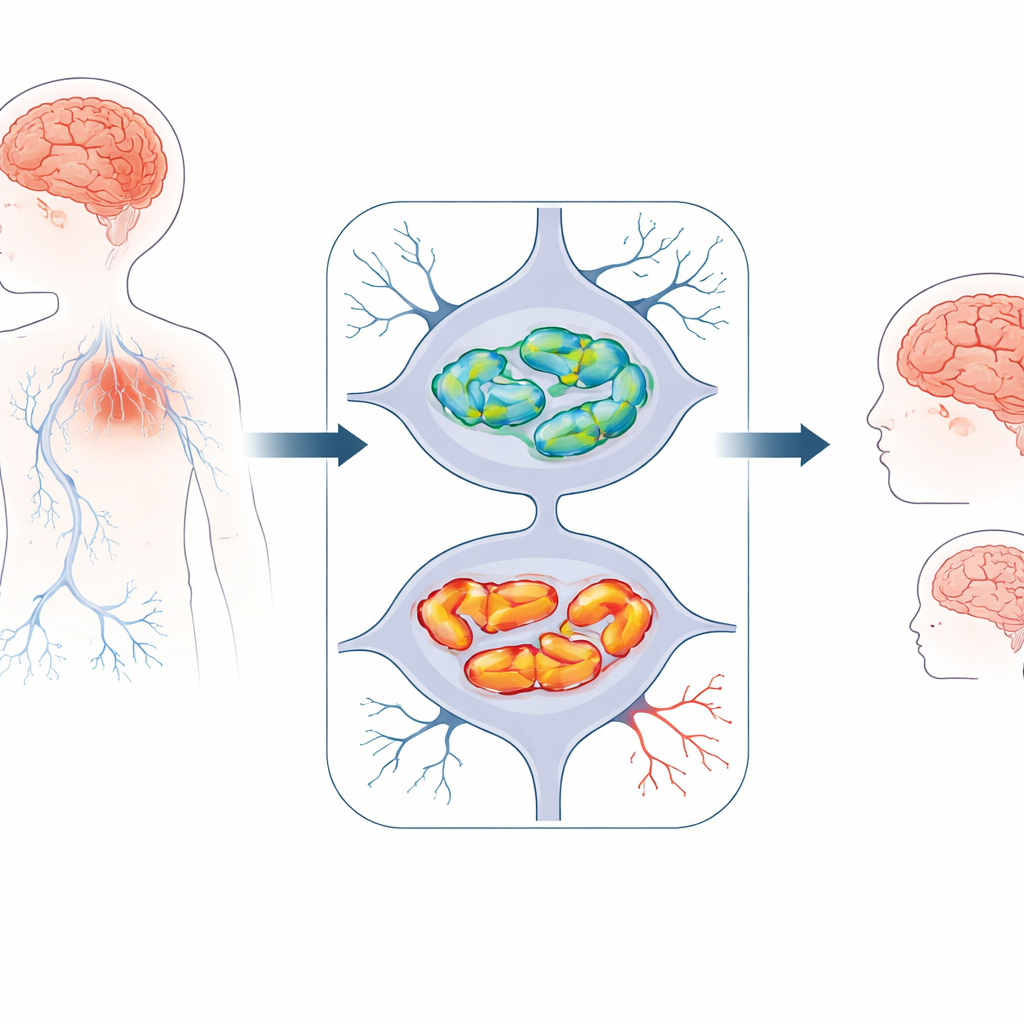
Um distúrbio cerebral infantil recém-reconhecido
Os pesquisadores estudaram três crianças de duas famílias não relacionadas que apresentaram problemas de desenvolvimento precoces. Elas eram menores que o esperado para a idade, aprenderam a sentar, andar e falar mais tarde do que o habitual e, depois, perderam gradualmente parte dessas habilidades. Todas desenvolveram dificuldades de movimento, como marcha instável, rigidez muscular ou tônus muscular reduzido, e convulsões. As imagens cerebrais mostraram um quadro consistente: o tecido tanto do cérebro maior (córtex/cérebro) quanto do “cerebelinho” na parte posterior (cerebelo) tornou-se mais fino ao longo do tempo, e uma ponte importante de fibras nervosas, o corpo caloso, estava incomumente estreita. Essas características apontam para uma perda progressiva de neurônios em vez de uma lesão isolada ao nascimento.
Um gene minúsculo com grandes consequências
Para buscar uma causa hereditária, a equipe sequenciou todos os genes codificadores de proteínas nas crianças afetadas e em seus pais. Eles focalizaram um gene chamado MTNAP1, que ajuda a organizar o DNA dentro das mitocôndrias, as usinas de energia da célula. Cada criança carregava duas cópias defeituosas de MTNAP1, uma herdada de cada pai saudável portador. Em dois irmãos, uma única mudança de “letra” no gene trocou um aminoácido por outro, distorcendo sutilmente a forma da proteína. Na terceira criança, um sinal de parada precoce no gene provavelmente impediu a síntese da proteína. Essas alterações não foram observadas em grandes bancos de dados populacionais, o que fortalece a hipótese de que são variantes raras e danosas, e não simples variações benignas.
Usinas de energia sob estresse
Em seguida, os cientistas examinaram células da pele das crianças e as compararam com células de indivíduos saudáveis. Ao microscópio, as células normais mostraram mitocôndrias longas e filamentosas formando uma rede conectada, enquanto as células das crianças continham mitocôndrias curtas, quebradas e agrupadas. Quando os pesquisadores reduziram experimentalmente os níveis de MTNAP1 em uma linhagem celular humana com características neurais, observaram a mesma fragmentação da rede mitocondrial, confirmando que a perda dessa proteína por si só pode perturbar sua estrutura. Medidas da atividade mitocondrial revelaram que etapas-chave da produção de energia estavam enfraquecidas, e as células produziam excesso de espécies reativas de oxigênio—subprodutos oxidados que agem como ferrugem molecular. As células estressadas pararam de se dividir adequadamente, acumularam-se em uma fase de repouso e ativaram marcadores de envelhecimento prematuro.
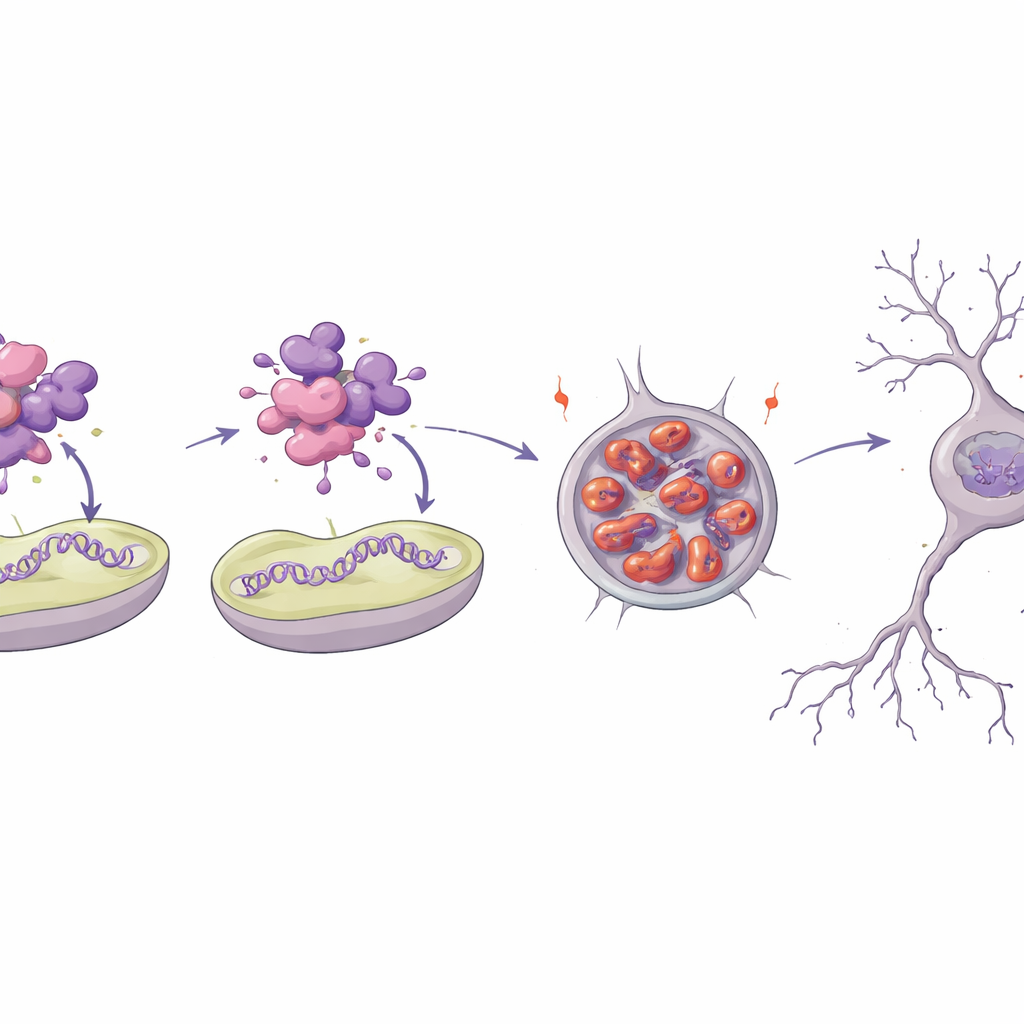
Como uma única alteração desmonta uma proteína vital
Para entender por que uma das variantes é tão destrutiva, a equipe modelou a estrutura 3D da proteína MTNAP1 e a recriou em laboratório. O aminoácido substituído fica em uma região helicoidal compacta que normalmente auxilia a proteína a interagir com o DNA mitocondrial e com a membrana interna. Simulações computacionais e testes biofísicos mostraram que a proteína mutante é menos estável, perde grande parte de sua estrutura ordenada e tende a formar agregados. Em experimentos de tubo de ensaio, a proteína normal ligou-se fortemente a pequenos fragmentos de DNA mitocondrial e a superfícies de membrana artificiais, enquanto a mutante mal interagia e, em vez disso, montava agregados semelhantes a amiloides. Quando introduzida em células com características neurais, a mutante acumulou-se ao longo do tempo em grandes grumos perinucleares, sinal de que os sistemas de controle de qualidade proteica estão sobrecarregados.
De mitocôndrias danificadas a um cérebro que falha
Juntando as peças, o estudo descreve um modelo em etapas: o MTNAP1 defeituoso enfraquece a estrutura que ajuda a organizar o DNA mitocondrial e a ancorá-lo à membrana interna; isso desestabiliza as mitocôndrias, fazendo com que se fragmentem e percam a capacidade de gerar energia de forma eficiente; o aumento do estresse oxidativo e os sinais de “envelhecimento prematuro” celular tornam os neurônios especialmente vulneráveis, já que eles têm demanda energética alta e constante e capacidade limitada de renovação. No cérebro em desenvolvimento, essa crise energética lenta e contínua se traduz em marcos interrompidos, perda de habilidades aprendidas e encolhimento gradual de regiões cerebrais-chave. Embora sejam necessários mais pacientes e estudos em animais para mapear completamente a síndrome, este trabalho posiciona firmemente o MTNAP1 como um guardião crucial da estabilidade mitocondrial e destaca a organização do DNA mitocondrial como um pilar central do desenvolvimento cerebral saudável.
Citação: Kumar, A., Saha, S., Nasir, N. et al. Variants in MTNAP1 underlie a neurodegenerative disorder by impairing mitochondrial stability. npj Genom. Med. 11, 19 (2026). https://doi.org/10.1038/s41525-026-00554-3
Palavras-chave: mitocôndrias, neurodegeneração, genética pediátrica, DNA mitocondrial, desdobramento proteico