Clear Sky Science · pt
Triagem neonatal genômica semi-automatizada destaca complexidades na comunicação de resultados
Por que Pequenas Gotas de Sangue Podem Conter Grandes Respostas
Nos primeiros dias de vida, a maioria dos recém-nascidos já passa por um teste silencioso que salva vidas: a picada no calcanhar que deixa sangue em um cartão. Este estudo investiga o que acontece se dermos um passo além e examinarmos muito mais do código genético do bebê a partir desse mesmo sangue. Os pesquisadores da Austrália do Sul se propuseram a verificar se acrescentar uma análise expansiva do DNA às rotinas de triagem neonatal poderia detectar com segurança mais condições tratáveis cedo — sem sobrecarregar famílias e médicos com informações confusas ou sem utilidade.
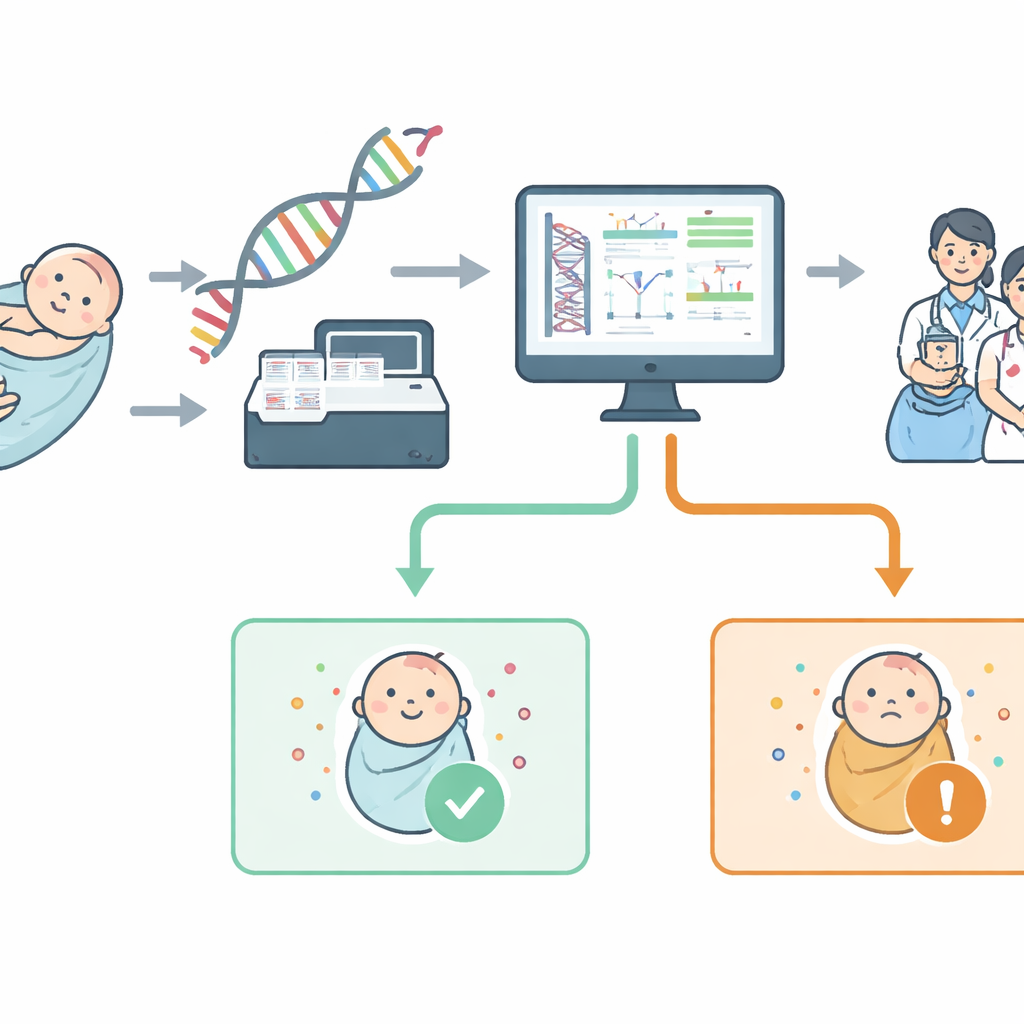
Da Picada no Calcanhar à Varredura do Genoma
A triagem neonatal tradicional busca algumas dezenas de condições medindo substâncias químicas no sangue. Em contraste, a triagem genômica lê trechos de DNA para procurar diretamente mudanças que causam doenças em genes específicos. O projeto NewbornsInSA desenvolveu um teste baseado em sequenciamento do genoma completo, mas deliberadamente limitou a busca a um painel “virtual” de 613 genes. Esses genes foram escolhidos com médicos locais usando regras simples: a condição deve começar na infância, causar problemas de saúde graves, ter uma estratégia significativa de tratamento ou prevenção, e ser detectável de forma confiável no laboratório. Grupos públicos e de pacientes ajudaram em seguida a agrupar essas condições em categorias por sistemas do corpo, para que os pais pudessem entender melhor o que o teste cobre.
Colocando o Novo Teste à Prova
Antes de oferecer essa verificação baseada em DNA às novas famílias, a equipe teve que demonstrar que funcionava. Eles recuperaram 46 cartões de sangue armazenados de crianças cujos diagnósticos genéticos já eram conhecidos, mas foram ocultados dos analistas. Usando sequenciamento do genoma completo e dois sistemas de software separados, perguntaram se seu fluxo de trabalho identificaria corretamente os bebês que realmente tinham uma das condições-alvo. O resultado foi encorajador: o processo encontrou 97% dos casos reais e não produziu alarmes falsos após revisão de especialistas. O único caso perdido destacou uma limitação chave de qualquer triagem baseada em genes — quando a evidência científica por trás de uma alteração específica no DNA é incompleta, computadores e até especialistas podem ser obrigados a rotulá-la como “incerta” e tratá-la como um não-resultado.
Deixando os Computadores Fazerem o Trabalho Pesado
Ler um genoma inteiro gera milhares de variantes para cada bebê — muito mais do que humanos podem inspecionar uma a uma. Para lidar com isso, os pesquisadores construíram um fluxo de trabalho semi-automatizado. Scripts personalizados, integrados a uma plataforma comercial de análise, varrem a lista anotada de variantes e automaticamente deixam de lado bebês que claramente não apresentam achados preocupantes, rotulando-os como “baixa chance”. Apenas casos com alterações que pareçam potencialmente prejudiciais — como variantes conhecidas por causar doenças ou prováveis interrupções deletérias de um gene — são encaminhados a analistas especialistas para revisão detalhada. Nos primeiros 100 recém-nascidos reais testados, essa automação reduziu imediatamente o número de bebês que precisavam de revisão manual em mais da metade, um passo crucial se tal triagem for ampliada para populações inteiras.
Bebês Reais, Decisões Reais
Quando a equipe aplicou o fluxo de trabalho aos primeiros 100 recém-nascidos incluídos, cinco bebês receberam resultados sugerindo alta probabilidade de uma condição específica. Entre eles estavam distúrbios do ritmo cardíaco que podem causar batimentos perigosamente irregulares, um problema metabólico já suspeito pela triagem padrão, uma alteração gênica que torna certos antibióticos arriscados para a audição, e uma forma leve de hiperglicemia hereditária. Em cada caso, o resultado desencadeou seguimento sob medida: avaliações cardíacas e monitoramento contínuo, alertas eletrônicos para evitar determinados medicamentos, ou planejamento para cuidados em gravidezes futuras. Ao mesmo tempo, muitos outros achados foram deliberadamente não reportados porque estavam ligados a sintomas leves, cânceres de início adulto, risco incerto ou padrões complexos que o conhecimento atual não consegue interpretar com confiança em um recém-nascido saudável. Essas decisões delicadas exigiram horas de leitura da literatura e discussão entre geneticistas e especialistas, ressaltando que o julgamento de especialistas continua sendo essencial.
Equilibrando Ajuda Precoce e Encargos Futuros
Este trabalho mostra que é tecnicamente possível usar dados do genoma completo a partir de uma pequena gota de sangue para detectar mais condições infantis tratáveis do que os testes padrão, com alta precisão e apoio de software inteligente. Mas também expõe a corda bamba ética e prática: cada gene adicional examinado aumenta a chance de descobrir informações que podem não ajudar o bebê agora, podem preocupar os pais, ou só se tornar relevantes décadas depois. A abordagem semi-automatizada e cuidadosamente curada da equipe NewbornsInSA — em que os computadores descartam negativos claros e os humanos se concentram nos casos mais sutis — oferece um modelo de como a triagem genômica neonatal pode ser implementada de forma responsável, enquanto estudos de seguimento em andamento monitoram seus benefícios e riscos no mundo real para as famílias.
Citação: Chowdhury, A., Marri, S., Anastasi, L. et al. Semi-automated genomic newborn screening highlights complexities in reporting. npj Genom. Med. 11, 13 (2026). https://doi.org/10.1038/s41525-026-00553-4
Palavras-chave: triagem neonatal genômica, sequenciamento do genoma completo, gotas de sangue secas, interpretação de variantes genéticas, detecção precoce de doenças raras