Clear Sky Science · pt
Imunocitoquimioterapia local programável para câncer de mama triplo-negativo via liberação espaço-temporalmente controlada de oligodeoxinucleotídeos CpG, gemcitabina e paclitaxel
Transformando um câncer de mama difícil em um alvo local
O câncer de mama triplo-negativo é uma das formas mais difíceis de tratar porque carece dos interruptores moleculares usuais aos quais muitos medicamentos modernos se ligam. Pacientes frequentemente precisam recorrer a quimioterapias potentes que circulam por todo o corpo, causando efeitos colaterais graves e, com frequência, controle a longo prazo insatisfatório. Este estudo explora uma ideia bem diferente: em vez de inundar o corpo com remédios, seria possível colocar um minúsculo depósito de medicamento programável ao lado do tumor, liberando agentes quimioterápicos e imunoestimuladores em uma sequência cuidadosamente temporizada exatamente onde são mais necessários?
Um depósito minúsculo com grandes ambições
Os pesquisadores criaram o que chamam de Plataforma de Imunocitoquimioterapia Local Programável, ou PLICT. Pense nisso como uma pequena esfera injetável e macia que fica ao lado de um tumor de mama e libera o tratamento lentamente ao longo de semanas. A esfera combina um gel hidrofílico que libera rapidamente um estimulador imune e um quimioterápico, a gemcitabina, com microesferas plásticas microscópicas que liberam lentamente um segundo fármaco, o paclitaxel. O estimulador imune, um pequeno trecho de DNA chamado CpG, foi projetado para despertar células imunes locais, enquanto as quimioterapias emparelhadas atacam diretamente as células tumorais e remodelam o microambiente do tumor para que as células imunes possam entrar e agir.
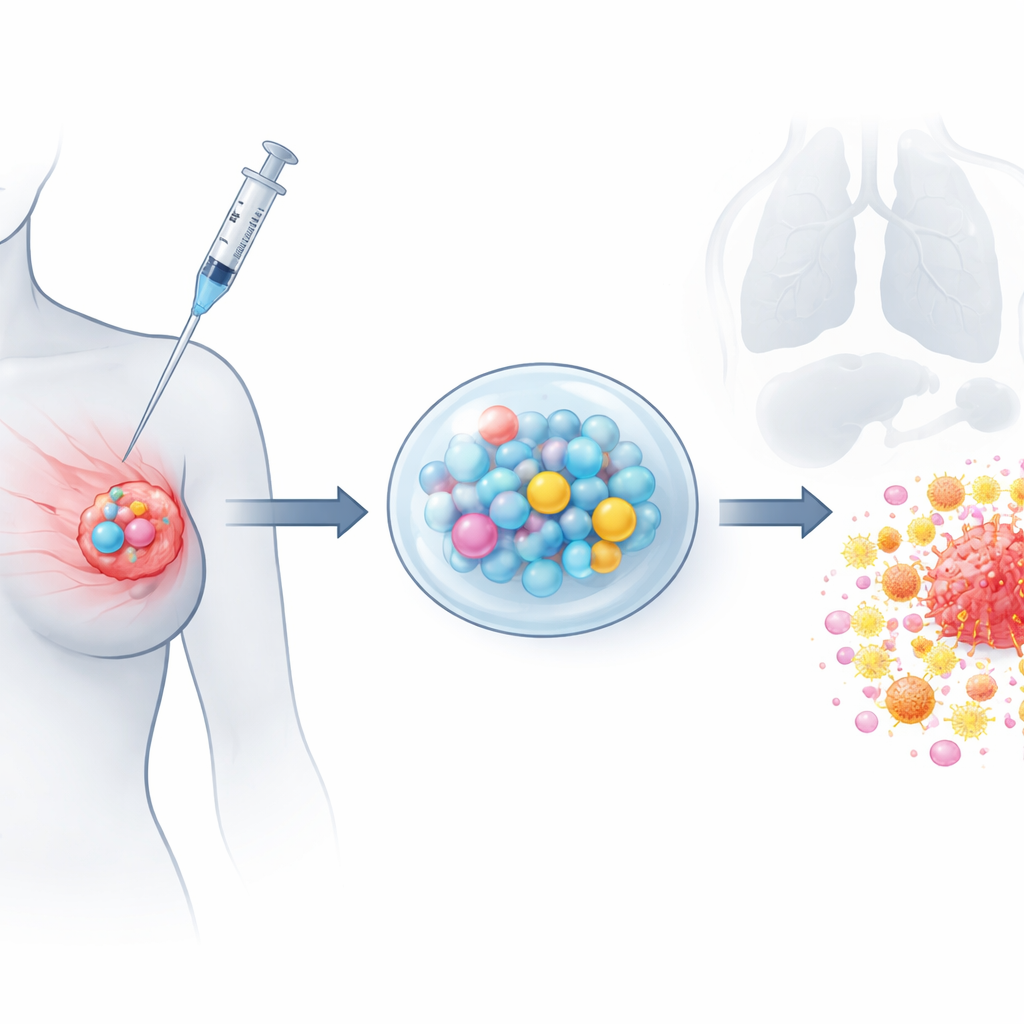
Engenharia de um ataque de liberação temporizada contra o câncer
Para construir esse sistema, a equipe usou um método de alta tensão chamado “electrospray” para formar microesferas uniformes carregadas com paclitaxel a partir de um polímero biodegradável. Imagens mostraram partículas lisas e esféricas com cerca de um décimo da largura de um fio de cabelo humano, e testes de laboratório confirmaram que o paclitaxel vazava de forma constante por pelo menos um mês sem um estouro inicial. Separadamente, eles incorporaram gemcitabina e CpG em um gel termossensível que é líquido quando resfriado e se torna semi-sólido na temperatura corporal. A caracterização química verificou que ambos os fármacos permaneceram intactos dentro de seus transportadores. Quando combinados, o gel fornece uma dose rápida e precoce de gemcitabina e CpG, enquanto as microesferas oferecem um gotejamento prolongado de paclitaxel, imitando os benefícios de uma quimioterapia de baixa dose e longa duração a partir de uma única aplicação local.
Testando a estratégia local em camundongos
A equipe então testou o PLICT em um modelo murino de câncer de mama triplo-negativo. Os camundongos primeiro desenvolveram pequenos tumores mamários e, em seguida, receberam ou injeções padrão de paclitaxel sozinho, paclitaxel mais gemcitabina, ou um único implante local de PLICT próximo ao tumor. Ao longo de quatro semanas, os tumores do grupo controle cresceram rapidamente, aqueles submetidos à quimioterapia padrão cresceram mais devagar, mas os tumores tratados com PLICT foram dramaticamente menores em tamanho e peso. Imagens do animal inteiro e de órgãos removidos mostraram que o PLICT também reduziu a disseminação do câncer para locais distantes, especialmente os pulmões, de forma mais eficaz do que as injeções convencionais. Medições dos níveis de fármaco revelaram o porquê: o paclitaxel estava altamente concentrado dentro dos tumores tratados com PLICT, mas em baixa concentração em tecidos adiposos distantes e similar no sangue, sugerindo forte retenção local com menos exposições fora do alvo.
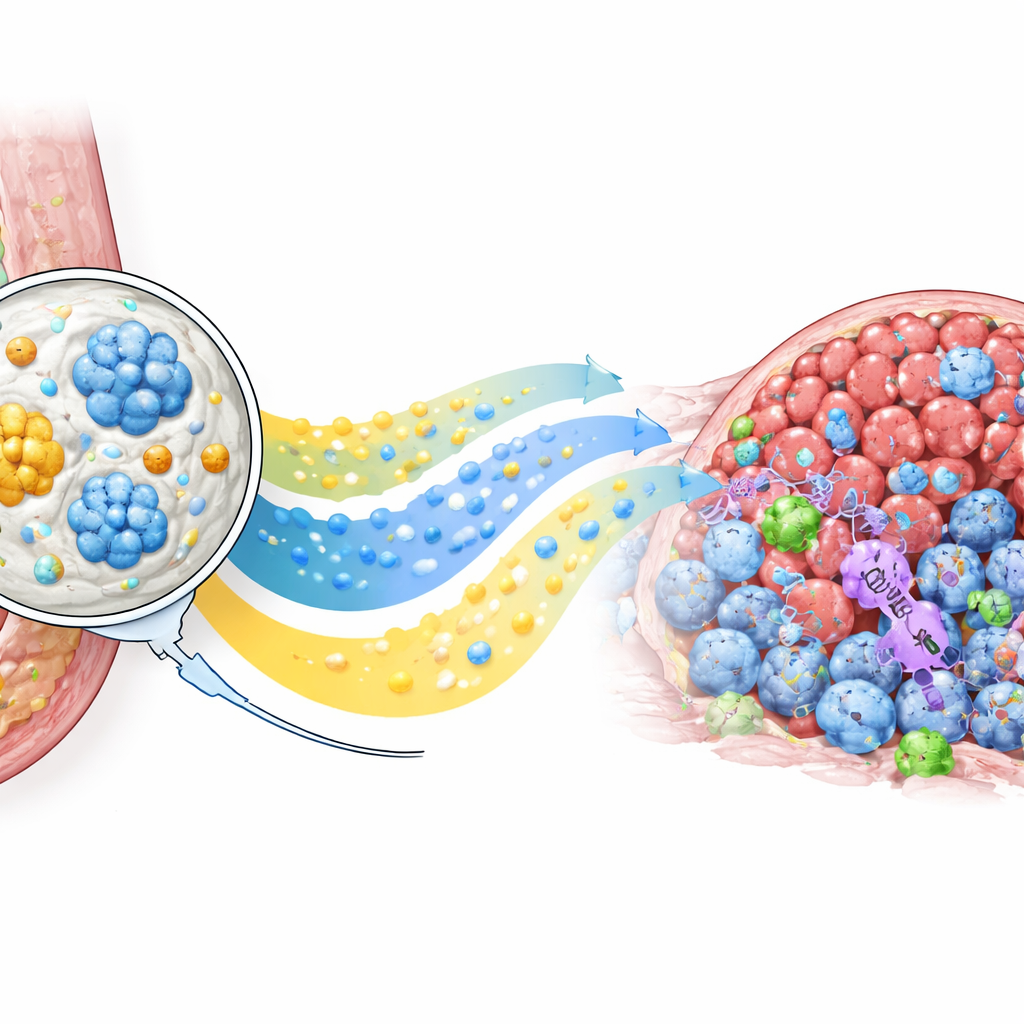
Recrutando os próprios defensores do corpo
Além de reduzir os tumores, o PLICT alterou o panorama imune dentro deles. Análises celulares detalhadas mostraram um aumento acentuado de células T CD8 citotóxicas nos tumores tratados com PLICT em comparação com todos os outros grupos, juntamente com uma queda em certos linfócitos T reguladores que normalmente atenuam os ataques imunes. A coloração tecidual para CD69, um marcador de células T recentemente ativadas, confirmou que muitas dessas células infiltrantes estavam ativadas e prontas para agir. Ao mesmo tempo, a quimioterapia padrão causou danos perceptíveis ao tecido hepático, enquanto órgãos de camundongos tratados com PLICT pareceram quase normais ao microscópio. Em conjunto, esses achados indicam que o depósito local não apenas aumenta a exposição direta ao fármaco no tumor, mas também desencadeia uma resposta imune mais favorável e menos suprimida sem acrescentar estresse extra aos órgãos vitais.
O que isso pode significar para o futuro do tratamento do câncer
Para não especialistas, a mensagem é direta: ao transformar a quimioterapia e a estimulação imune em um gotejamento lento e precisamente escalonado entregue ao lado do tumor, essa abordagem alcançou controle tumoral mais forte e menos efeitos colaterais sistêmicos em animais do que injeções padrão de medicamentos. O trabalho ainda está em estágio pré-clínico, e permanecem questões sobre quão bem tal sistema funcionaria em humanos ou em diferentes cenários de tratamento. Mas o conceito de um “depósito de medicamentos” injetável e programável que libera discretamente múltiplos agentes em sequência pode abrir novas maneiras de tratar cânceres agressivos como o triplo-negativo — concentrando a luta onde importa mais e poupando o restante do corpo.
Citação: Hsieh, CH., Hsu, MY., Lin, CF. et al. Programmable local immunochemotherapy for triple-negative breast cancer via spatiotemporally controlled release of CpG oligodeoxynucleotides, gemcitabine, and paclitaxel. npj Breast Cancer 12, 45 (2026). https://doi.org/10.1038/s41523-026-00910-7
Palavras-chave: câncer de mama triplo-negativo, liberação local de fármacos, imunoterapia, liberação controlada, microesferas de hidrogel