Clear Sky Science · pt
Expressão de genes-alvo do receptor de estrogênio β revela novas funções repressoras em câncer de mama agressivo
Por que essa pesquisa importa
O câncer de mama inflamatório é uma das formas mais agressivas e letais de câncer de mama, frequentemente se espalhando rapidamente e deixando poucas opções de tratamento direcionado aos pacientes. Este estudo explora um sensor hormonal menos conhecido nas células mamárias, chamado receptor de estrogênio beta, e mostra como ele pode atuar como um freio natural à disseminação tumoral. Entender como esse freio interno funciona pode abrir caminho para novos medicamentos que retardem ou previnam a metástase em pacientes que atualmente têm escolhas muito limitadas.
Uma face diferente do câncer de mama inflamatório
Ao contrário de muitos cânceres de mama que dependem do receptor clássico de estrogênio alfa, o câncer de mama inflamatório normalmente carece dessa molécula e, portanto, não responde bem às terapias hormonais padrão. Os autores focam, em vez disso, em um segundo receptor de estrogênio, o receptor de estrogênio beta (ERβ), que eles haviam vinculado anteriormente a menos metástases tanto em pacientes quanto em modelos de camundongo. Trabalhos anteriores sugeriram que o ERβ desacelera o maquinário interno da célula responsável pela arquitetura e movimento. Neste estudo, a equipe buscou mapear, em todo o genoma, como o ERβ altera a atividade gênica e quais moléculas a jusante poderiam explicar seu papel protetor e antimetastático.
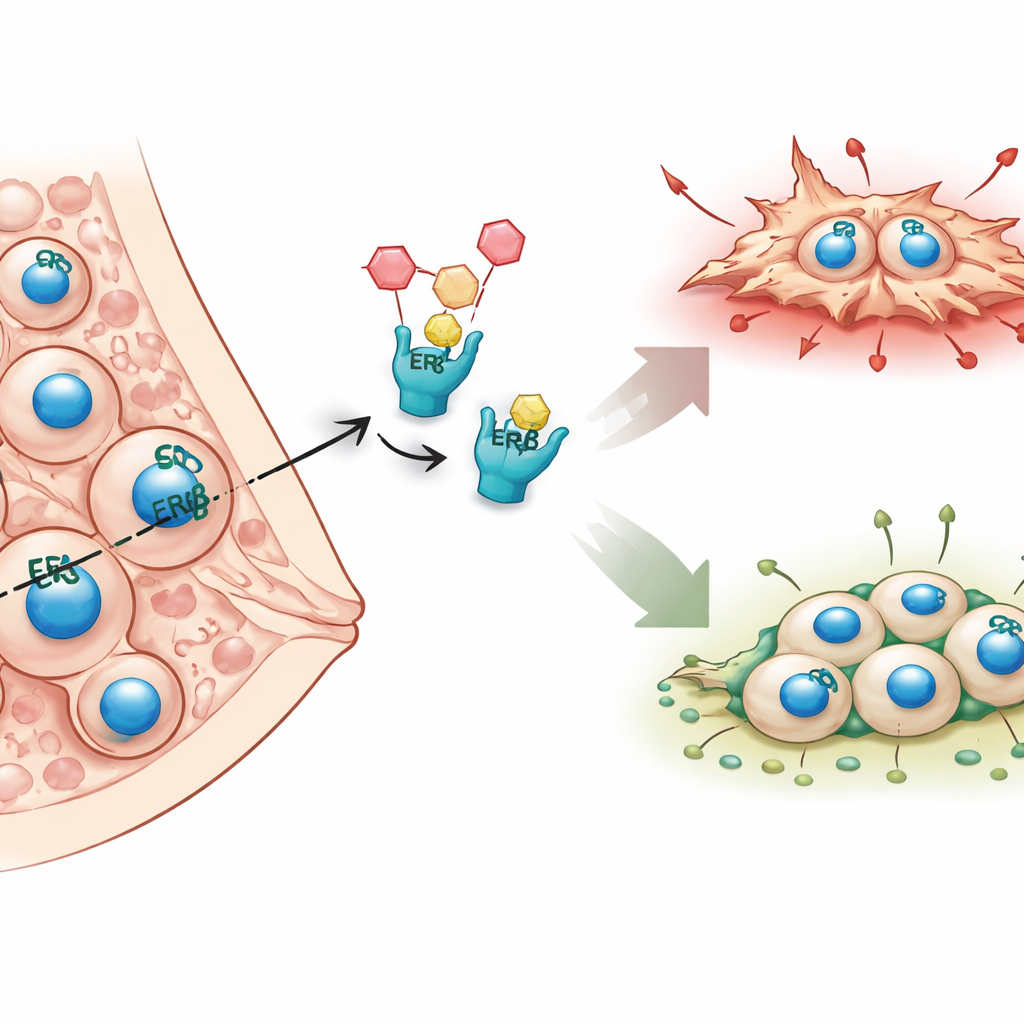
Lendo o manual de instruções da célula cancerosa
Para revelar a influência do ERβ, os pesquisadores utilizaram duas abordagens poderosas de sequenciamento em linhas celulares de câncer de mama inflamatório. Um método, ChIP-seq, aponta exatamente onde o ERβ se liga ao DNA, como sinalizar páginas e linhas específicas no manual de instruções da célula. O outro método, RNA-seq, mede quais genes são ativados ou reprimidos quando o ERβ está presente, ausente ou ativado por um fármaco seletivo. Ao comparar esses conjuntos de dados, eles encontraram milhares de sítios de DNA ligados pelo ERβ, a maioria não apenas em interruptores de ligar/desligar genes, mas profundamente dentro ou entre genes, sugerindo um controle de amplo alcance. Também descobriram que o ERβ frequentemente trabalha em conjunto com famílias de outros fatores de transcrição, formando complexos que coletivamente decidem quais genes são silenciados ou ativados.
Reprogramando crescimento, movimento e metabolismo
A análise integrada mostrou que o ERβ tende a reduzir a expressão de genes que promovem movimento celular, mudanças de forma e invasão, especialmente aqueles ligados ao citoesqueleto de actina e à sinalização de GTPases Rho — vias conhecidas por impulsionar a metástase. Ao mesmo tempo, o ERβ sustenta programas gênicos associados ao desenvolvimento tecidual e à diferenciação celular, empurrando as células cancerosas em direção a um estado mais estável e menos agressivo. O estudo também revelou um papel surpreendente do ERβ em ajustar vias metabólicas, particularmente as que envolvem ácidos graxos e fosfolipídios, que são combustíveis e blocos de construção-chave para tumores de crescimento rápido. Importante, esses efeitos foram observados não apenas em células modificadas para superexpressar ERβ, mas também em células com níveis naturais do receptor, reforçando sua relevância no contexto clínico.
Pequenas mensageiras de RNA e impacto clínico
Além de genes codificadores de proteínas, a equipe examinou microRNAs — pequenas moléculas de RNA que afinam a expressão gênica. Eles identificaram dezenas de microRNAs cujos níveis mudaram quando o ERβ foi removido ou restaurado, muitos dos quais já foram associados à supressão tumoral no câncer de mama. Ao conectar esses microRNAs a seus genes-alvo, os autores mostraram que o ERβ controla indiretamente alguns motores do câncer, por meio de uma rede regulatória em camadas. Em seguida, voltaram-se para dados de pacientes, examinando tumores de indivíduos com câncer de mama inflamatório e não inflamatório. Diversos genes controlados pelo ERβ se mostraram fortemente ligados à sobrevida dos pacientes: altos níveis de alguns (como SERPINA1 e HSPB8) previram melhores desfechos, enquanto altos níveis de outros (como PITX1 e HOMER3) estiveram associados a pior sobrevida. Isso posiciona essas moléculas a jusante como potenciais marcadores prognósticos e futuros alvos terapêuticos.
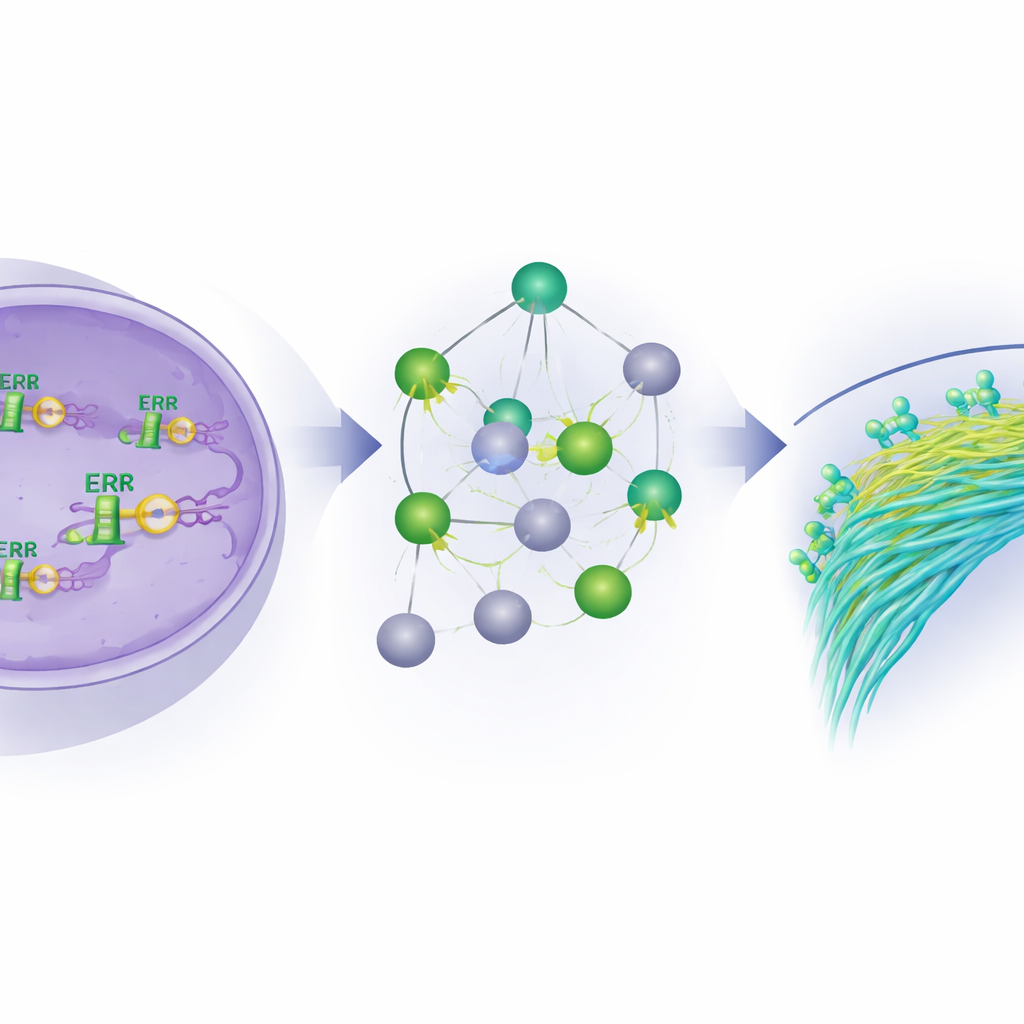
Do freio molecular às terapias futuras
Em conjunto, o estudo apresenta o ERβ como um freio central ao comportamento invasivo das células do câncer de mama inflamatório. Ao se ligar ao DNA, fazer parcerias com outros reguladores e moldar tanto redes de genes quanto de microRNAs, o ERβ silencia programas que impulsionam migração celular e metástase, ao mesmo tempo que promove estados mais estáveis e diferenciados e reorienta o metabolismo do câncer. Para os pacientes, isso sugere que fármacos que ativem o ERβ ou que inibam seus principais alvos a jusante — especialmente aqueles envolvidos no movimento celular e no uso de ácidos graxos — poderiam formar a base de novos tratamentos mais precisos para essa doença difícil de tratar.
Citação: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
Palavras-chave: câncer de mama inflamatório, receptor de estrogênio beta, metástase, regulação gênica, metabolismo do câncer