Clear Sky Science · pt
O eixo CXCL10/CXCR3 é essencial para sustentar a dormência imunológica no câncer de mama triplo‑negativo
Por que alguns cânceres “dormem” em vez de se espalhar
O câncer de mama às vezes se comporta como um agente adormecido. Após o tratamento inicial, algumas células tumorais podem se ocultar no organismo por anos, sem crescer o suficiente para serem detectadas por exames — mas ainda capazes de despertar mais tarde e causar metástases potencialmente fatais. Este estudo investiga por que esse estado de “sono”, chamado dormência, ocorre em uma forma particularmente agressiva da doença, o câncer de mama triplo‑negativo, e identifica um sinal químico que ajuda o sistema imunológico a manter essas células sob controle.
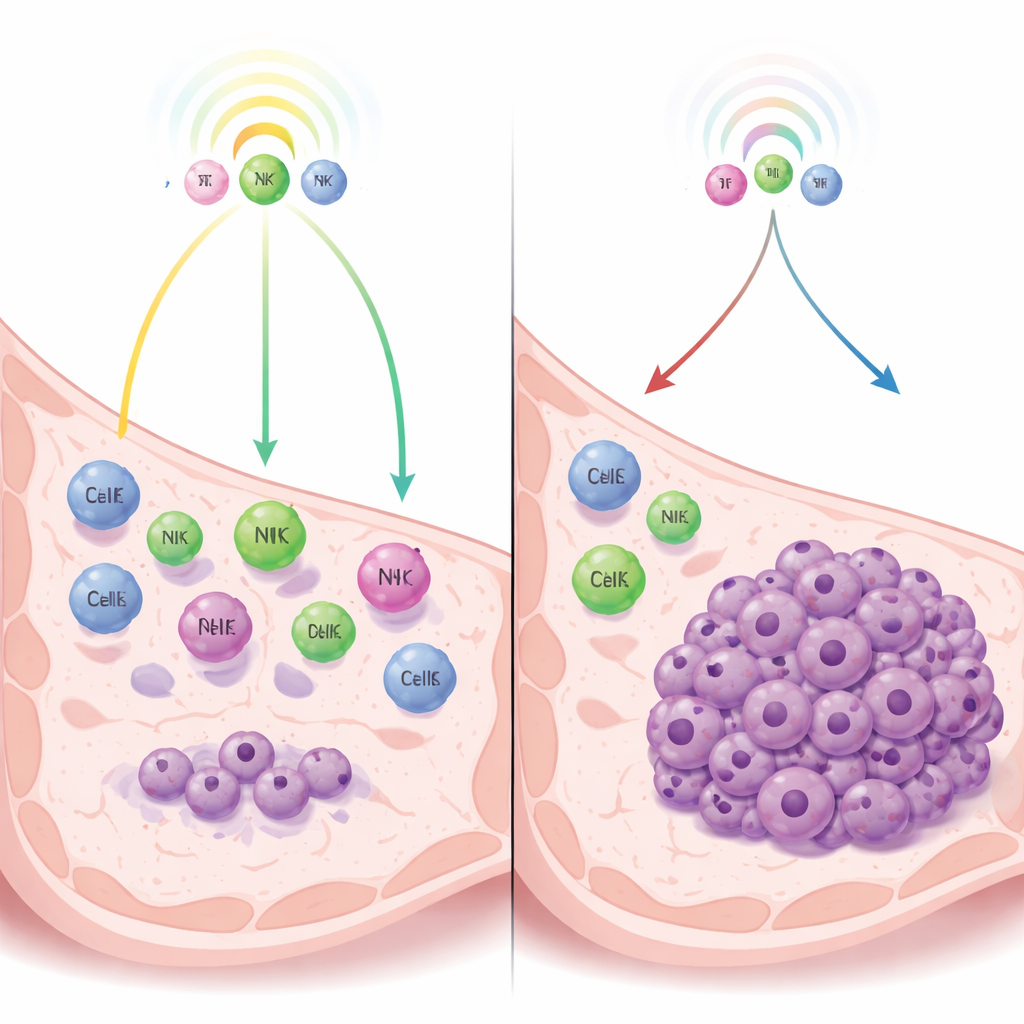
Uma disputa entre o câncer e o sistema imune
Os autores concentram‑se em um tipo de dormência controlada não pela falta de suprimento sanguíneo ou por freios internos das células, mas pela vigilância imunológica — a vigilância constante feita pelas células imunes que pode conter tumores sem eliminá‑los por completo. Usando modelos de camundongo de câncer de mama triplo‑negativo, eles comparam células tumorais que permanecem espontaneamente dormentes com células intimamente relacionadas que formam tumores de crescimento rápido. Ao examinar quais genes estão ativados, descobrem que as células dormentes ativam fortemente vias de interferon — sistemas de alarme imune que estimulam a liberação de mensageiros químicos que atraem células imunes para a área tumoral.
Um mensageiro químico chave que mantém os tumores silenciosos
Entre as muitas moléculas ativadas nas células dormentes, uma se destaca: CXCL10, uma pequena proteína que funciona como um farol para células imunes que carregam seu receptor parceiro, CXCR3. Células cancerosas dormentes produzem bem mais CXCL10 do que suas contrapartes agressivas. Quando os pesquisadores desativam deliberadamente o CXCL10 em células dormentes e as implantam em camundongos com sistemas imunes intactos, as células antes silenciosas formam tumores rapidamente. Bloquear o receptor CXCR3 com um anticorpo tem efeito similar. Em ambos os casos, as células cancerosas escapam do impasse imune e começam a crescer, mostrando que o eixo CXCL10/CXCR3 não está apenas correlacionado com a dormência — ele é necessário para mantê‑la.
Como mudar o bairro local muda o equilíbrio
Reduzir o CXCL10 faz mais do que alterar uma única via; remodela todo o cenário imune local. Em tumores que perderam CXCL10, células T CD4 e CD8 benéficas são reduzidas, enquanto certos células mieloides capazes de suprimir respostas imunes tornam‑se mais abundantes. Células natural killer e células dendríticas também variam em número. Esse padrão aparece tanto em tumores primários quanto nos pulmões, para onde células cancerosas podem viajar e permanecer adormecidas. Mesmo quando metástases pulmonares são pequenas demais para serem vistas ao microscópio, marcadores moleculares mostram que mais células tumorais conseguem semear os pulmões na ausência de CXCL10, e menos células T infiltram esses tecidos. Ainda assim, em camundongos que não têm um sistema imune funcional, remover o CXCL10 não faz diferença — células dormentes crescem independentemente — ressaltando que esse sinal age por meio do controle imune, e não como um freio direto ao crescimento das células cancerosas.
Por que mais sinal ajuda, mas não é um interruptor mágico
A equipe também testa a ideia oposta: aumentar o CXCL10 pode transformar um tumor agressivo em dormente? Quando eles modificam células cancerosas de crescimento rápido para produzir CXCL10 extra, os tumores crescem mais lentamente e demoram mais a aparecer, e alguns tipos de células imunes no sangue aumentam. No entanto, a dormência completa não se estabelece; eventualmente todos os camundongos ainda desenvolvem tumores. Isso sugere que, embora o CXCL10 seja essencial para manter a dormência quando o restante da maquinaria imune está presente, ele não consegue sozinho construir esse estado complexo do zero. Outras vias devem cooperar para criar um equilíbrio duradouro entre ataque imunológico e sobrevivência das células tumorais.
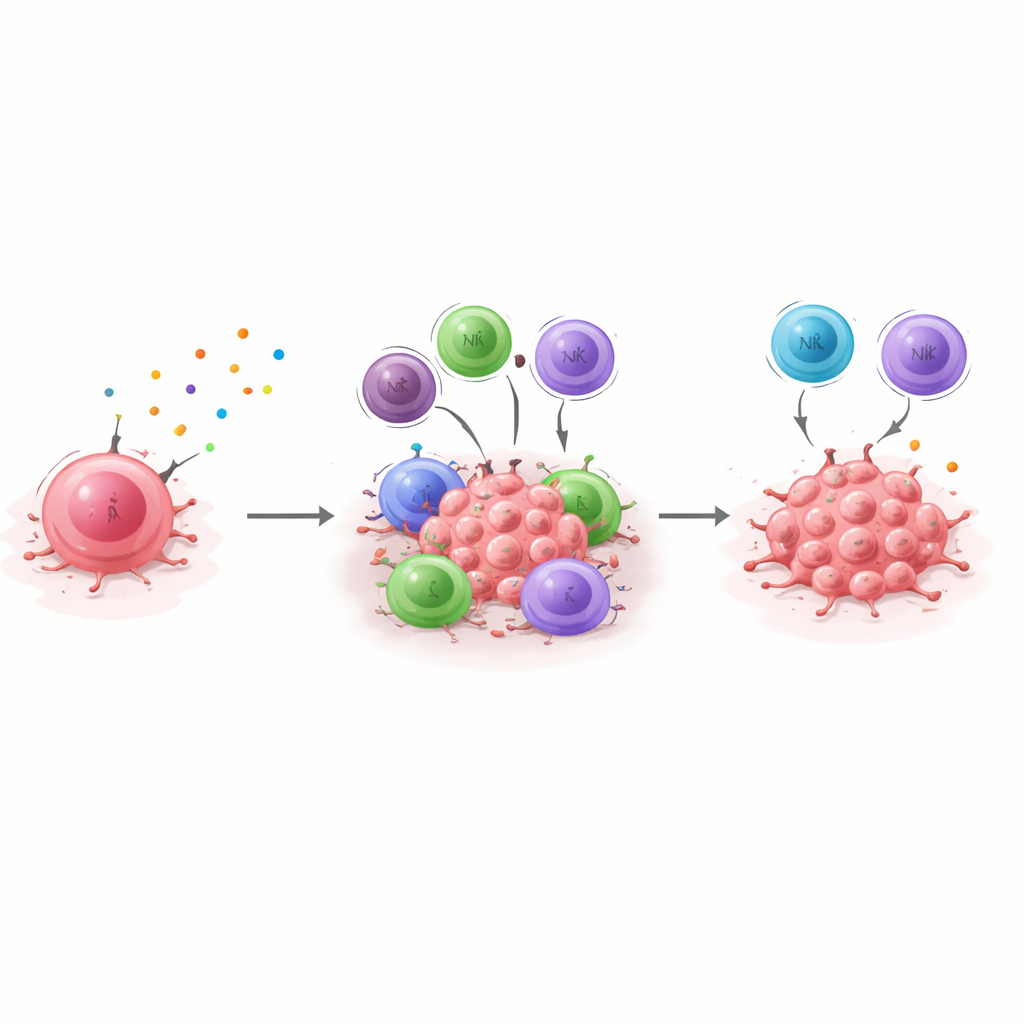
De experimentos em camundongos à perspectiva clínica
Para conectar suas descobertas à doença humana, os pesquisadores derivam uma “assinatura de dormência” — um conjunto de genes consistentemente mais altos em células dormentes e que caem quando o CXCL10 é silenciado. Em seguida, eles analisam grandes conjuntos de dados de pacientes com câncer de mama e investigam como essa assinatura se relaciona com a sobrevida. No câncer de mama triplo‑negativo, pacientes cujos tumores expressam essa assinatura de dormência em níveis mais altos vivem mais tempo em geral e tendem a permanecer livres de recidiva por mais anos, consistente com um estado dormente controlado pelo sistema imune que atrasa a recorrência. O efeito não é observado da mesma forma em tumores hormonais positivos, destacando diferenças biológicas entre subtipos de câncer de mama. Em conjunto, os resultados sugerem que o eixo CXCL10/CXCR3 é um pilar central da dormência mediada pelo sistema imune no câncer de mama triplo‑negativo, e que medir essa assinatura de dormência pode ajudar a identificar pacientes mais propensos a se beneficiar de terapias que reforcem o controle imune — ou, inversamente, aqueles que podem precisar de monitoramento de longo prazo mais atento porque seu câncer está menos bem contido.
Citação: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
Palavras-chave: câncer de mama triplo‑negativo, dormência tumoral, vigilância imunológica, sinalização de quimiocinas, eixo CXCL10 CXCR3