Clear Sky Science · pt
Análise espacial da expressão gênica revela motores da metástase em gânglios linfáticos extremamente precoce no câncer de mama
Por que pequenas células cancerosas viajantes importam
Quando o câncer de mama se espalha além da mama, frequentemente estaciona primeiro nos gânglios linfáticos próximos — pequenos filtros que ajudam a combater infecções. Os médicos sabem que encontrar câncer nesses gânglios normalmente indica maior risco de recidiva. Mas o que realmente acontece nos momentos iniciais, quando apenas algumas células chegam a um gânglio linfático, tem sido quase impossível de observar em pacientes reais. Este estudo usou um novo tipo de “mapa” microscópico da atividade gênica para acompanhar esses passos iniciais com detalhes sem precedentes, revelando quais células têm sucesso, quais falham e por que isso importa para o desfecho dos pacientes.
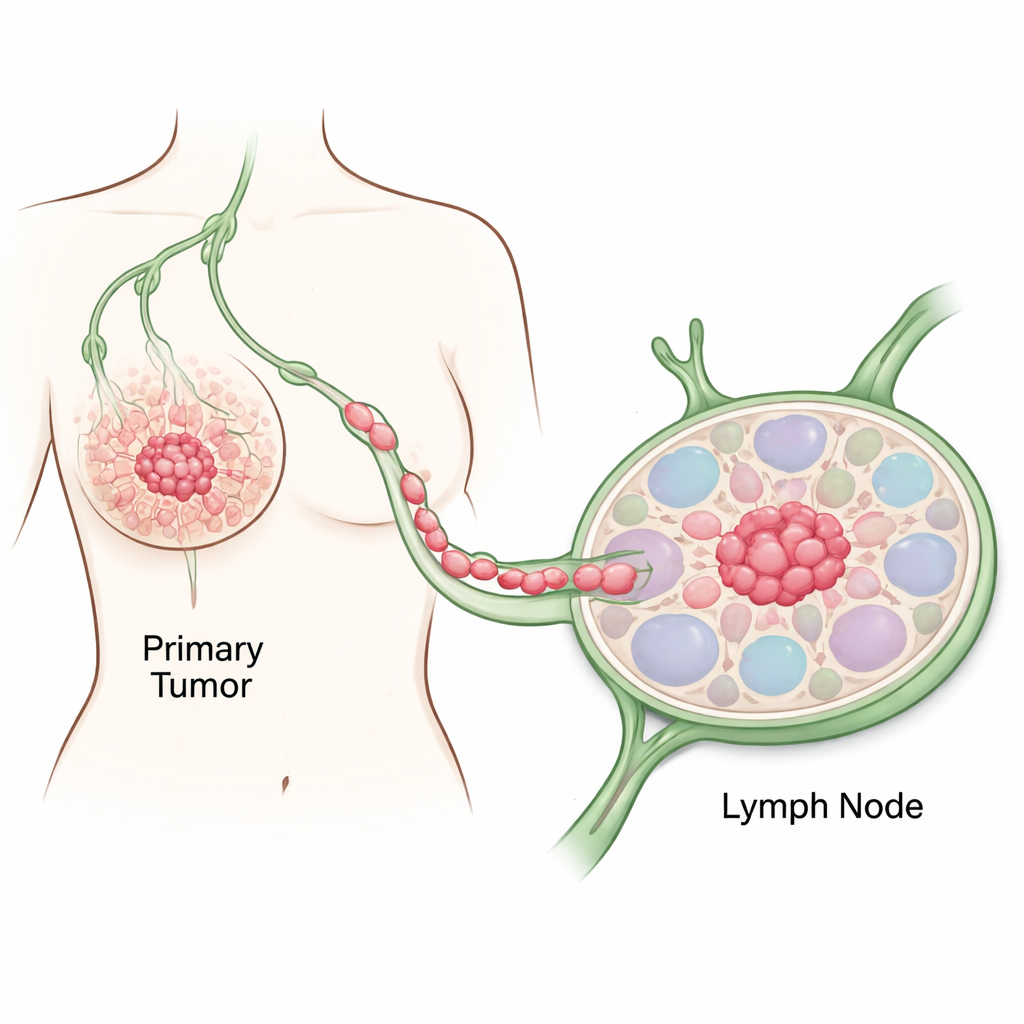
Seguindo os primeiros passos do câncer
Os pesquisadores focaram em tecido de uma mulher de 80 anos com um câncer de mama agressivo, HER2-positivo. Amostraram tanto áreas de aparência normal da mama quanto regiões tumorais próximas, e então usaram múltiplos testes de DNA e RNA para traçar como células comuns se tornaram cancerosas. Em comparação com tecido saudável, as regiões tumorais exibiram sinais clássicos do câncer: adesão celular interrompida, divisão celular hiperativa, alterações em larga escala na metilação do DNA e mutações-chave em genes que controlam crescimento e estabilidade do genoma. Essas mudanças moleculares coincidiram com o que os patologistas viram ao microscópio, confirmando uma progressão etapa a etapa de células mamárias normais a células plenamente malignas.
Células que mudam de forma em movimento
Para entender como células tumorais começam a viajar, a equipe usou uma técnica de alta resolução que lê a atividade gênica em células individuais mantendo suas posições exatas no tecido. Isso permitiu reconstruir como as células cancerosas mudaram de identidade ao sair das estruturas mamárias normais e se moverem rumo à metástase. Eles descobriram que o câncer parecia surgir de um tipo particular de célula mamária madura, que gradualmente adotou características de um processo chamado transição epitélio–mesenquimal — uma espécie de mudança de forma que ajuda as células a se soltarem, se moverem e invadirem tecido próximo. Em vez de um interruptor simples ligado/desligado, as células ocuparam um espectro de estados mistos, mesclando traços “epiteliais” (ordenados, aderidos) com traços “mesenquimais” (móveis, invasivos). Algumas dessas células híbridas dispersearam pelo tumor, enquanto outras se agruparam em populações mais avançadas preparadas para se espalhar aos gânglios linfáticos.
O primeiro cabeço remoto em um gânglio linfático
Em um gânglio linfático que foi considerado livre de metástase pelos testes clínicos padrão, os cientistas notaram algo notável: apenas 30 células tumorais perdidas, ocupando uma região de cerca de 200 micrômetros de largura — aproximadamente o dobro da espessura de um fio de cabelo humano. Essas células tumorais isoladas provinham de vários estados híbridos distintos, cada um com seu próprio padrão de atividade gênica. Ao agrupar células cancerosas relacionadas, a equipe definiu seis subtipos com papéis diferentes. Um subtipo, fortemente “mesenquimal”, parecia especialmente apto a resistir à morte celular e escapar do ataque imune. Outro subtipo, que recuperou mais características epiteliais, mostrou uma mudança marcante em seu uso de energia, favorecendo o metabolismo de ácidos graxos. Somente esse grupo metabolicamente reprogramado e mais epitelialmente parecido formou com sucesso pequenas colônias nos gânglios linfáticos, sugerindo que a escolha do combustível — não apenas a capacidade de invasão — ajuda a determinar se as chegadas iniciais conseguem se estabelecer.
Um gânglio linfático que silenciosamente ajuda o câncer
O estudo também examinou como o ambiente do gânglio linfático respondeu a esses intrusos. Mesmo antes de uma metástase visível se formar, células imunes, células vasculares e tecido conjuntivo já estavam enviando sinais que atenuavam reações imunes e apoiavam a sobrevivência tumoral. Certos pares receptor–ligante entre células imunes sugeriram tolerância imune precoce, enquanto outros incentivavam o crescimento de novos vasos sanguíneos e a remodelação da matriz tecidual. Juntas, essas mudanças construíram um nicho surpreendentemente acolhedor para as células cancerosas metabolicamente adaptadas, ajudando-as a sobreviver, crescer e potencialmente semear disseminações futuras.
O que isso significa para os pacientes
Ao comparar suas descobertas com grandes conjuntos de dados de pacientes existentes, os pesquisadores fizeram uma descoberta contraintuitiva. As células mais aptas a formar colônias iniciais em gânglios linfáticos, e mesmo aquelas com características mesenquimais mais fortes, não corresponderam aos piores desfechos clínicos. Em vez disso, os pacientes tiveram prognóstico pior quando seus tumores abrigavam certos tipos híbridos agressivos marcados por alta atividade do ciclo celular e programas de queima de açúcar (glicólise) impulsionados por genes como MYC. Em outras palavras, diferentes estados de células que mudam de forma parecem se especializar: alguns são especialistas em colonizar silenciosamente novos sítios, enquanto outros impulsionam crescimento rápido e recidiva. Entender e direcionar esses estados celulares distintos e suas preferências metabólicas pode levar a tratamentos mais precisos — que não apenas detectem a disseminação mais precoce de forma mais confiável, mas também cortem os tipos de células tumorais mais propensas a causar recaídas fatais.
Citação: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
Palavras-chave: metástase do câncer de mama, gânglio linfático, transição epitélio-mesenquimal, transcriptômica espacial, metabolismo do câncer