Clear Sky Science · pt
Sinalização de CD52 via Siglec-G de macrófagos representa um alvo terapêutico para imunoterapia do câncer
Por que alguns cânceres de mama se escondem do sistema imunológico
O câncer de mama triplo‑negativo é uma das formas mais perigosas de câncer de mama porque se espalha rapidamente e carece de muitos dos alvos comuns de tratamento. Este estudo investiga uma forma recém‑descoberta pela qual esses tumores podem escapar das defesas do organismo e mostra como bloquear essa rota de fuga pode tornar as terapias baseadas no sistema imune mais eficazes.
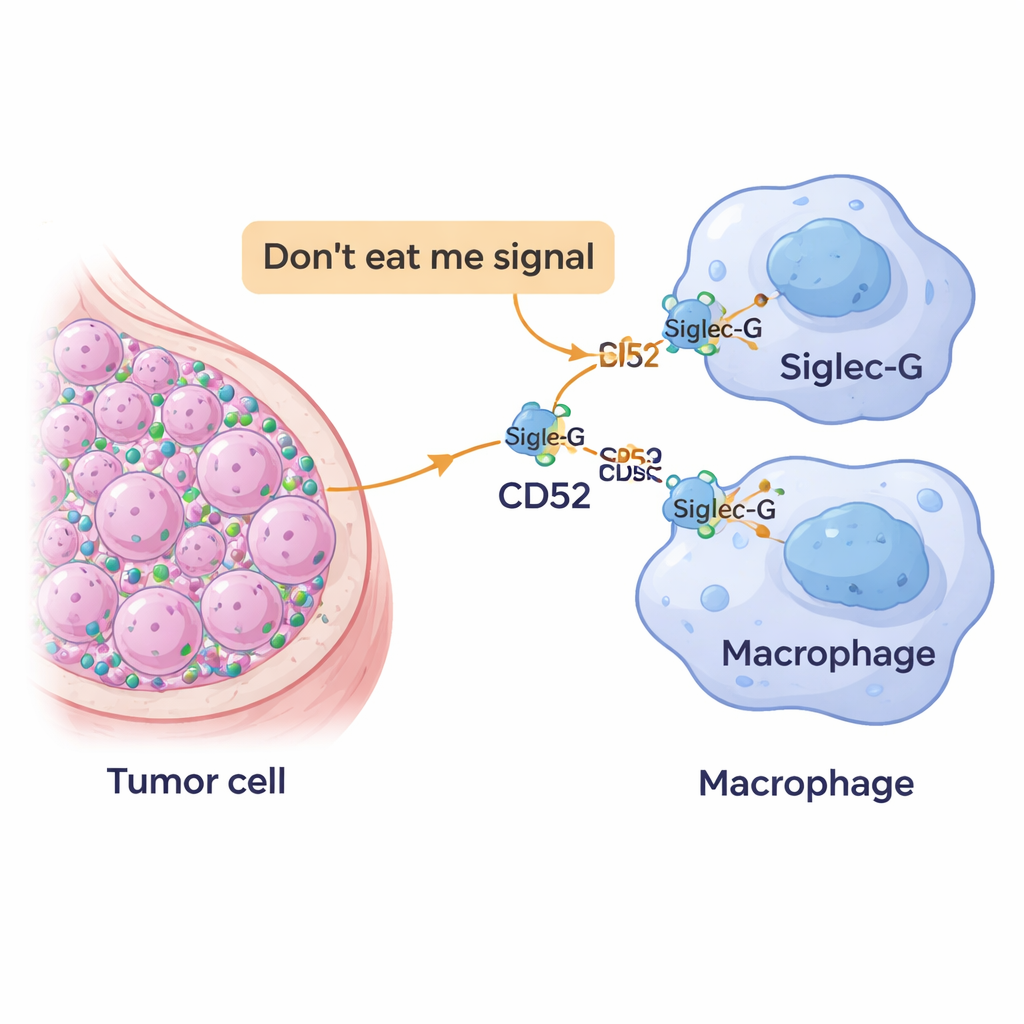
Uma nova “bandeira não me coma” nas células cancerosas
Nosso sistema imune depende de células devoradoras chamadas macrófagos para patrulhar os tecidos e engolir células perigosas ou anormais. Para evitar serem destruídas por engano, células saudáveis exibem marcadores de superfície que sinalizam, em essência, “eu pertenço aqui”. Células cancerosas frequentemente se apropriam desse sistema ao exagerar esses sinais protetores, transformando‑os em poderosas bandeiras de “não me coma”. Os pesquisadores se concentraram em uma molécula chamada CD52, já conhecida em cânceres sanguíneos e doenças autoimunes, e perguntaram se células tumorais de mama também a usam para escapar do ataque de macrófagos.
Detectando CD52 em tumores de mama agressivos
A equipe analisou grandes bancos de dados públicos de câncer e amostras de tecido de pacientes. Eles descobriram que tumores de mama, especialmente os triplo‑negativos, produziam mais CD52 do que o tecido mamário normal. Além disso, tumores com níveis mais altos de CD52 tendiam a ser menos diferenciados, uma característica frequentemente associada a doenças mais agressivas. Ao mesmo tempo, células imunes dentro e ao redor dos tumores exibiam altos níveis de uma molécula parceira chamada Siglec‑10 (e seu equivalente em camundongos, Siglec‑G), que se localiza em macrófagos e pode enviar sinais calmantes para dentro dessas células. Em conjunto, esses padrões sugeriram que o CD52 nas células tumorais poderia estar conversando diretamente com Siglec‑G em macrófagos para impedir que cumprissem sua função.
Desligando o CD52 para libertar os macrófagos
Para testar essa hipótese, os cientistas usaram ferramentas de edição genética para remover o CD52 de células de câncer de mama triplo‑negativo de camundongos. Quando essas células modificadas foram misturadas com macrófagos em laboratório, os macrófagos engoliram significativamente mais células tumorais do que quando enfrentaram células cancerosas não modificadas. Importante, as próprias células cancerosas não cresceram nem morreram de forma diferente após perderem CD52, indicando que o efeito principal era sobre o reconhecimento imune e não sobre a biologia intrínseca das células tumorais. Quando as mesmas células tumorais foram implantadas em camundongos, aquelas sem CD52 formaram tumores menores e ficaram rodeadas por macrófagos que mostraram mais evidências de terem engolido células cancerosas. Se os macrófagos fossem depletados dos camundongos, essa vantagem de crescimento desaparecia, confirmando que o papel principal do CD52 era proteger os tumores de serem devorados.
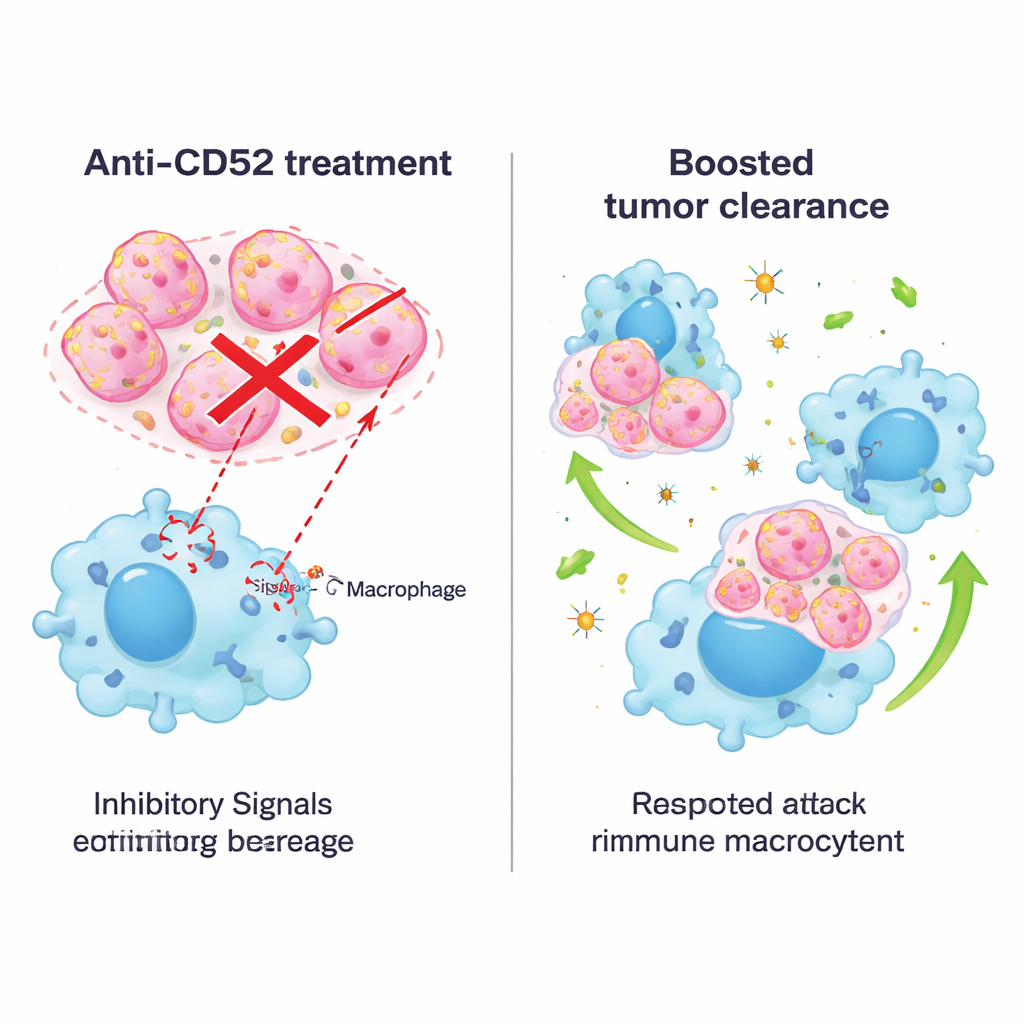
Bloqueando o sinal com anticorpos e combinando tratamentos
Como fármacos que têm como alvo o CD52 já são usados em outras doenças, os pesquisadores testaram em seguida um anticorpo bloqueador em modelos murinos. Tratar camundongos com tumor com um anticorpo anti‑CD52 reduziu o crescimento tumoral, aumentou a sobrevida e não causou danos óbvios a órgãos nem perda de peso. Em placas, anticorpos similares ampliaram a capacidade de macrófagos de camundongo e humanos de engolfar células de câncer de mama de vários subtipos, não apenas triplo‑negativos. A equipe então combinou o bloqueio de CD52 com terapia anti‑PD‑1, um fármaco de checkpoint amplamente usado que atua sobre linfócitos T. Em um modelo espontâneo de camundongo com câncer de mama triplo‑negativo, a combinação funcionou melhor do que qualquer um dos tratamentos isoladamente: os tumores encolheram mais, os macrófagos tornaram‑se mais inflamatórios e ativos, e células T mais potentes capazes de matar o câncer infiltraram o tumor enquanto menos células T exauridas permaneciam.
O que isso significa para o futuro do tratamento do câncer de mama
Este trabalho revela o CD52 como um sinal de “não me coma” até então não reconhecido que células de câncer de mama triplo‑negativo usam para se defender dos macrófagos. Ao interromper a conversa entre CD52 nas células tumorais e Siglec‑G nos macrófagos, os pesquisadores puderam reativar tanto as células imunes inatas quanto, indiretamente, as células T, especialmente quando combinado com bloqueio de PD‑1. Embora sejam necessários mais estudos de segurança e clínicos — porque o CD52 também aparece em muitas células imunes normais — os achados apontam para uma estratégia promissora de duplo checkpoint que pode ajudar a transformar tumores de mama resistentes ao sistema imune em tumores mais responsivos à imunoterapia.
Citação: Qin, X., Chang, Y., Qiu, Y. et al. CD52 signaling via macrophage Siglec-G represents a therapeutic target for cancer immunotherapy. npj Breast Cancer 12, 29 (2026). https://doi.org/10.1038/s41523-026-00895-3
Palavras-chave: câncer de mama triplo-negativo, macrófagos, imunoterapia, CD52, bloqueio de checkpoint